Clear Sky Science · he
הונוקיאול חוסם התפתחות וגידול גרורות באמצעות השפעות ממוקדות במיטוכונדריה
להפוך תרכובת מעץ ללוחם בסרטן
תרופות רבות נגד סרטן מקורן בצמחים, ומדענים ממשיכים לחשוף כיצד חלק מהמולקולות הטבעיות הללו פועלות בתוך תאי הגוף. המחקר הזה מתמקד בהונוקיאול, חומר הנמצא בקליפת עץ המגנוליה ושימש זמן רב ברפואה מסורתית, ומראה כיצד הוא יכול לתקוף ישירות את תחנות הכוח הקטנות בתוך תאי הסרטן, להאט את גדילת הגידול ולחסום את ההתפשטות, תוך פגיעה מועטה יחסית בתאים תקינים.
תחנות הכוח שבתוך התאים שלנו
כל תא מסתמך על המיטוכונדריות, שלעיתים קרובות מכונות "תחנות הכוח" של התא, כדי לייצר את מולקולת האנרגיה ATP. בסרטן, המיטוכונדריות עושות יותר מאשר לייצר דלק—הן עוזרות להכריע האם תא ישרוד או ימות. מכונה מולקולרית גדולה אחת, ATP synthase, ממוקמת בממברנה הפנימית של המיטוכונדריה ומייצרת ATP. בתאים סרטניים, לעתים קרובות מיוצר בכמות גבוהה חלבון שותף בשם IF1, הנצמד ל-ATP synthase ופועל כמו מנעול בטיחות, ועוזר לגידולים להתנגד לצורת מוות התאית הקשורה לפתיחת מעבר חדירות מיטוכונדריאלי ומוות תאי לאחריו.
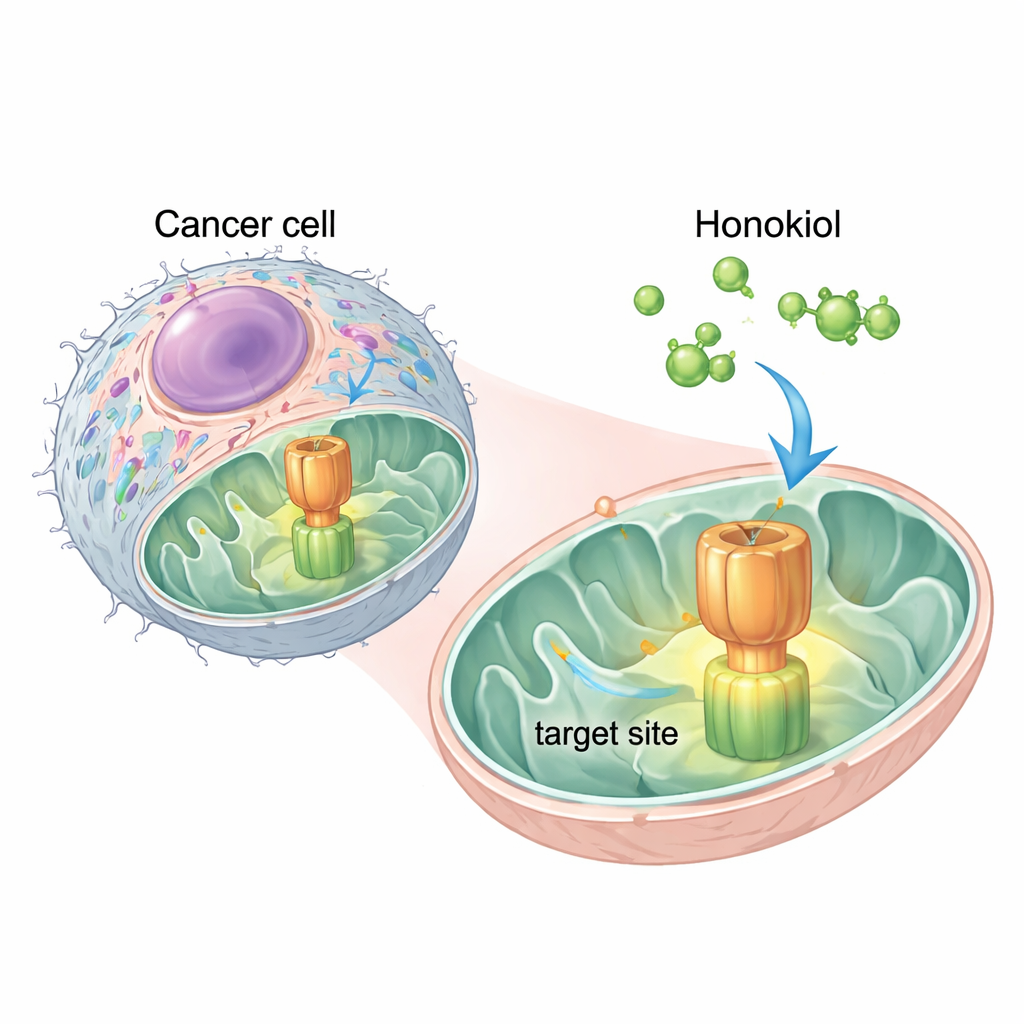
מולקולה טבעית מוצאת מתג קריטי
החוקרים השתמשו בסימולציות מחשב כדי לבדוק היכן עלולה הונוקיאול להיקשר ל-ATP synthase. הם מצאו שני אתרי "עגינה" מבטיחים באחד מרכיביו, אזור שנקרא OSCP. האתר החזק ביותר חפף עם אותו רושם שבו IF1 משתמשת כדי להיאחז ב-ATP synthase. הממצא הזה הציע שהונוקיאול עלול לשמש ככלי יתד מולקולרי, להחדר ל-OSCP ולדחוק את IF1 משם. ניסויים בתאי סרטן צוואר הרחם האנושיים HeLa אישרו רעיון זה: הוספת הונוקיאול הקטינה את המגע הפיזי בין IF1 ל-OSCP, מבלי להפריע לחלקים אחרים של האנזים, מה שמראה שההשפעה הייתה ספציפית.
מתאים חיים לבעלי חיים חיים: פחות גידול, פחות התפשטות
כדי לבדוק האם הדחיפה המולקולרית הזו יש לה השפעה בעולם האמיתי, הצוות השתיל תאי סרטן אנושיים זוהרים בעוברים זברה זעירים, מודל חיה שלם מבוסס למעקב אחר גדילת גידול וגרורתיות. בדגים שהושתלו בתאי HeLa עשירים ב-IF1, טיפול בהונוקיאול הקטין באופן משמעותי את מסות הגידול וצמצם את מספר תאי הסרטן שהתפשטו לאזורים מרוחקים, והדפוס הפך דומה לזה של דגים שהושתלו בתאים בהם IF1 נותקה (IF1‑knockout) וחסר החלבון המגן. באופן מעניין, הונוקיאול גם הפחית את מספר התאים המטסטטיים גם כאשר IF1 היתה חסרה, מה שמעיד על מסלול שני, בלתי תלוי ב-IF1, המגביל את התפשטות הסרטן.
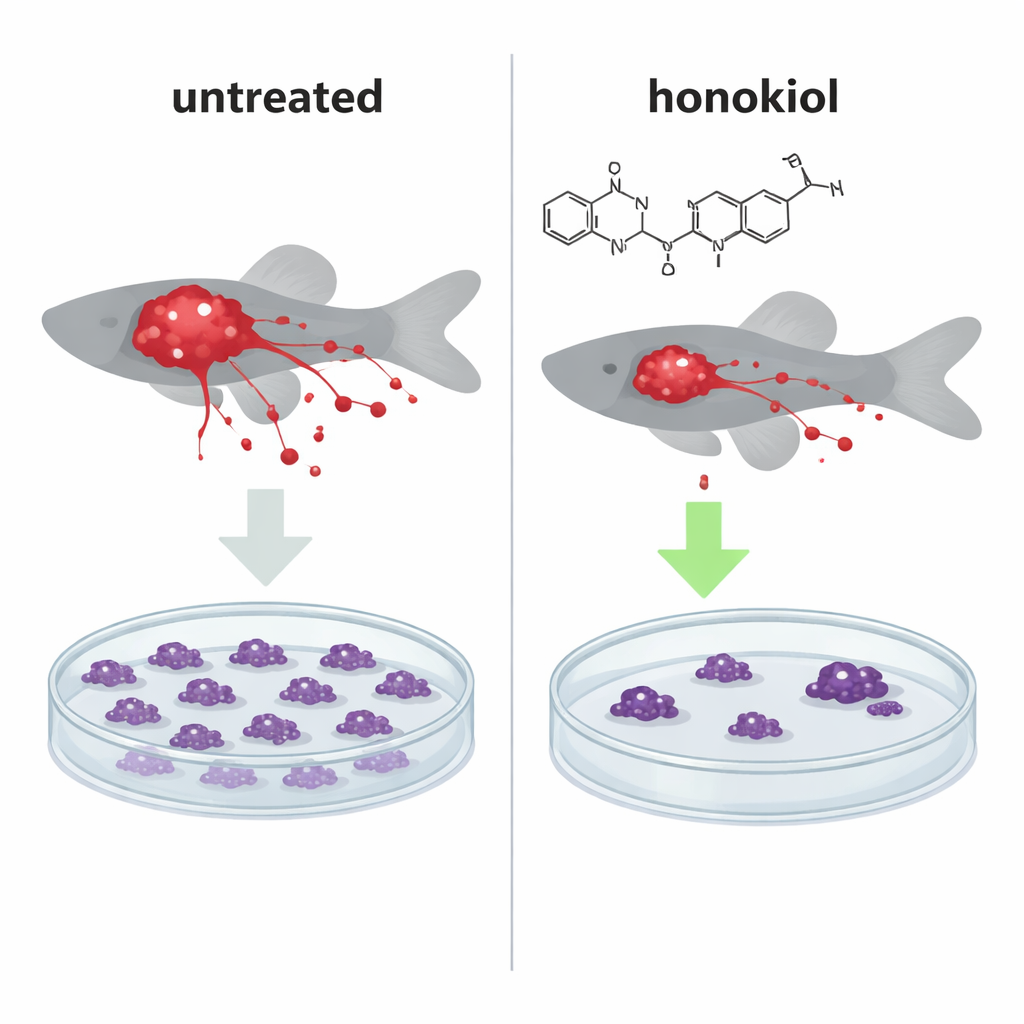
כפייה של תחנות כוח פגומות להפעיל מוות עצמי
בחזרה במבחנה, הונוקיאול הקטין את יכולת תאי הסרטן ליצור מושבות גדולות בגלי-אגאר רך, מבחן שמדמה את התנאים הלוחצים והדלים בחמצן בתוך גידולים מוצקים. זה קרה دون האטה משמעותית בחלוקה התאית הרגילה או בנשימה המיטוכונדריאלית הבסיסית, והצביע במקום זאת על שינוי באופן שבו המיטוכונדריה מקבלת החלטה בין חיים ומוות. מדידות של טיפול בסידן הראו שהונוקיאול הוריד את רמת הסידן שבה המיטוכונדריות כורתות את נקב הפרמיאביליות (mPTP), טריגר ידוע לנפיחות ולשחרור גורמים המקודמים מוות. במינונים מתונים אפקט זה התבסס על העתקת IF1; במינונים גבוהים יותר הונוקיאול פעל דרך אתר הקישור השני ל-OSCP ודרך העלאת רמות של סוגי חמצן תגובתי (ROS), מה שהפך אפילו תאים חסרי IF1 לרגישים למוות מתוכנן.
עיכוב נדידת תאי סרטן
הסכנה הגדולה ביותר של סרטן נובעת מתאי הגידול שנפרדים ונודדים לאיברים חדשים. במבחני "גירוד" המדמים פצע, הונוקיאול האט בעוצמה את ההגירה הקולקטיבית של סדיני תאים סרטניים והקטין סמנים של מעבר אפיתל־מזנכימלי (EMT), תהליך שמצייד תאי גידול ביכולת לנוע ולחדור. תמונות מיקרוסקופ אלקטרוני מפורטות הראו כי תאים נודדים בדרך כלל מגדילים ומשנים את צורת מיטוכונדריותיהם, ומוסיפים קיפולים פנימיים כדי לענות על דרישות אנרגטיות גבוהות בקצה המוביל. בנוכחות הונוקיאול, מיטוכונדריות אלה בקו הקדמי הפכו לנפוחות וניזוקו מבנית—מאפיינים של פתיחת נקב הפרמיאביליות—בעוד שמיטוכונדריות באזורים שאינם נעים הושפעו פחות או אף גדלו במספרן, בהתאם לנוכחות IF1.
מה משמעות הדבר לטיפולים עתידיים בסרטן
פשוטו כמשמעו, עבודה זו מראה שהונוקיאול יכול להגיע לאזור בקרה קטן במכונת ייצור ה-ATP המיטוכונדריאלית ולהפעיל מתג בטיחות מובנה שתאים סרטניים לעתים קרובות שומרים נעול. על ידי גרימת שחרור IF1 ודחיפה ישירה של נקב הפרמיאביליות לכיוון פתיחה, הונוקיאול מעודד תאי גידול לבצע מוות עצמי ומקשה עליהם להגר ולזרוע גרורות. כיוון שההשפעות נובעות מתכונות שמשותפות לרבים מסוגי הסרטנים—ולא מסמן יחיד על פני התא—מיקוד באזור OSCP של ATP synthase עשוי להניע יצירת כיתה חדשה של טיפולים שמנצלים את הפגיעויות של תחנות הכוח בתאי הסרטן תוך הגבלת הנזק לרקמות בריאות.
ציטוט: Grandi, M., Boldrin, F., Risato, G. et al. Honokiol blocks tumor development and metastasis through mitochondrion-targeted effects. Cell Death Dis 17, 186 (2026). https://doi.org/10.1038/s41419-026-08441-6
מילות מפתח: הונוקיאול, מיטוכונדריות, ATP synthase, אפופטוזה, גרורתיות