Clear Sky Science · he
פנאומוניטיס הקשורה למעקבי המערכת החיסונית: התקדמות עדכנית והתפקיד האפשרי של טיפול בתאי גזע מזנכימליים
כאשר טיפול בסרטן פוגע בריאות
תרופות שמשחררות את מערכת החיסון נגד סרטן שינו את הטיפול במחלות כמו סרטן הריאה ומלנומה. עם זאת, הכוח החדש הזה מגיע עם מחיר: אצל חלק מהמטופלים אותה תגובת חיסון שמכוונת לגידולים יכולה גם להפנות את הפעילות אל הריאות ולגרום למצב הנקרא פנאומוניטיס הקשורה למעקבי המערכת החיסונית (ICIP). הסקירה הזו מסבירה מהי ICIP, מדוע היא מתרחשת, איך המטפלים מטפלים בה כיום, ולמה סוג מיוחד של תאי גזע — תאים מזנכימליים (MSCs) — עשוי בעתיד להציע דרך בטוחה וממוקדת יותר להרגיע את הסערה מבלי לפגוע בשליטה על הסרטן. 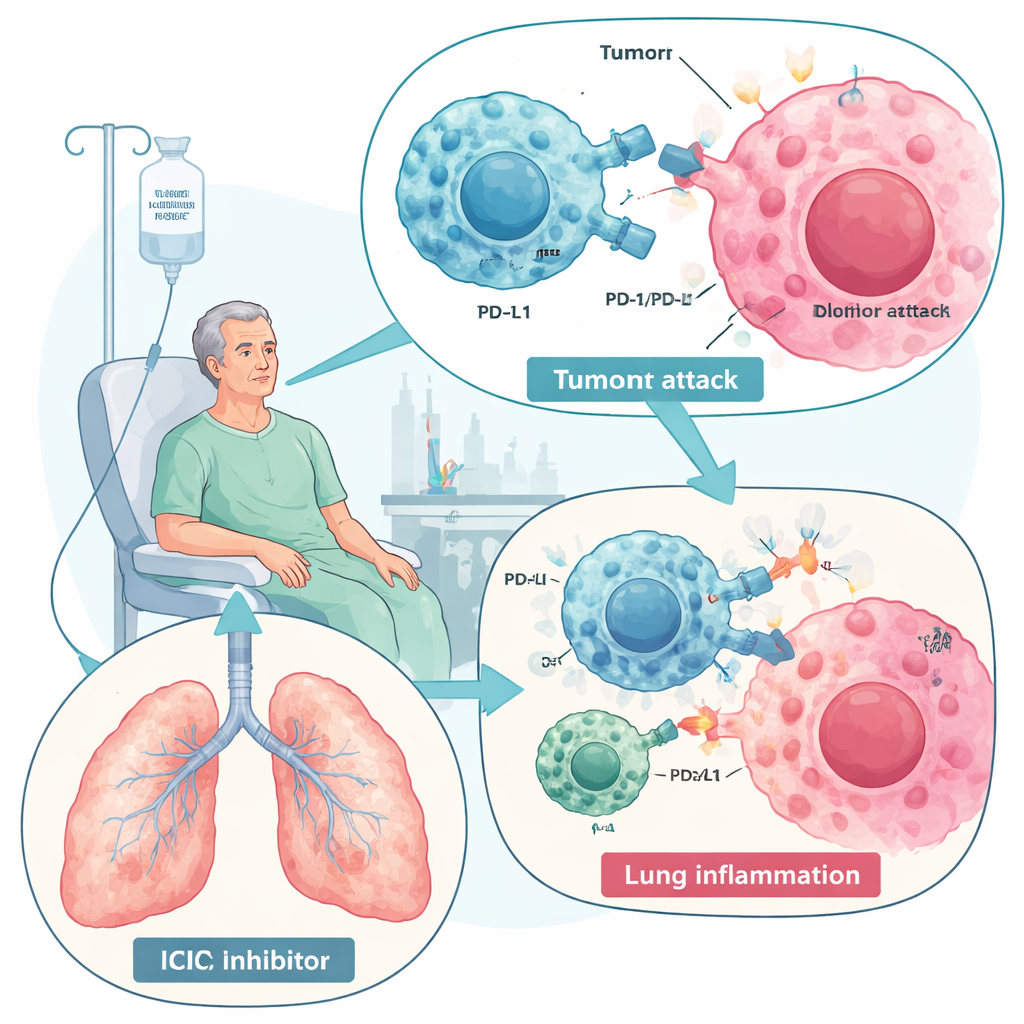
תרופות סרטן עוצמתיות עם סיכון ריאתי סמוי
מעכבי נקודות הבדיקה של המערכת החיסונית, ובמיוחד אלה החוסמים PD-1 ו-PD-L1, פועלים על ידי הסרת "בלמים" מולקולאריים שמגבילים בדרך כלל תגובות חיסוניות. כשמוסירים את הבלמים, תאי T מזהים והורסים טוב יותר תאי סרטן, ומשפרים הישרדות בסוגי גידול רבים. אך אותו חיזוק עלול לשבור סבילות נורמלית ולגרום לתופעות לוואי חיסוניות במערכות איברים שונות. ICIP היא הסיבוך הריאתי החמור ביותר של תרופות אלו ואחת הסיבות המובילות לתמותה הקשורה לתגובות חיסוניות לטיפול. שיעור ההשפעה נע ממספר אחוזים ועד כמעט שליש מהמטופלים במחקרים מעשיים מסוימים, במיוחד אצל חולי סרטן ריאה או כאלה עם מחלת ריאות קיימת כגון COPD או מחלת interstitial. התסמינים נעים משיעול קל וקוצר נשימה עד לכשל נשימתי מסכן חיים.
כיצד המערכת החיסונית פוגעת בריאה
הסקירה מתארת את ICIP כתוצאה מאיזון חיסוני מופרע בתוך הריאות. תאים "לוחמים" פעילות יתר — תאי T CD8, סוגים מסוימים של תאי T עוזרים, מאקרופאגים דלקתיים, נויטרופילים ותאי טבעיים לרצח — מוצפים ברקמת הריאה ומשחררים חלבוני איתות אגרסיביים, כולל אינטרפרון‑גמא, TNF‑אלפא, וציטוקינים כגון IL‑6 ו-IL‑17. במקביל, תאים שמגוננים בדרך כלל ומרגיעים דלקת, כגון תאים רגולטוריים מסוג T ומאקרופאגים מתמקדי-תיקון, מופחתים. אצל חלק מהמטופלים נצפים גם רמות גוברות של נוגדנים עצמיים לפני או במהלך הטיפול, מה שמעיד כי ICIP עשויה בדמיון להיות חלקית למחלה אוטואימונית. בנוזל שהושקע מהריאות מוצאים רופאים דפוס דלקתי עשיר בתאי T ותמהיל ציטוקינים שונה מזה של זיהום או התקדמות גידול, דבר שעשוי לסייע באבחון.
זיהוי, דירוג וטיפול בנזק
בסריקות CT, ICIP בדרך כלל מופיעה כשטחים מעומעמים מסוג "זכוכית טבועה" או כעיבושים מקוטעים המפוזרים בשתי הריאות, דפוסים השונים מנזק קרינתי שנשאר בתחום המוכתם בלבד. הרופאים מאבחנים ICIP על ידי שילוב ממצאי סריקה, תסמינים, והדרה קפדנית של זיהום וסיבות אחרות. קווי מנחה בינלאומיים מדרגים את החומרה מ-1 (קל, לעיתים רק רדיולוגי) עד 4 (כשל נשימתי מסכן חיים). הבסיס של הטיפול היום הוא גלוקוקורטיקואידים — סטרואידים אנטי‑דלקתיים עוצמתיים — שלעיתים משולבים עם מדכאי חיסון אחרים כמו טוביליזומאב (חוסם IL‑6) או אינפליקסימאב (חוסם TNF‑אלפא) במקרים קשים או עמידים לסטרואידים. גישות אלה יכולות להציל חיים, אך הן כלים גסים: לסטרואידים יש תופעות לוואי רבות, חלק מהמטופלים אינם מגיבים, ודיכוי חיסוני רחב עלול להחליש את תגובת האנטי‑גידול שהתרופות נועדו לחזק.
מדוע תאי גזע נכנסים לשיח
תאים מזנכימליים, שניתן לכרותם ממח עצם, שומן או רקמת חבל הטבור, עלו כ"ממודלטורי חיסוני" מבטיחים במקום פשוט בנאים של רקמה. כאשר מוזרקים לזרם הדם, רבים מהתאים נלכדים זמנית בכלי הדם הדקים של הריאה — מה שנקרא אפקט הפרוסה הראשונה — שמום יתרון לטיפול באיברים מרוחקים אך יתרון פוטנציאלי למחלת ריאה. במודלים בעכבר וניסויים אנושיים מוקדמים במצבים כמו דלקת ריאות קשה, תסמונת מצוקה נשימתית חריפה, מחלות דלקתיות של המעי ומחלת השתל נגד המאכסן, MSCs מורידים תגובות חיסוניות-יתר, מזיזים את מאזן התאים החיסוניים לעבר מצב מאוזן יותר ומשחררים גורמי גדילה המעודדים תיקון רקמה תוך הגבלת צלקת. חשוב: היתרון שלהם נובע לעיתים קרובות לא מהבדילה לתאי ריאה, אלא מתערובת מולקולות האיתות וחלוקיות מזעירות שהם משחררים. 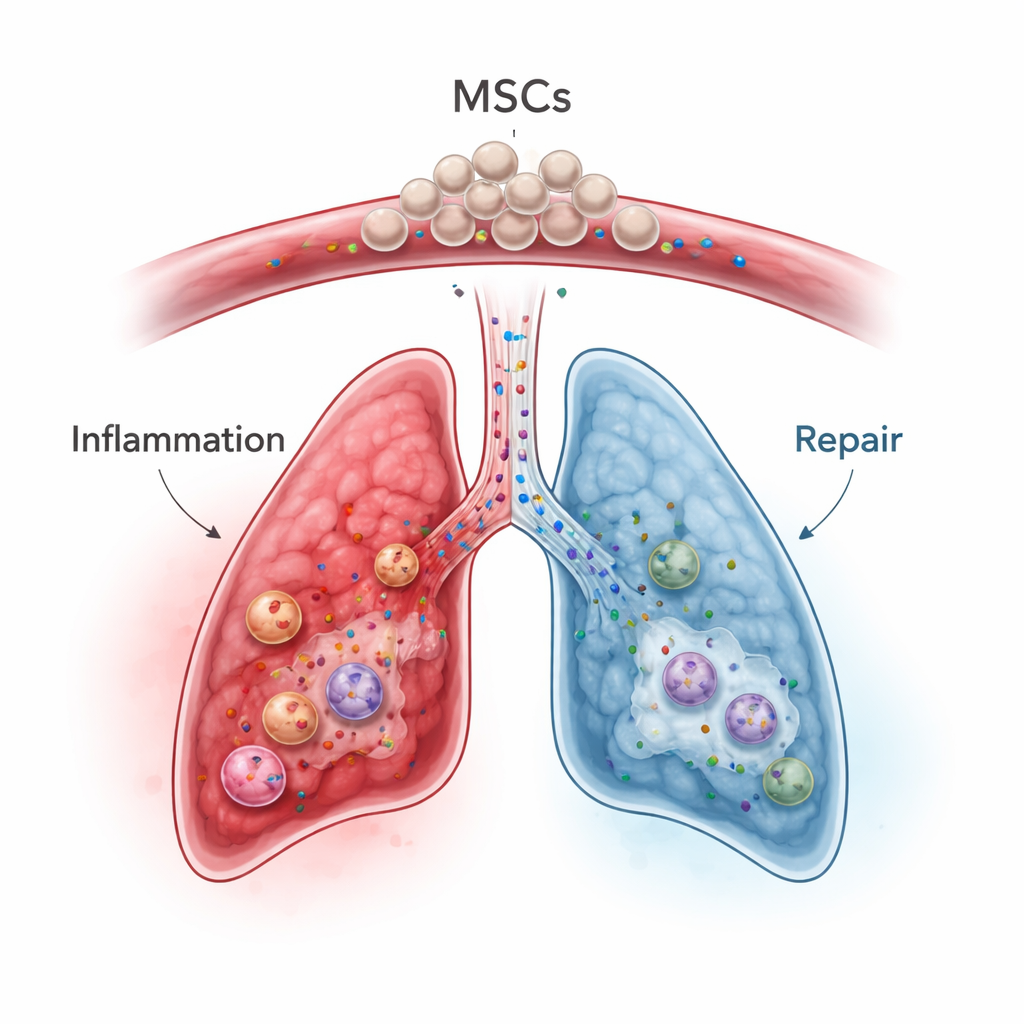
כיצד MSCs עשויים להרגיע ICIP מבלי להרוס את הריפוי
בהקשר של ICIP, MSCs עשויים, בעקרון, לטפל בכמה בעיות במקביל. הם יכולים להגביל ישירות תאי T פעילים, לקדם את צמיחת ותפקוד תאי T רגולטוריים, ולכוון מאקרופאגים ממצב תוקפני ופוגע ברקמה למצב מרפא ותומך. הם גם מורידים מוליכי דלקת מרכזיים כגון IL‑6, IL‑1β ו-TNF‑אלפא, ומגבירים גורמים אנטי‑דלקתיים וחלבונים מגןיים כמו TSG‑6 שעוזרים להגביל פגיעה ורקמת צלקת ריאתית. מחקרים קדם‑קליניים מציעים ש-MSCs או אקסוזומים הנגזרים מהם יכולים להקטין סופות ציטוקינים ונזק לאיברים שנגרמו על ידי מעכבי נקודות ביקורת או קרינה, בעוד שבכמה הגדרות שומרים טוב יותר על פעילות אנטי‑גידול בהשוואה לדיכוי חיסוני סטנדרטי. עם זאת, המחברים מזהירים ש-MSCs עשויים גם לקיים אינטראקציות מורכבות עם גידולים ועם קרישת דם, ושאפקטיהם תלויים במידה רבה בסביבה הדלקתית המקומית ואפילו במקור ה‑MSC (מח עצם, רקמת שומן או חבל טבור).
מבט קדימה: הבטחה שדורשת בדיקה זהירה
למטופלים שטיפולם בסרטן נעצר או מאוים על ידי רעילות ריאתית חמורה, טיפולים מבוססי MSC עשויים בסופו של דבר לספק דרך ממוקדת יותר לקרר דלקת, לתקן רקמת ריאה ולמנוע צלקת ארוכת‑טווח — ובאידיאל ללא ביטול היתרונות שמצילת החיים של מעכבי נקודות הבדיקה. עם זאת, טרם הושלמו ניסויים ספציפיים ב‑ICIP עם MSCs. המחברים טוענים שיש צורך דחוף במחקרים חיות ובניסויים קליניים מתוכננים בקפידה כדי להגדיר איזה סוג MSC או מוצר אקסוזומים עובד הטוב ביותר, כמה לתת, מתי לתת ביחס לסטרואידים ולאימונותרפיה, וכיצד לנטר סיכונים כמו גדילת גידול או קרישה. עד אז, MSCs נשארים אפשרות מלאת תקווה אך עדיין ניסיונית באופק לניהול תופעת הלוואי החמורה הזו של טיפול סרטן מודרני.
ציטוט: Li, Z., Zheng, X., Xia, H. et al. Immune checkpoint inhibitor-related pneumonitis: current advances and the putative role of mesenchymal stem cell therapy. Cell Death Dis 17, 200 (2026). https://doi.org/10.1038/s41419-026-08440-7
מילות מפתח: תופעות לוואי של אימונותרפיה, פנאומוניטיס, מעכבי נקודות ביקורת, תאי גזע מזנכימליים, דלקת ריאות