Clear Sky Science · he
BCL-xL כיעד טיפולי בסרטן המעי הגס העמיד לצטוקסימאב
מדוע זה חשוב לאנשים עם סרטן המעי הגס
סרטן המעי הגס והחלחולת הוא אחד הסוגים השכיחים ביותר של סרטן בעולם, ומטופלים רבים עם מחלה מתקדמת מקבלים נוגדן ממוקד בשם צטוקסימאב. תרופה זו יכולה להקטין גידולים בתחילה, אך אצל רוב החולים הסרטן מוצא דרכים להתחמק בתוך חודשים, ומשאיר לרופאים מעט אפשרויות טובות. המחקר הזה שואל שאלה דחופה: כשהגידולים מפסיקים להגיב לצטוקסימאב, האם קיים נקודת תורפה נוספת שתרופות חדשות יכולות לנצל כדי להביא למות תאי הסרטן?
כשתרופה ממוקדת מפסיקה לעבוד
צטוקסימאב פועל על ידי חסימת אנטנה חיצונית בתאי הסרטן שנקראת קולטן ל-EGF (EGFR), אשר מקדם את גדילתם. החוקרים בנו מודל מעבדה של עמידות על ידי חשיפת קו תאי סרטן המעי הרגיש (LIM1215) למינונים הולכים ועולים של צטוקסימאב במשך שישה חודשים. הופיעו שתי אוכלוסיות תאים עמידות שיוכלו להמשיך לגדול גם ברמות גבוהות של התרופה, ובו־זמנית נראו בריאות ומהירות גדילה כמו התאים המקוריים כשהתרופה הוסרה. משמעותית, התאים העמידים עדיין נשאו על פני השטח את המטרת התרופה וצטוקסימאב עדיין יכול לקשור אותה, מה שמרמז שהסרטן לא פשוט "הסתיר" או שינה את הקולטן.
תאים עמידים מנתבים מחדש את אותות הגדילה שלהם
בכדי להבין כיצד התאים עקפו את צטוקסימאב, החוקרים בחנו מסלולי גדילה מרכזיים בתוך התא. בתאים ההורים צטוקסימאב כרגיל החליש את מסלול ה-MAPK, מנוע מרכזי לחלוקה תאית. בתאים העמידים פעילות MAPK נשמרה גבוהה גם כאשר EGFR נחסם, מה שמראה שאות הגדילה הופרה מקשרו עם הקולטן המקורי. רצפי RNA של התאים חשפו מוטציות פעילות חדשות בגֵן RAS נוסף, HRAS, בתתי־אוכלוסיות של התאים העמידים, אך לא במחשודים הרגילים כמו KRAS, NRAS או BRAF. ניסיונות לשתק את אות ההסלמה הזה בעזרת מעכב MEK (העובד במטה‑RAS) הקטינו את הגדילה באופן מתון בלבד. זה הדגיש כי במקום לרדוף אחרי כל מוטציה חדשה, ייתכן שיותר יעיל לתקוף את מנגנוני החיים והמוות התאית המשותפים לשכבות שונות של תאים עמידים. 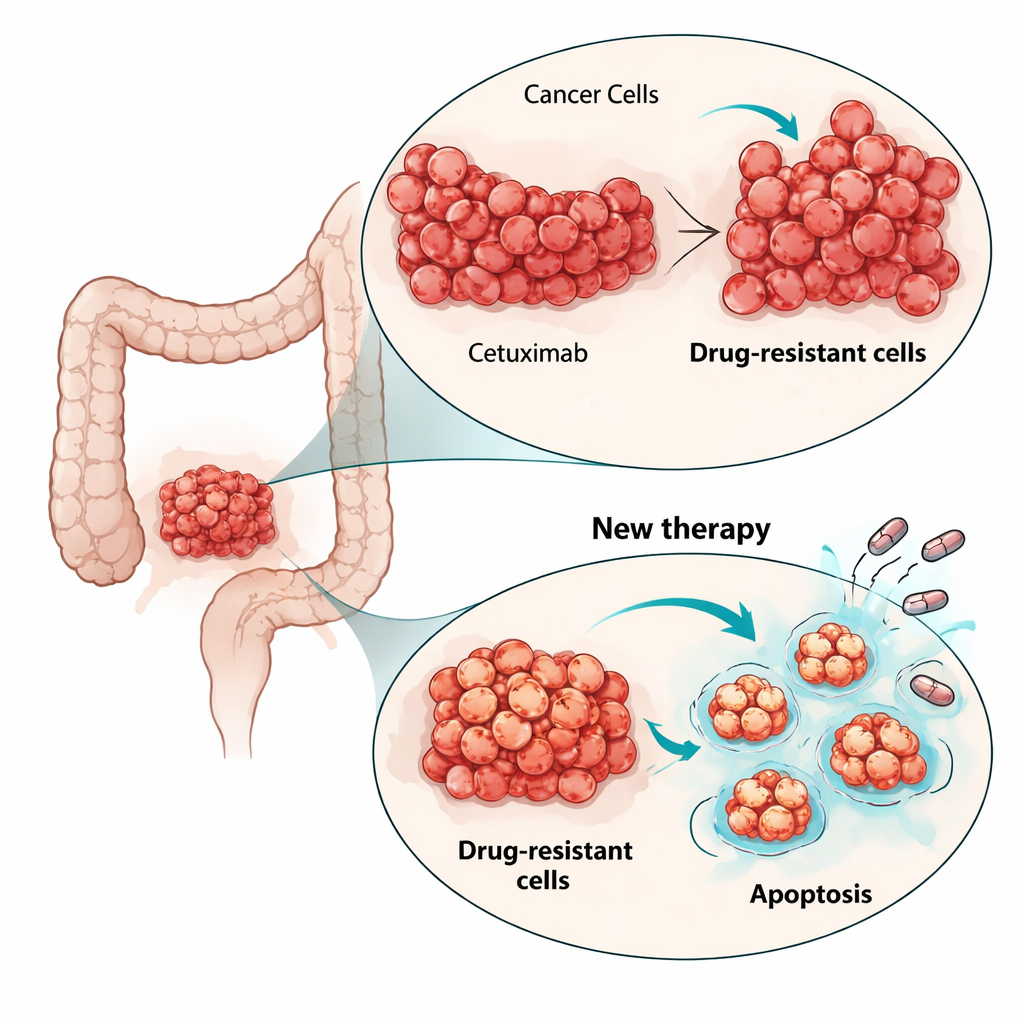
לחיצה על מערכת התמיכה החיים של הסרטן
המדענים הפנו את המבט שלהם לאפופטוזיס, תכנית ההתאבדות התאית המובנית שסרטנים לעתים קרובות מדכאים. ניתוח ביטוי גנים הראה שמסלולי אפופטוזיס שונו בתאים העמידים. במיוחד, החלבון המונע־מוות BCL-xL היה גבוה באוכלוסייה עמידה אחת ובעל עלייה מתונה בשנייה, בעוד חלבון הישרדות נוסף, MCL-1, היה גם הוא נוכח. הצוות בחן מולקולות קטנות שנקראות חיקויי BH3 שנועדו לחסום חלבוני הישרדות אלה ולשחרר את מנגנון המוות. בתרבויות דו־ממדיות כל שלוש שורות התאים — ההורית והעמידות — הראו רגישות לתרופות החוסמות BCL-xL או MCL-1, אך באופן בולט מינונים נמוכים יותר הרגו את התאים העמידים לצטוקסימאב ביעילות רבה יותר. הוספת מינון נמוך של מדכא הפרוטאוזום בורטזומיב, שעוזר להצטברות אותות פרו‑מוות, הגברה עוד יותר את ההרג, במיוחד בשילוב עם החוסם של MCL-1.
מצלחות שטוחות למיני‑גידולים תלת־ממדיים ולרקמות מטופלים
מכיוון ששכבות תאים שטוחות אינן משכפלות במלואן גידולים בגוף, הצוות לאחר מכן גדל את התאים כספירואידים תלת‑ממדיים המשתקעים בג'ל, המשקפים טוב יותר את הארכיטקטורה ואת אתגרי החדירה של תרופות בגידולים אמיתיים. שוב, חסימת BCL-xL או MCL-1 הפחיתה את חיות הספירואידים, ושילוב התרופות עם בורטזומיב גרם לצניחה דרמטית בפעילות המטבולית וסימני מוות תאי ברורים. כדי לבדוק האם פגיעות זו קיימת בחומר גידולי אנושי מציאותי יותר, השתמשו בפרוסות דקות של גידולים עמידים לצטוקסימאב שגודלו בעכברים ממקור גידולי חולים (patient-derived xenografts). מודלים אלה היו כולם מסוג KRAS בר־טיפוס כמו תאי LIM1215 המקוריים אך נשאו מוטציות נוספות שונות, כולל ב‑BRAF ו‑TP53, המשקפות את המגוון הגנטי הנצפה במרפאה. 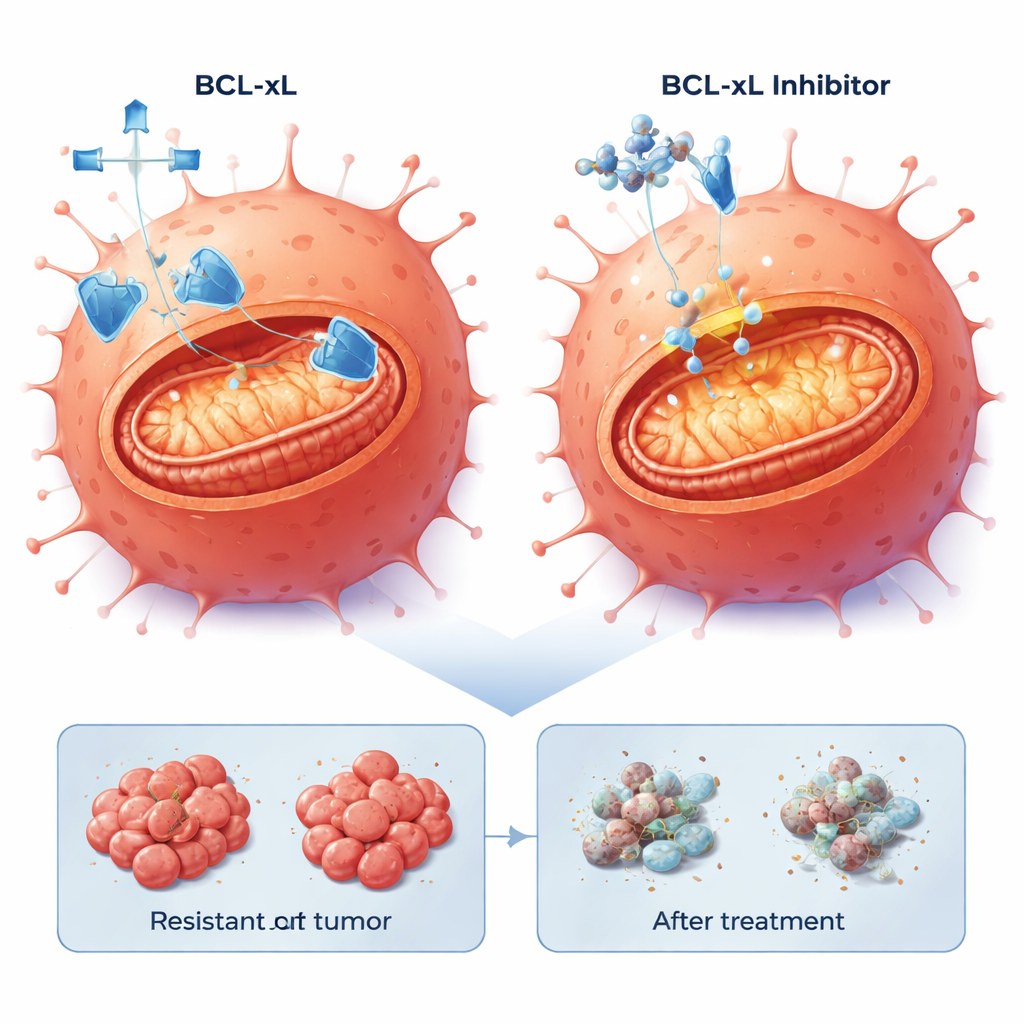
מיקוד ב‑BCL-xL עובד במגוון גידולים עמידים
בפרוסות הגידול המופקות מחולים, השילוב של מעכב BCL-xL עם מינון נמוך של בורטזומיב עורר בעקביות מוות תאי חזק ב‑20–40% מתאי הגידול בארבעה מודלים שונים, כולל אלה עם מוטציות אגרסיביות ב‑BRAF. לעומת זאת, חסימת MCL-1 יחד עם בורטזומיב הראתה השפעות חזקות רק בתת‑קבוצה של גידולים. חשוב לציין שהיכולת של תאים עמידים לחוות אפופטוזיס נשמרה: ברגע שנטרלה רשת הביטחון של BCL-xL, תוכנית המוות הפנימית יכלה עדיין להתפעול, ללא תלות בדרך הגנטית הספציפית שהגידול בחר כדי להימלט מצטוקסימאב.
מה זה אומר עבור מטופלים
לאנשים שסרטן המעי הגס שלהם מפסיק להגיב לצטוקסימאב, המחקר הזה מציע אופטימיות זהירה. הוא מצביע על כך שגם לאחר שהגידולים מפתחים עמידות לטיפול ממוקד ב‑EGFR, תאים רבים עדיין מוכנים למות אם יחסום חלבון הישרדות מרכזי, BCL-xL. מעכבי BCL-xL עלולים לגרום לתופעות לוואי, במיוחד על טסיות הדם, אך העבודה מצביעה על אסטרטגיות של שילוב ואופטימיזציית מינון שיכולות להגביל רעילות ובו־זמנית לנצל נקודת תורפה משותפת של גידולים קשים לטיפול. בעתיד, תרופות שמנטרלות את BCL-xL עשויות להוות את עמוד השדרה של טיפולים קו שני חדשים לסרטן המעי הגס העמיד לצטוקסימאב, פחות תלויות בנוף המוטציות המשתנה של הגידול.
ציטוט: Asmanidou, S., Thiel, J., Ekstrom, T.L. et al. BCL-xL as a therapeutic target in cetuximab-refractory colorectal cancer. Cell Death Dis 17, 187 (2026). https://doi.org/10.1038/s41419-026-08434-5
מילות מפתח: סרטן המעי הגס, עמידות לתרופות, צטוקסימאב, עיכוב BCL-xL, אפופטוזיס