Clear Sky Science · he
מיקוד ב-IGFBP2 אקסוזומלי בהיפוקסיה מתגבר על התחמקות חיסונית בתיווך CD47 בגְּלִיובְּלַסטוֹמָה
מדוע גרימת רעב לחמצן בגידול עלולה לחזור כבומרנג
רופאים ידעו זמן רב שגליובלסטומה, סרטן מוח קטלני, לעתים קרובות גדל באזורים המצומצמים בחמצן. כיסי היפוקסיה אלה מקשים על הטיפול בגידול. המחקר הזה מגלה כיצד רמות חמצן נמוכות מסייעות לתאים סרטניים להסתיר עצמם ממערכת החיסון, ומציע טיפול משולב חדש שעשוי להפוך אותם לנגישים יותר להתקפה על-ידי הגוף.
גידול מוחי קטלני שמתחמק ממערכת ההגנה שלנו
גליובלסטומה הוא הגידול המוחי ההתנהגותי ביותר ובשכיחותו במבוגרים, עם הישרדות אופיינית הנמדדת בחודשים. אף על פי שתאי חיסון חודרים לגידולים אלה, תאי הסרטן לעתים קרובות מתחמקים מהשמדתם. נתיב מפתח להתחמקות הוא חלבון ממברנלי בשם CD47, המכונה לפעמים אות "אל תאכלו אותי", שמאותת למקרופאגים ותאי חיסון סמוכים שלא לבלוע ולהשמיד את תא הגידול. תרופות החוסמות את CD47 כבר נבחנות, אך התוצאות בגידולים מוצקים כמו גליובלסטומה היו מעורבות, מה שמרמז כי גורמים נוספים בסביבת הגידול עלולים לערער על היעילות של טיפולים אלה.
אזורי היפוקסיה וחבילות קטנטנות של סרטן
באמצעות ריצוף RNA בתא-יחיד, החוקרים מיפו אלפי תאים מאזורים שונים בדגימות גליובלסטומה, והשוו בין הליבה הדלה בחמצן לשפה החיצונית של הגידול. הם מצאו תת-סוג תאי תוקפני במיוחד בליבת ההיפוקסיה, הקרוי תאים בדמיון מזנכימלי של GBM, שהביעו בחוזקה CD47 וחלבון בשם IGFBP2. במקביל גילו כי תאי הליבה האלה משחררים מספר רב של וניקולות בגודל ננו המכונות אקסוזומים, שנושאות על פני השטח שלהן את IGFBP2. מאחר שאקסוזומים יכולים להסתעף במוח ואפילו לחדור לזרם הדם, הם יכולים להפיץ אותות הרבה מעבר למקום ייצורם. 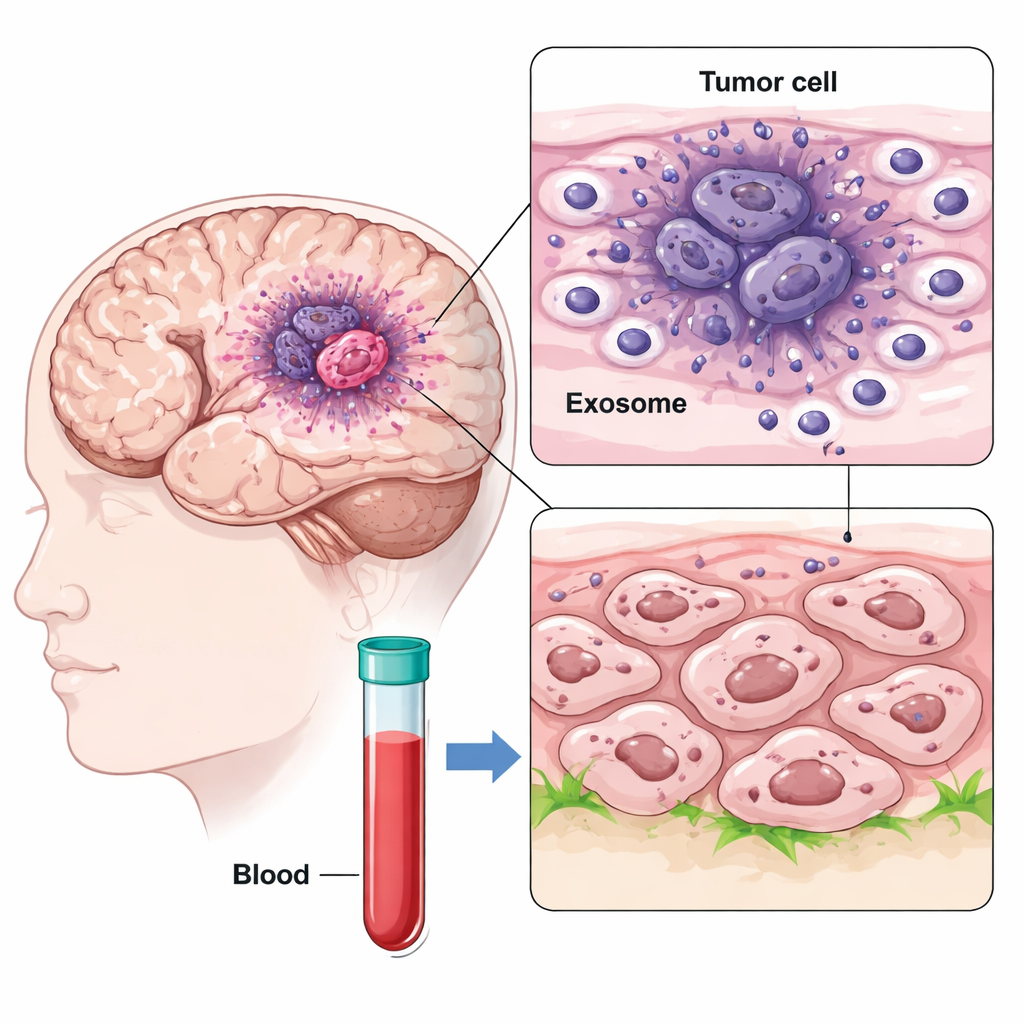
כיצד חלבון שותף מחזק את אות "אל תאכלו אותי"
הצוות חקר אז מה תפקידו של IGFBP2. הם הראו שתחת חוסר חמצן, חלבון חישה של היפוקסיה בשם HIF-2α מפעיל את הגן של IGFBP2 בתאי הגידול. לאחר מכן IGFBP2 נקשר לקולטנים ספציפיים מסוג אינטגרינים על פני האקסוזומים, ומקשט את הממברנה החיצונית שלהם. כאשר אקסוזומים מצופים ב-IGFBP2 מתמזגים עם תאים סרטניים אחרים, הם מפעילים קסקדה של אותות תוך-תאיים הכוללת חלבונים הידועים כ-FAK ו-STAT3. קסקדה זו בסופו של דבר מעלה את כמות ה-CD47 על פני תא הגידול, ומחזקת את המסר "אל תאכלו אותי" למקרופאגים ומספקת הגנה נוספת לתאים הסרטניים מפני התקפה חיסונית. 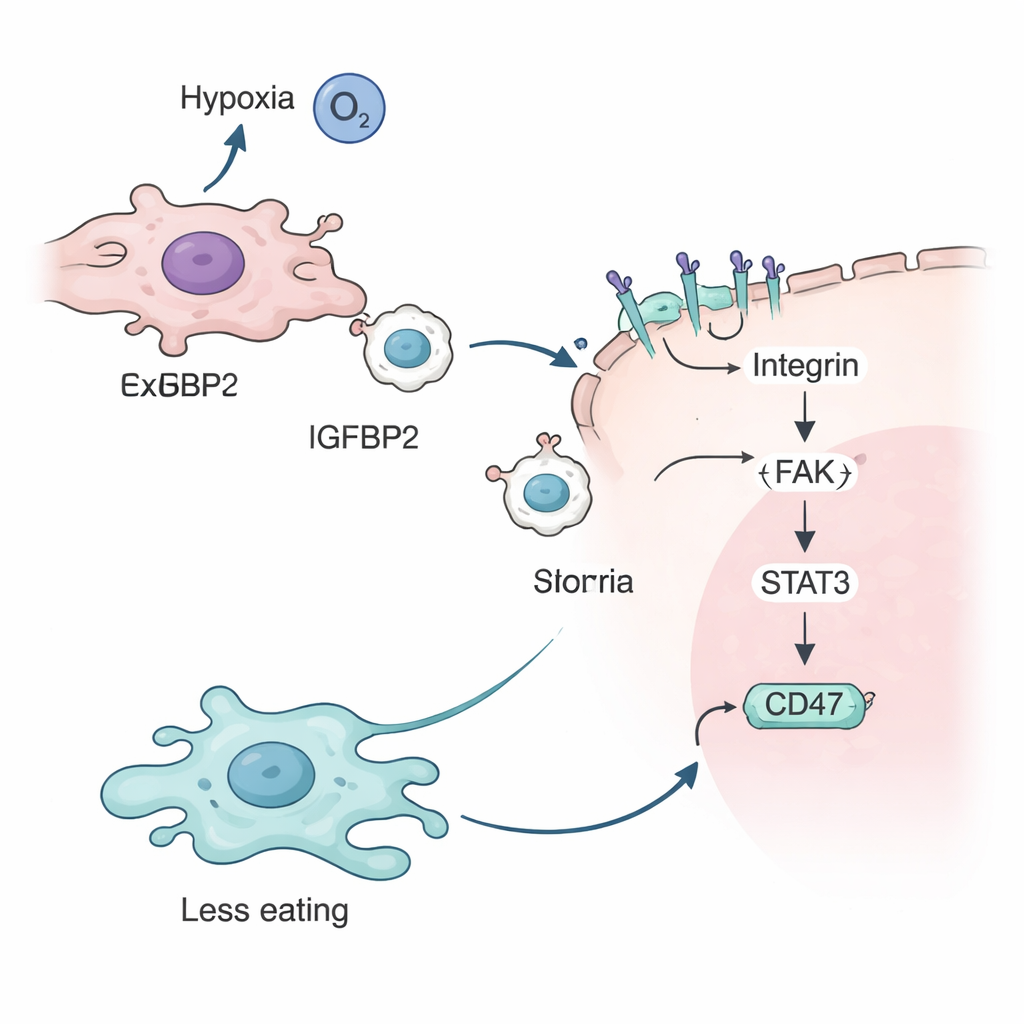
ראיות מתרביות מטופלים ומדגמי בעלי חיים
כדי לקשר ממצאים במעבדה למחלה אמיתית, החוקרים בחנו רקמות גידול ודם מאנשים עם גליאומה. הם מצאו שרמות IGFBP2 היו גבוהות יותר גם בגידולים וגם באקסוזומים בדם של מטופלים עם מחלה מתקדמת יותר, מה שמרמז שאקסוזומים חיוביים ל-IGFBP2 עשויים לשמש כסמן מוגדר בדם למידת החומרה של הגידול. במודלים עכבריים, הפחתת רמות IGFBP2 בתאי גליובלסטומה הפכה אותם לפגיעים יותר לבליעה על-ידי מקרופאגים, האטה את גדילת הגידול והאריכה את ההישרדות. להפך, הוספת אקסוזומים עשירים ב-IGFBP2 הגבירה את רמות ה-CD47, הקטינה את בליעת תאי החיסון והאיצה את התקדמות הגידול.
מכה מבטיחה בשני אפיקים לטיפול
לבסוף, הצוות בדק האם חסימת IGFBP2 יכולה להפוך טיפול המכוון CD47 ליעיל יותר. בעכברים עם גידולי מוח, טיפול בנוגדנים נגד גם IGFBP2 וגם CD47 הוביל לפעילות מקרופאגית חזקה יותר, גידולים קטנים יותר והישרדות ארוכה יותר מאשר כל אחד מהטיפולים בנפרד. על ידי ניתוק אות IGFBP2 המונע על-ידי היפוקסיה וחסימת אות ה"אל תאכלו אותי" של CD47 ישירות, הטיפול המשולב תקף את מסווה החיסון של הגידול משתי חזיתות. עבור מטופלים, הממצאים האלה מציעים כי מדידת IGFBP2 באקסוזומים בדם עשויה לעזור לזהות את אלה הסבירים להפיק תועלת מתחליפי חיסון מבוססי CD47, וכי שילוב מעכבי IGFBP2 ו-CD47 יכול להיות אסטרטגיה חזקה יותר נגד גליובלסטומה מאשר כל תרופה בנפרד.
ציטוט: Qi, Y., Zhao, R., Zhang, X. et al. Targeting hypoxic exosomal IGFBP2 overcomes CD47-mediated immune evasion in glioblastoma. Cell Death Dis 17, 192 (2026). https://doi.org/10.1038/s41419-026-08430-9
מילות מפתח: גליובלסטומה, אקסוזומים, התחמקות חיסונית, CD47, היפוקסיה