Clear Sky Science · he
עצירת מחזור התא ב-G0/G1 בתיווך p16 מובילה ל-SASP ולסיבוך ברקמת חיבור בדיסטורפיה האנדותליאלית של הקורניאה מסוג פוכר
מדוע המחלות העיניים האלה חשובות
במהלך ההזדקנות, אחד האיומים הפחות-מוכרים על הראייה הוא מצב הנקרא דיסטורפיה אנדותליאלית של הקרנית מסוג פוכר (FECD), שמטשטש בהדרגה את החלון הקדמי של העין שנמצא בדרך כלל צלול. המאמר חוקר מדוע תאים מסוימים על המשטח הפנימי של הקרנית מתשמשים ויוצרים צלקות עם הזמן, ומדוע נשים נפגעות בתדירות גבוהה יותר. הבנת השינויים הנסתרים הללו עשויה לפתוח דלת לפיתוח תרופות שיאחרו או אפילו ימנעו את הצורך בהשתלות קרנית.
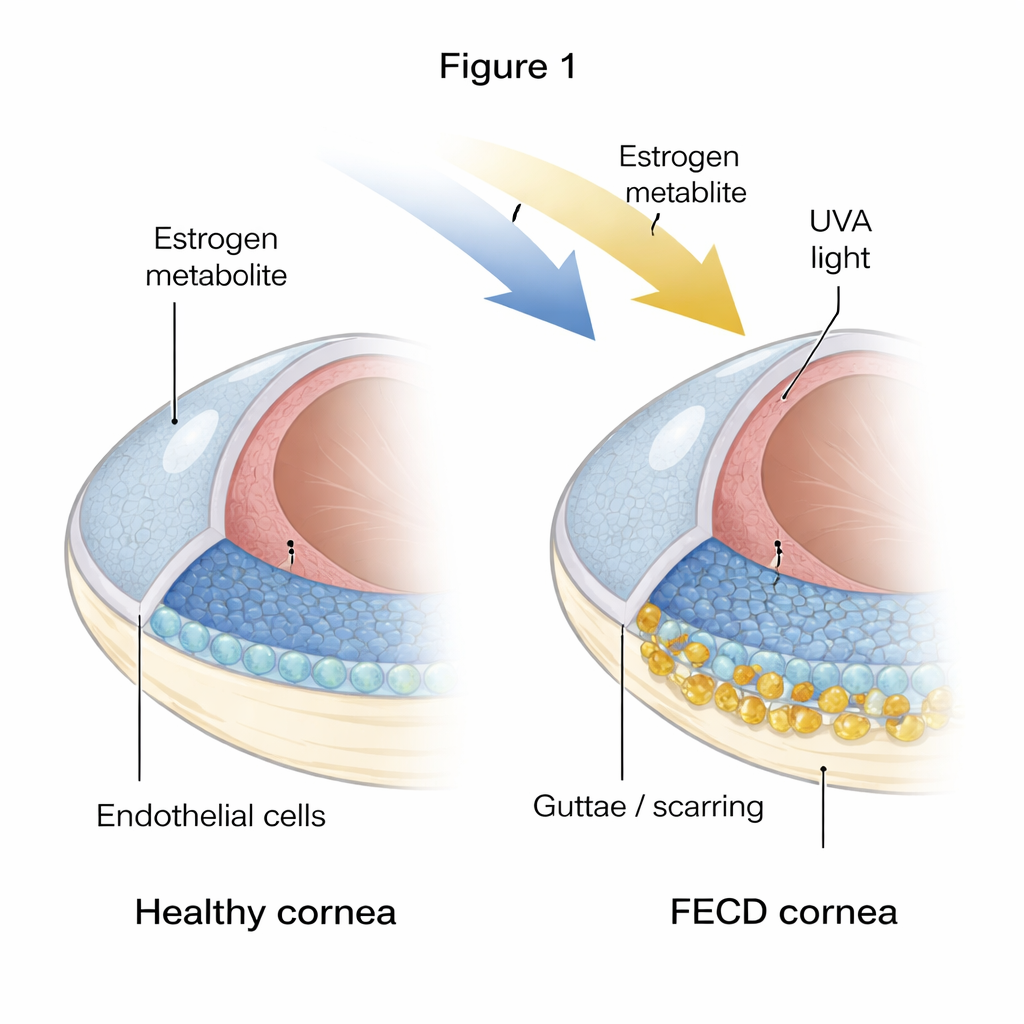
השכבה הפנימית הרגישה של הקרנית
על מנת לשמור על שקיפות הקרנית חייבת להישאר מיובשת בדיוק, עבודה שמבוצעת על ידי שכבה אחת של תאים המסתדרים במשושים הנקראים תאי האנדותל של הקרנית. ב-FECD רבים מתאים אלה מתים והשכבה הופכת לבלויה ולא אחידה. במקביל, גושים קשים וחומר מעובה, הידועים כגוטה וחומר בין-תאי עודף, מצטברים על המשטח הפנימי. המחברים השוו קרניות של תורמים בריאים לקרניות של מטופלים עם FECD ומצאו סימנים חזקים כי הרקמה החולה היא גם "מזדקנת" וגם פיברוטית: תאים הראו סמנים של זקנה תאית (מצב סגירה קבוע) וסמנים של פיברוזיס (תאים שמתנהגים יותר כמו תאי יוצרי צלקת ומשחררים רקמה נוספת).
לחץ ממושך של אור והורמונים דוחף תאים לקצה בלתי מתקן
כדי לבחון כיצד הנזק מתחיל, החוקרים ייצרו במעבדה לחץ דמוי-FECD. הם חשפו תאי אנדותל קרנית בריאים לאור אולטרה-סגול A (UVA) ול-4-הידרוקסיאסטרדיול, תוצר חמצון של אסטרוגן המקושר לנזק ל-DNA. חשיפה קצרה וחד־פעמית גרמה לתאים לעצור זמנית בשלב מאוחר במחזור התא ולהתחיל מעבר ראשוני למצב דמוי פיברובלסט, אך נותרה ביכולתם התאוששות מסוימת. בניגוד לכך, חשיפה חוזרת ומתמשכת דחפה את התאים למצב שונה: הם הצטברו בשלב מוקדם של מחזור התא הנקרא G0/G1 והפעילו את הגן p16, שמנעל את מחזור התא באמצעות חלבון השותף pRB. תאים אלו הפכו לגדולים, שטוחים ובולטים כסנזנטיים, ובמקביל הראו הבעה חזקה של סימני פיברוזיס וחלבונים המרכיבים את ה-guttae המעובים ב-FECD.
תאים סנזנטיים משדרים אותות מזיקים ומפיצים צלקות
תאים סנזנטיים אינם שוהים בשקט; הם מפרישים תערובת של מולקולות איתות הידועה כתופעת ההפרשה הקשורה להזדקנות תאית (SASP). הצוות אסף נוזל מתאים שנמצאו בלחץ והחיל אותו על תאים חדשים ועל קרניות תורמות בריאות. ה-SASP "האקוטי" יצר סימנים ראשונים לשינוי צורת התאים, בעוד ש-SASP "כרוני" דחף תאים רבים לכניסה לסנescence והגביר ביטוי גנים הקשורים לפיברוזיס ולהצטברות מטריקס נוסף. בדיקות מפורטות הראו כי ה-SASP הכרוני שופע שליחים דלקתיים כמו IL-8 ו-IL-17, הידועים בקידום הזדקנות תאית, צלקות פיברוטיות וגיוס תאי חיסון. כאשר החוקרים חסמו את מסלול ה-IL-17 או את קולטנית IL-8 (CXCR2), תאים שנחשפו ל-SASP הכרוני הראו פחות סמני סנזנס וסיבוך פיברוטי מופחת, מה שמרמז כי אותות אלה הם מנוע מרכזי של המחלה.
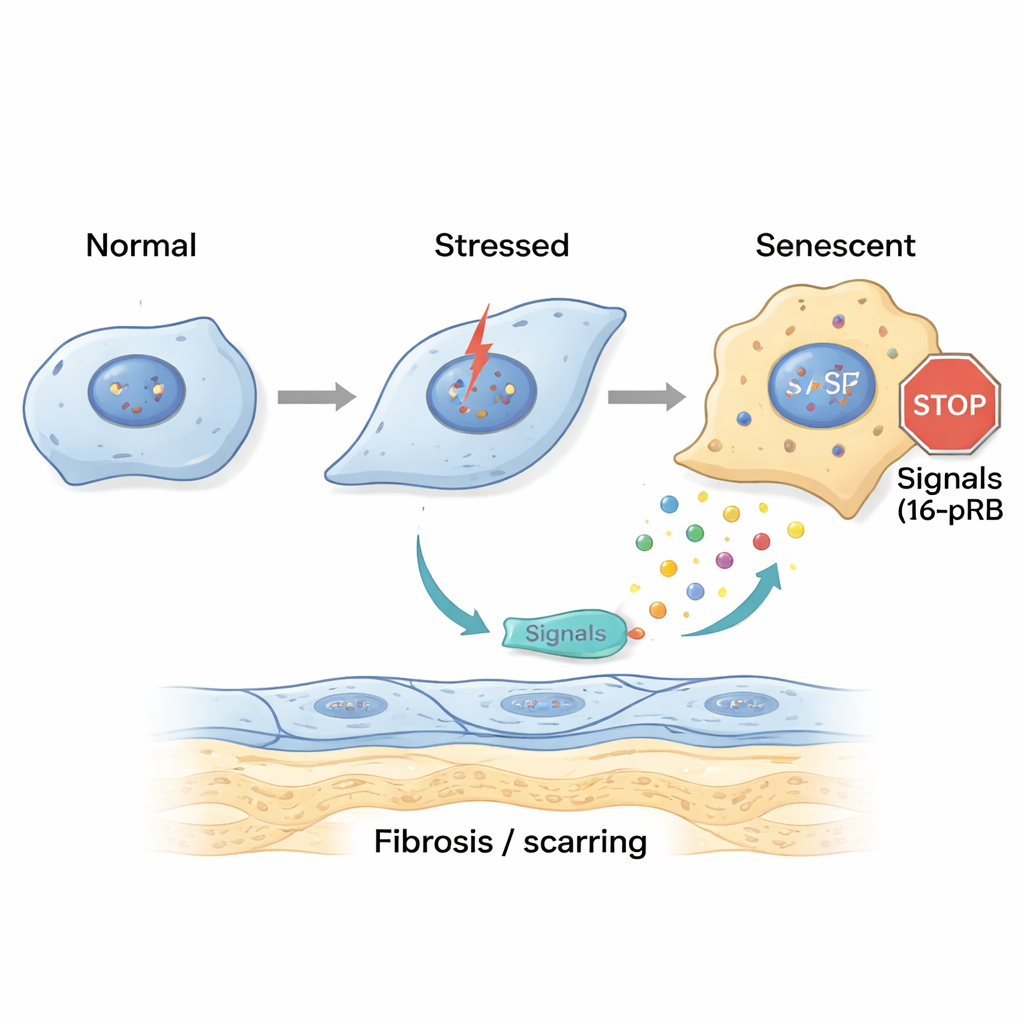
הסרת תאים שחוקים כדי להגן על הראייה
מכיוון שתאים סנזנטיים חיוביים ל-p16 היו קשורים בחוזקה להצטלקות, המחברים בחנו האם סילוקם יכול להגן על הקרנית. במודל עכבר שבו אור UVA מעורר שינויים דמויי FECD, טיפלו בבעלי החיים בתרכובת סנוליטית — דזטיניב בתוספת קווירצטין — שהורגת באופן סלקטיבי תאים סנזנטיים. בהשוואה לעכברים שלא טופלו, עכברים שטופלו בסנוליטיקה שמרו על רשת אנדותל סדירה יותר, שמרו על יותר תאים בסך הכל והראו פחות סמני סנזנס, פיברוזיס ומטריקס עודף. במילים אחרות, פינוי התאים הפגועים ביותר הקטין את עומס ההפרשות המזיקות ועזר לשמור על משטח קורניאלי בריא יותר.
מה משמעות הדבר לאנשים עם FECD
לוּמטופלים, FECD כיום לעתים קרובות מובילה להשתלת קרנית כאשר הראייה נהיית מטושטשת מדי. המחקר מציע מסלול שונה: ייתכן שהמחלה מונעת על ידי הצטברות איטית של תאים לחוצים שאינם מתחלקים — שתפקידם לקוי והם גם מזרזים הרעלה של שכנים באמצעות אותות דלקתיים ופיברוטיים. מיקוד אותות אלה באמצעות תרופות נגד מסלולי IL-17 או IL-8, או שימוש בטיפולים סנוליטיים להסרת התאים הפגועים ביותר, עשוי יום אחד לעכב את ההצטלקות, לשמר יותר מרקמת העין הטבעית ולהשהות או להפחית את הצורך בניתוח.
ציטוט: Parekh, M., Adhikari, Y., Deshpande, N. et al. p16-mediated G0/G1 cell cycle arrest leads to SASP and fibrosis in Fuchs endothelial corneal dystrophy. Cell Death Dis 17, 197 (2026). https://doi.org/10.1038/s41419-026-08425-6
מילות מפתח: דיסטורפיית פוכר, אפיתל האנדותל של הקרנית, הזדקנות תאית, פיברוזיס, טיפול סנוליטי