Clear Sky Science · he
DNA מיטוכונדריאלי מפעיל את ציר NLRP3-IL-1β במיקרוגליה באמצעות קשירה ל-NLRP3, ומוביל לנוירודגנרציה במודלים של מחלת פרקינסון
מדוע זה חשוב למחלת פרקינסון
מחלת פרקינסון ידועה בעיקר ברעד ובהאטת התנועה, אך מתחת לתסמינים אלה מתנהלת מלחמה פנימית מורכבת במוח. מחקר זה חושף כיצד חתיכות קטנות של חומר גנטי המגיעותמיטוכונדריות פגועות בתאי החיסון של המוח יכולות להצית דלקת שמאיטה מאוחר יותר הורגת את נוירוני הדופמין הנדרשים לתנועה חלקה. הבנת שרשרת תגובות זו פותחת יעדים תרופתיים חדשים ומדויקים שעשויים להאט או למנוע נזק בדומה לפרקינסון.
תאי חיסון מוחיים וכוחיות תחת לחץ
המוח מכיל לא רק תאי עצב אלא גם מיקרוגליה, תאי החיסון המקומיים שלו. במחלת פרקינסון מיקרוגליה לעיתים נעשות יתר פעילות, ומשחררות מולקולות רעילות ואותות דלקתיים הפוגעים בעצבונים הסמוכים. המחברים התרכזו במיטוכונדריה, "תחנות הכוח" של התאים, הנושאות DNA משלהן. כאשר מיטוכונדריה נפגעת — על ידי רעלנים, הזדקנות או לחצים אחרים — ה-DNA שלה עלול לעבור חמצון, סוג של נזק כימי הנגרם על ידי רדיקלים חופשיים. מאחר ש-DNA מיטוכונדריאלי דומה ל-DNA חיידקי, שרידים פגועים אלה יכולים לפעול כאותות אזעקה בתוך המוח, לעורר את מערכת החיסון ועלולים להניע דלקת כרונית.
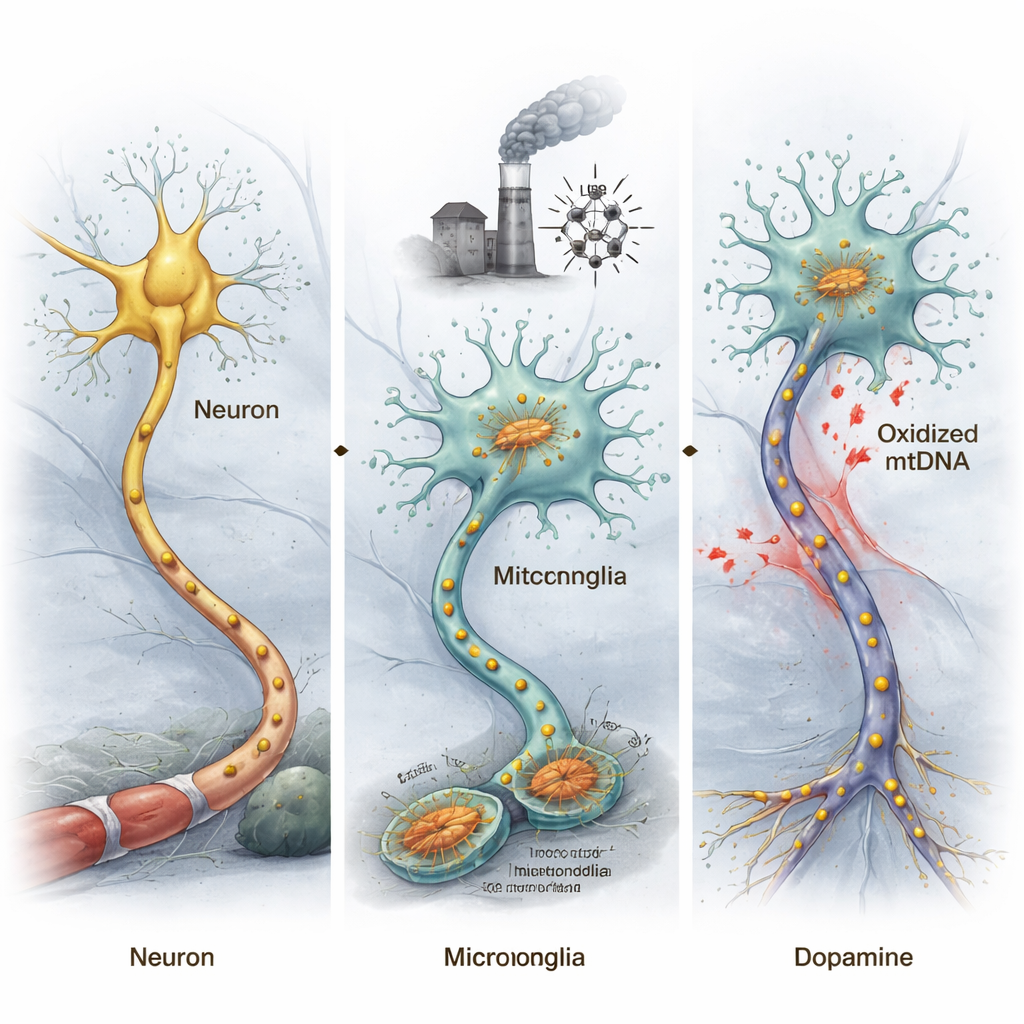
DNA מיטוכונדריאלי פגוע יכול להטות עכברים למחלה בדומה לפרקינסון
כדי לבדוק האם DNA מיטוכונדריאלי מחומצן (ox-mtDNA) יכול להיות בעצם הגורם לשינויים בדומה לפרקינסון, החוקריים חילצו ox-mtDNA מתאים מיקרוגליה בלחץ והזריקו אותו ישירות לאזור מוחי שמכיל בדרך כלל נוירונים המייצרים דופמין החשובים לתנועה. עכברים שנחשפו ל-ox-mtDNA הראו ירידה בתנועה במבחני התנהגות ואובדן של נוירוני דופמין אלה, משקף תכונות מרכזיות של מחלת פרקינסון. על ידי מיון תאים (נוירונים ומיקרוגליה) מהמידבריין וניתוח ביטוי הגנים שלהם, מצאו החוקרים שגנים המקושרים לפרקינסון הפכו לבלתי תקינים יותר בנוירונים, בעוד שגנים הקשורים לדלקת הופעלו בחוזקה במיקרוגליה.
מתג אזעקה מולקולרי בתוך המיקרוגליה
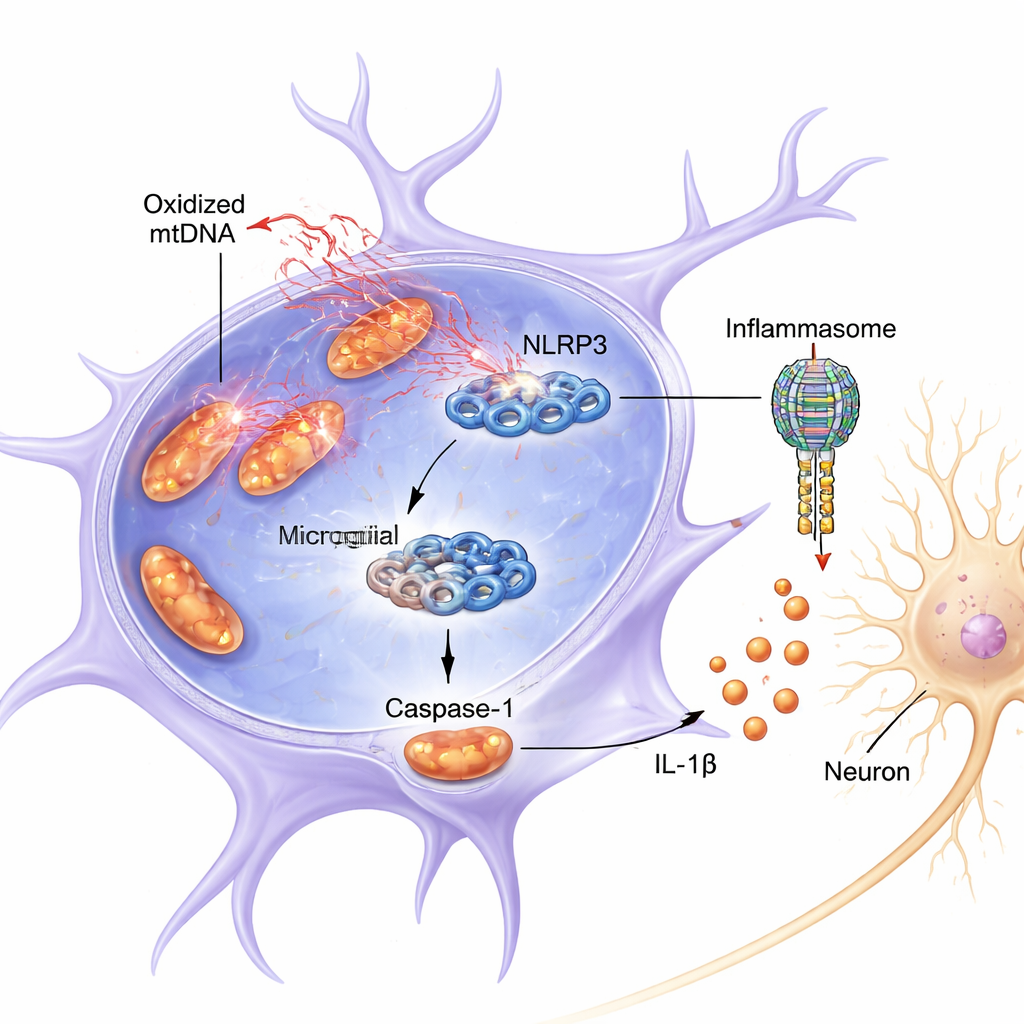
המחקר התמקד במורכבות חלבונית במיקרוגליה הנקראת NLRP3, חלק מרכבה גדולה יותר הידועה כאינפלמזום. כשהיא מופעלת, NLRP3 מסייעת להפעיל את קספאז-1, אנזים החותך את המולקולה הדלקתית IL-1β לצורתה הפעילה והנזיקית. הן בעכברים והן בתאים במאגר, שילוב של אות תצעול דלקתי (LPS, רכיב חיידקי) והרעל הדמוי חומרי הדברה רוטנון גרם למיטוכונדריה במיקרוגליה לשחרר DNA מיטוכונדריאלי מחומצן לנוזל התאי. שחרור זה לווה בהפעלה מוגברת של NLRP3, יותר קספאז-1 חתוך (פעיל) ורמות גבוהות יותר של IL-1β. מדיה שנלקחה מהמיקרוגליה המופרזת הזו הייתה רעילה ישירות לנוירונים דמויי דופמין שגודלו במנה, הפחיתה את הישרדותם ואת רמת הסמן המרכזי שלהם, טירוזין הידרוקסילאז.
קשירה ישירה: כיצד DNA מחומצן מדליק את מתג ה-NLRP3
מעבר לקורלציה פשוטה, הראו המחברים כי ox-mtDNA לא רק נוכח בזמן הדלקת — הוא נראה קשור פיזית ל-NLRP3 ומפעיל אותו. כשחסמו את שחרור ה-DNA המיטוכונדריאלי בעזרת תרופה, יורדו ההפעלות של קספאז-1 ו-IL-1β. להפך, העברה ישירה של DNA מיטוכונדריאלי מחומצן לתוך מיקרוגליה חיזקה באופן משמעותי את איתות NLRP3, יותר מאשר mtDNA לא מחומצן. באמצעות ניסויי משיכה ביוכימיים זוהו mtDNA, עשיר בסימני נזק חמצוני, קשור ל-NLRP3. מודלים ממוחשבים וכימיה חלבונית הראו כי ox-mtDNA נקשר למקטע חיובי וגמיש של NLRP3 ("אזור בלתי מסודר פנימית" המתפרש על חומצות אמינו 180–187). כאשר מקטע קריטי זה הוסר מ-NLRP3, יכולתו לקשור ox-mtDNA ולהפעיל קספאז-1 פחתה משמעותית.
כיבוי האינפלמזום שומר על הנוירונים
לאחר מכן שאלו החוקרים האם התערבות ב-NLRP3 יכולה להגן על נוירונים. במיקרוגליה בתרבית, הפחתה גנטית של NLRP3 הורידה באופן חד את הפעלת קספאז-1 ו-IL-1β לאחר טיפול ב-LPS ורוטנון, והמדיה המתונה מתאים אלה הייתה הרעילה פחות בהרבה לנוירונים דמויי דופמין. בעכברים, מעכב NLRP3 סלקטיבי (MCC950) הפחית את ההפעלה המיקרוגליאלית, שמר על נוירוני דופמין והוריד את החלבונים הקשורים לאינפלמזום במודלים שהונעו או על ידי LPS פלוס רוטנון או על ידי הזרקת mtDNA. יחד, ניסויים אלה מראים כי שרשרת ox-mtDNA–NLRP3–IL-1β אינה רק קשורה לנזק; היא דרושה לחלק גדול מאובדן הנוירונים שנצפה.
מה משמעות הדבר לטיפולים עתידיים בפרקינסון
ללא-מומחים, המסר המרכזי הוא ש-DNA מיטוכונדריאלי פגום הנוזל מתוך תאי החיסון של המוח יכול להיצמד ישירות ל"מתג אזעקה" פנימי (NLRP3), ולגרום גל דלקתי הפוגע בנוירוני דופמין ומניע מחלה בדומה לפרקינסון במודלים. מכיוון שאינטראקציה זו תלויה במקטע קצר ומוגדר של חלבון NLRP3 ובטבע המחומצן של ה-DNA המיטוכונדריאלי, היא מציעה יעדים תרופתיים מדויקים. תרפיות שמונעות נזק או דליפה של DNA מיטוכונדריאלי, חוסמות את קשירתו ל-NLRP3, או מעכבות את NLRP3 עצמו עשויות, מבחינה עקרונית, לקרר את קסקדת הדלקת הזאת ולעכב את התקדמות מחלת הפרקינסון.
ציטוט: Gan, Q., Fu, X., Zhou, T. et al. Mitochondrial DNA drives NLRP3-IL-1β axis activation in microglia by binding to NLRP3, leading to neurodegeneration in Parkinson’s disease models. Cell Death Dis 17, 213 (2026). https://doi.org/10.1038/s41419-026-08424-7
מילות מפתח: מחלת פרקינסון, מיקרוגליה, DNA מיטוכונדריאלי, אינפלמזום NLRP3, דלקת עצבית