Clear Sky Science · he
מיקוד ב-GNG4 מונע התקדמות גידול ומשיב רגישות לאנזלוטומיד בסרטן הערמונית על ידי דיכוי אוטופאגיה
מדוע המחקר הזה חשוב
לגברים רבים עם סרטן ערמונית מתקדם, תרופות חוסמות הורמונים חזקות כמו אנזלוטומיד עובדות היטב בתחילה אך לאחר מכן מאבדות אפקטיביות בהדרגה. המחקר הזה חושף תרגיל הישרדות סמוי שהתאים סרטניים משתמשים בו ומצביע על חלבון ספציפי, שנקרא GNG4, שעוזר לסרטן להמשיך לגדול ולהתנגד לטיפול. הבנת המנגנון הזה עשויה להוביל לשילובי טיפולים שיגרמו לתרופות הנוכחיות לעבוד טוב יותר ולמשך זמן ארוך יותר.
מתג חלבוני שמוסתר לעין
תאי סרטן הערמונית מונעים במידה רבה על ידי הורמונים גבריים, ולכן הטיפול הסטנדרטי במחלה מתקדמת חוסם את אותות אלה. עם זאת, רוב הגידולים בסופו של דבר הופכים ל"עמידים לאחר כריתת זקיקי המין" (castration resistant) ומתחילים לגדול שוב. המחברים חיפשו גנים שהיו פעילים הרבה יותר ברקמת הגידול לעומת הרקמה הערמונית הנורמלית הסמוכה מאותו מטופל. בין כמה מועמדים, GNG4 בלט: כאשר הורידו את רמותיו בתאי סרטן הערמונית, גדילת התאים ירדה באופן חד. ניתוחים של מאות דגימות מטופלים איששו כי GNG4 גבוה יותר בגידולים ראשוניים של הערמונית מאשר ברקמה נורמלית, ובמיוחד מוגבר בגידולים אגרסיביים יותר ובדרגה גבוהה יותר.
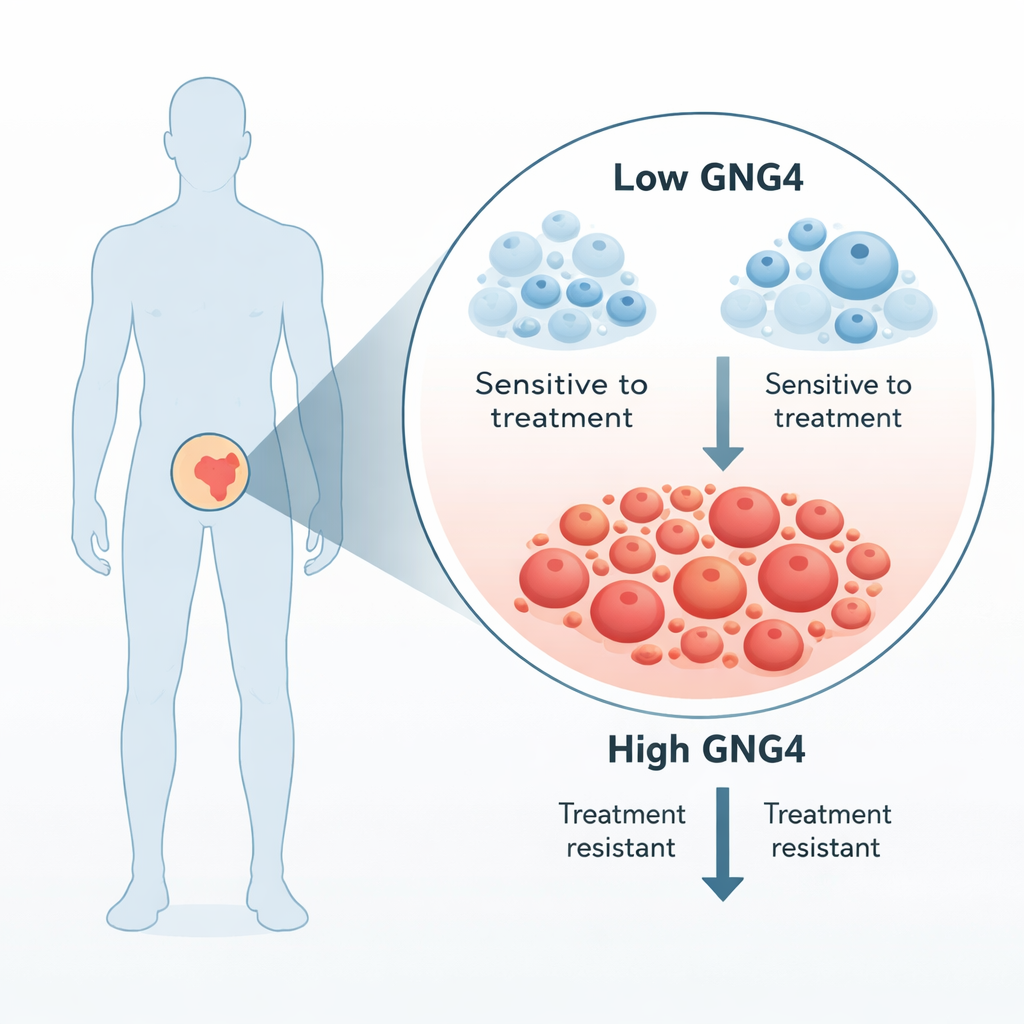
כיצד GNG4 מסייע לגידולים לשגשג
GNG4 הוא חלק ממשפחה גדולה של אותות הידועה כחלבוני G, שנמצאים בממברנת התאים ומעבירים אותות מהסביבה החיצונית אל חלל התא. הצוות הראה כי השתקת GNG4 בקו תאי סרטן הערמונית האטה את חלוקת התאים, דחפה תאים לעצירה בשלב ביקורת במחזור התא והגברה של מוות תאי מתוכנן. שינויים אלה גם צמצמו את יכולת התאים הסרטניים לנוע ולסגור פצעים במבחנות, וגידולים שנוצרו מתאים חסרי GNG4 גדלו באיטיות יחסית בעכברים. יחד, הממצאים הללו מרמזים ש-GNG4 פועל כמדמה גז לצמיחה ולהתפשטות סרטן הערמונית.
אוטופאגיה: המחסן החירום של התא הסרטני
החוקרים התמקדו לאחר מכן בתהליך שנקרא אוטופאגיה, שבו תאים מפרקים וממוחזרים רכיבים פנימיים כדי לשרוד לחץ, כגון רעב או טיפול תרופתי. בהרבה סרטן מתקדם, האוטופאגיה משמשת כמחסן חירום שעוזר לתאי הגידול להתמודד עם תנאים קשים. במחקר זה, תאי סרטן ערמונית עם פעילות גבוהה של GNG4 הראו יותר סימנים של אוטופאגיה פעילה, בעוד שתאים שבהם הושתק GNG4 הציגו פחות מבנים ממחזרים ורמות נמוכות יותר של סמני אוטופאגיה מרכזיים. כאשר GNG4 הועבר בהגברה, התאים עמדו טוב יותר בפני אנזלוטומיד וחוו פחות מוות תאי. חסימת האוטופאגיה באמצעות מעכב כימי מחקה במידה רבה את ההגנה הזו, מה שמרמז ש-GNG4 מסייע לגידולים לעמוד בטיפול בעיקר על ידי הגברת מערכת המיחזור הזו.
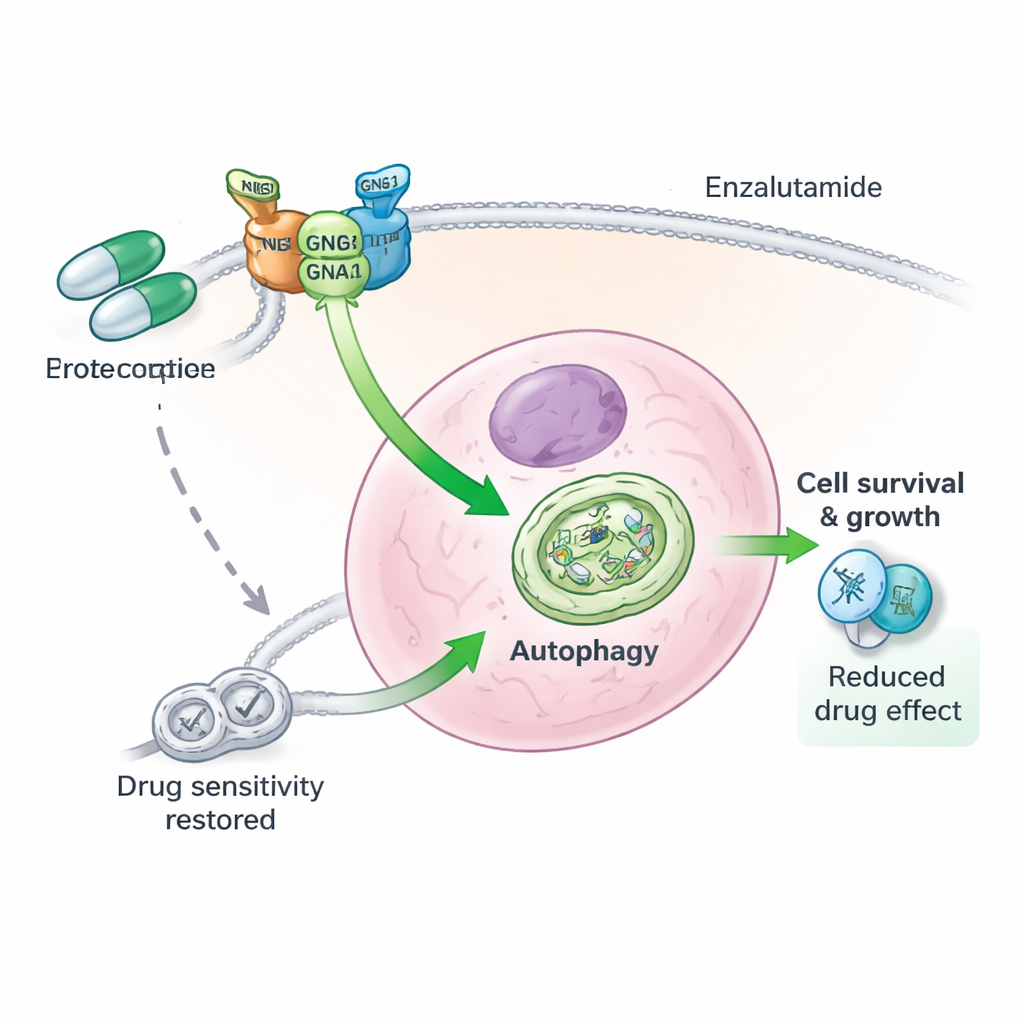
צמד חלבונים תלת-חלקי מאחורי עמידות לתרופות
בהעמקה נוספת, המחברים גילו כי GNG4 אינו פועל לבדו. הוא יוצר אינטראקציה פיזית עם רכיב אחר של חלבוני G, GNB1, כדי לייצב חלבון שלישי, GNAI3. ביחד, שלוש תת-היחידות הללו יוצרות קומפלקס פונקציונלי שמחזק אוטופאגיה בתוך תאי סרטן הערמונית. כאשר GNG4 הושתק, חלבון GNAI3 סומן במהירות רבה יותר להרס והפורק על ידי מנגנון ההשלכת של התא, מה שהשבית את איתות האוטופאגיה. הסרת GNAI3 עצמה ביטלה את יתרונות הגדילה וההישרדות שניתנו על ידי עודף GNG4, הן בתאים ממוקדמים והן בגידולים בעכברים. במילים אחרות, GNG4 מדחף מלינות והתנגדות ללחץ ברובו דרך ציר GNG4–GNB1–GNAI3 הזה.
להגביר את יעילות התרופות הקיימות
לבסוף, הצוות בדק מה קורה כאשר ממקדים ב-GNG4 בשילוב עם אנזלוטומיד, תרופה מובילה לסרטן הערמונית המתקדם. במעבדה, השתקת GNG4 הפכה תאים סרטניים לרגישים יותר באופן ניכר לאנזלוטומיד וצמצמה את יכולתם ליצור מושבות לאחר הטיפול. בעכברים, גידולים עם רמות GNG4 מופחתות התקטנו יותר בעת קבלת אנזלוטומיד מאשר גידולים עם רמות GNG4 רגילות, ללא רעילות נוספת בולטת. חסימת האוטופאגיה ישירות הביאה לשיפורים דומים. תוצאות אלו מרמזות כי הפרעה לאוטופאגיה המונעת על ידי GNG4 יכולה לשלול מתאי הגידול מנגנון התמודדות קריטי, ולאפשר לטיפולים החוסמי-הורמונים הקיימים להנחית מכה חזקה ועמידה יותר.
מה משמעות הדבר עבור מטופלים
ללא-מומחה, המסר המרכזי הוא כי חלק מסרטני הערמונית שורדים טיפול על ידי הדלקת מערכת מיחזור פנימית שפועלת כמו גנרטור גיבוי. מחקר זה מזהה את GNG4 כמתג הראשי שמדליק את המערכת הזו, הפועל יחד עם חלבונים שותפים כדי להגן על תאי הסרטן מפני אנזלוטומיד. על ידי כיבוי המתג הזה — בין אם על ידי מיקוד ישיר ב-GNG4 ובין אם על ידי דיכוי מבוקר של האוטופאגיה — טיפולים עתידיים עשויים להאט את גדילת הגידול ולהחזיר את הרגישות לתרופות בגברים שסרטןם הפך קשה לטיפול.
ציטוט: Chen, L., Zhang, J., Hu, Y. et al. Targeting GNG4 inhibits tumor progression and restores enzalutamide sensitivity in prostate cancer by suppressing autophagy. Cell Death Dis 17, 160 (2026). https://doi.org/10.1038/s41419-026-08421-w
מילות מפתח: סרטן הערמונית, התנגדות לתרופות, אוטופאגיה, חלבוני G, אנזלוטומיד