Clear Sky Science · he
DNA-PKcs מארגן ישנות תאית שנגרמת מהדילול של CTLA-4 בתאי סרטן
להפוך את מתג הצמיחה של הסרטן לאות עצור
תרופות מבוססות חיסון נגד סרטן מתמקדות לעיתים קרובות במולקולה בשם CTLA-4, הנמצאת על תאי המערכת החיסונית, כדי לסייע לגוף לתקוף גידולים. המחקר הזה חושף תפנית מפתיעה: CTLA-4 נמצא גם בתוך תאי הסרטן עצמם ועלול לפעול כמסייע צמיחה סמוי. כאשר החוקרים הסירו מכוון את ה-CTLA-4 הפנימי מתאי מלנומה, תאי הסרטן הפסיקו להתחלק ונכנסו למצב «פרישה» ארוכת טווח המכונה ישנות תאית. הבנת התפקיד הבלתי צפוי הזה פותחת דרכים חדשות להאט או אפילו להקטין גידולים על ידי מטרה של CTLA-4 בתוך תאי הסרטן — לא רק על תאי החיסון.
כשתאים בוחרים פרישה על פני גדילה פראית
תאים בדרך כלל מתחלקים, מתקנים נזקים—and כאשר הנזק חורג מהיכולת לתקן — או שמתים או נכנסים לישנות, השהייה קבועה בצמיחה. תאים ישנים בדרך כלל מתנפחים, משנים צורה ומפיקים סימנים ייחודיים שניתן לזהות במעבדה. החוקרים מצאו כי כאשר הם הפחיתו את ה-CTLA-4 בתוך תאי מלנומה של עכבר ואדם, התאים גדלו יותר בגודל, קצב הגדילה שלהם ירד באופן חזק ואיתותי ישנות קלאסיים עלו — כולל אנזימים הניתנים לזיהוי בצביעות מיוחדות וחלבונים כמו p16 ו-p21 החוסמים את מחזור התא. השינויים היו נראים הן בהשתקה זמנית של CTLA-4 והן בהדחה קבועה שלו באמצעות כלים לעריכת גנים.
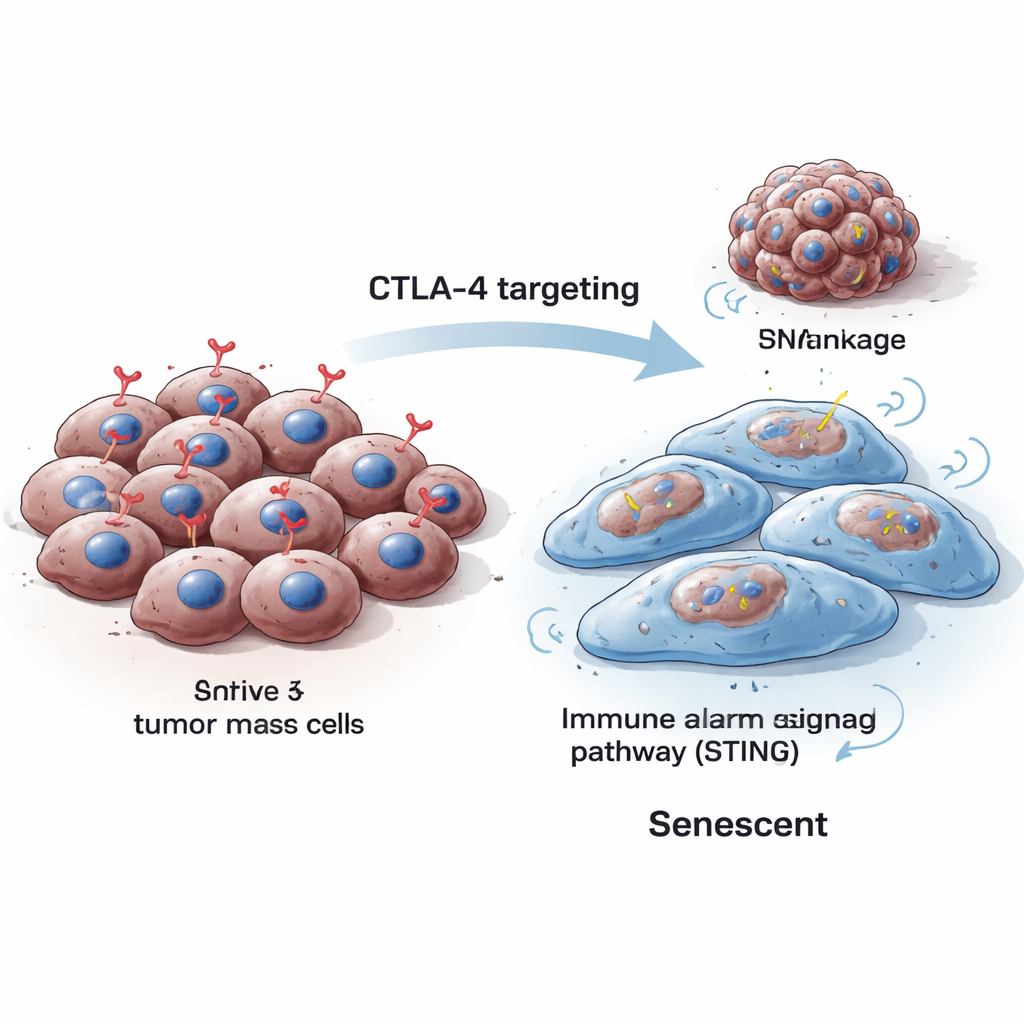
סדקים בתוכנית הגנטית מובילים לעצירה
כדי להבין מדוע אובדן CTLA-4 דוחף תאי סרטן לישנות, הצוות בחן כיצד תאים אלה מטפלים בדנ"א במהלך חלוקה. הם גילו כי דילול CTLA-4 הפחית רמות של Aurora B, חלבון המסייע להפרדה נקייה של כרומוזומים בעת חלוקה. כאשר Aurora B ירד, התפתחה חוסר יציבות גנומית: הופיעו גופים מיקרונוקליים קטנים המכילים דנ"א, וסימני נזק לדנ"א עלו. סוג זה של מתח בדנ"א ידוע כמדחף תאים לעבר ישנות במקום צמיחה בלתי מבוקרת. באופן חשוב, שחזור רמות Aurora B עזר להפחית את המיקרונוקליים, וקישר ישירות את אובדן ה-CTLA-4 לטיפול לקוי בכרומוזומים ונזק לדנ"א.
נזק לדנ"א מדליק רשת אזעקה פנימית
הדנ"א השבור והמוקצה במקומות לא נכונים בתאים דלים ב-CTLA-4 לא נשאר ללא תשומת לב. הוא הפעיל את DNA-PKcs, חיישן נזק לדנ"א, שהשפיע בתורו על מסלול STING — מערכת אזעקה פנימית שמגיבה לדנ"א זר בתוך התאים. לאחר שה-STING הופעל, הוא אותת מולקולות מטה בזרם, כולל TBK1 ו-IRF3, וגם הגביר נתיב מרכזי נוסף שבקרת צמיחה — את מסלול AKT. במקום לקדם צמיחה, שילוב האיתותים הזה בסופו של דבר העלה את p21, מעצור חזק של מחזור התא, ומחזק את מצב הישות. כאשר החוקרים חסמו את DNA-PKcs, הפעלת STING ותכונות הישנות ירדו במידה רבה, מה שמראה כי DNA-PKcs תופס מקום מרכזי במערכת האזעקה הזו.
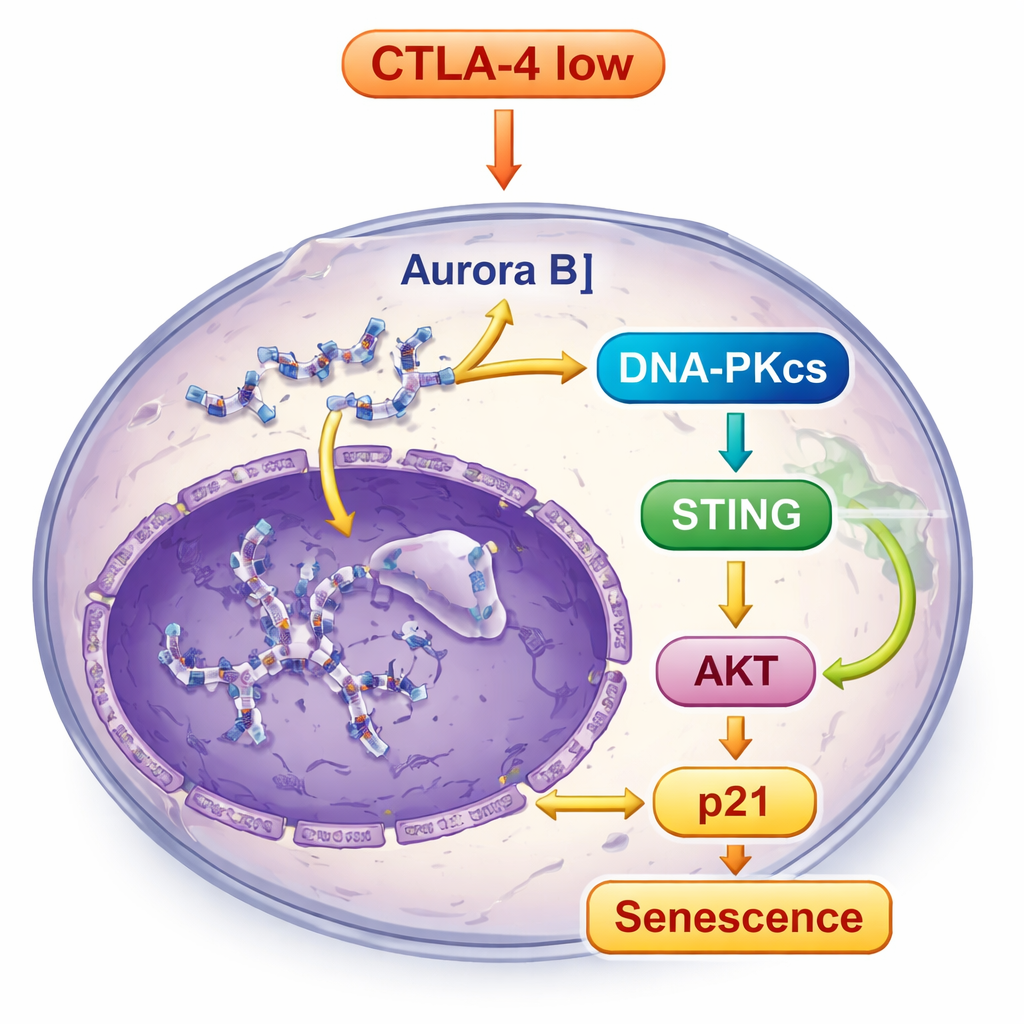
מן תרבית תאים אל גידולים בחיות חיות
צלחות מעבדה אומרות רק חלק מהסיפור, לכן החוקרים בדקו האם אובדן CTLA-4 ישפיע על גידולים אמיתיים בעכברים. הם השתילו תאי מלנומה עם או בלי CTLA-4 בצדי בעלי החיים. גידולים חסרי CTLA-4 גדלו לאט יותר, שקלו פחות והיו קטנים יותר בנפח ביחס לאלו שהכילו CTLA-4. גידולים חסרי CTLA-4 גם הראו צביעת ישנות חזקה יותר ורמות גבוהות יותר של נזק לדנ"א והפעלה של מסלול STING. ניתוח נתוני חולי סרטן ממאגרי מידע ציבוריים רחבים תמך בקשר: במספר סוגי סרטן, ביטוי CTLA-4 נטה להיות ביחס הפוך ל-DNA-PKcs ולרכיבי תיקון דנ"א אחרים, מה שהדהד את הממצאים במעבדה במחלות אנושיות.
מה משמעות זה לטיפולי סרטן עתידיים
בסך הכל, המחקר מראה כי CTLA-4 בתוך תאי סרטן מסייע להם לשמור על יציבות גנטית ולהמשיך להתחלק. כאשר CTLA-4 מוסר, הכרומוזומים נעשים לא יציבים, שברי דנ"א מצטברים, ומסלול אזעקה פנימי — שמרכזו DNA-PKcs ו-STING — דוחף את התאים לעצירה צמיחה קבועה. עבור הקורא הכללי, משמעות הדבר היא שכיבוי CTLA-4 בתאי הגידול מניע את הסרטן הרחק מהתנהגות מהירה ומסוכנת של גדילה ולעבר מצב "פרישה" בטוח יותר. התובנות האלו מציעות שטיפולי סרטן עתידיים יכולים להיות מעוצבים לא רק על מנת לשחרר את המערכת החיסונית באמצעות חסימת CTLA-4 על תאי החיסון, אלא גם לפגוע ישירות בגידולים על ידי מטרה של CTLA-4 בתוך תאי הסרטן וניצול הישנות כבלם פנימי לצמיחת הסרטן.
ציטוט: Lee, JJ., Rhee, W.J., Kim, S.Y. et al. DNA-PKcs orchestrates CTLA-4 depletion-induced senescence in cancer cells. Cell Death Dis 17, 204 (2026). https://doi.org/10.1038/s41419-026-08419-4
מילות מפתח: ישנות תאית, מלנומה, CTLA-4, נזק לדנ"א, מסלול STING