Clear Sky Science · he
תחזוקה חריגה של גורם השעתוק ההתפתחותי PAX6 מקדמת מוות של תאים עצביים באמצעות איתות JNK3
מדוע המחקר הזה חשוב לראייה
גלאוקומה היא אחת הסיבות המובילות לעיוורון קבוע, בעיקר מכיוון שתאי העצב המעבירים מידע חזותי מהעין למוח מתים בהדרגה. טיפולים רבים מורידים את הלחץ התוך-עיני, אך אנשים עדיין עלולים לאבד את הראייה גם כשהלחץ נשלט היטב. המחקר הזה שואל שאלה עמוקה יותר: מה גורם לתאי העצב של הרשתית לקבל החלטה למות כאשר הם תחת מתח, והאם ניתן לכבות את ההחלטה הזו ברמה של שליטת הגנים בתוך גרעין התא?
רשתית בלחץ תחת התקפה
בלב הגלאוקומה ומחלות עין קשורות עומד אובדן איטי של תאי הגנגליון של הרשתית (RGCs), נוירונים היוצאים של העין. תאים אלה פגיעים לצורות רבות של מתח, כולל רמות רעילות של הנוירוטרנסמיטר גלוטמט, שמפעיל ביתר את קולטני NMDA וגורם לחדירת סידן מזיקה. החוקרים השתמשו במודל עכבר מבוסס היטב שבו מוזרקת כמות קטנה של NMDA לעין, פוגעת באופן סלקטיבי ב-RGCs ומשאירה את שכבות הרשתית האחרות ברובן שלמות. הם אימתו שהטיפול הזה לא שינה את הלחץ התוך-עיני, אך גרם לסימנים אופייניים של מוות מתוכנת בתאי RGC, כמו שחרור ציטוכרום c מהמיטוכונדריה והופעת גרעינים חיוביים ב-TUNEL.
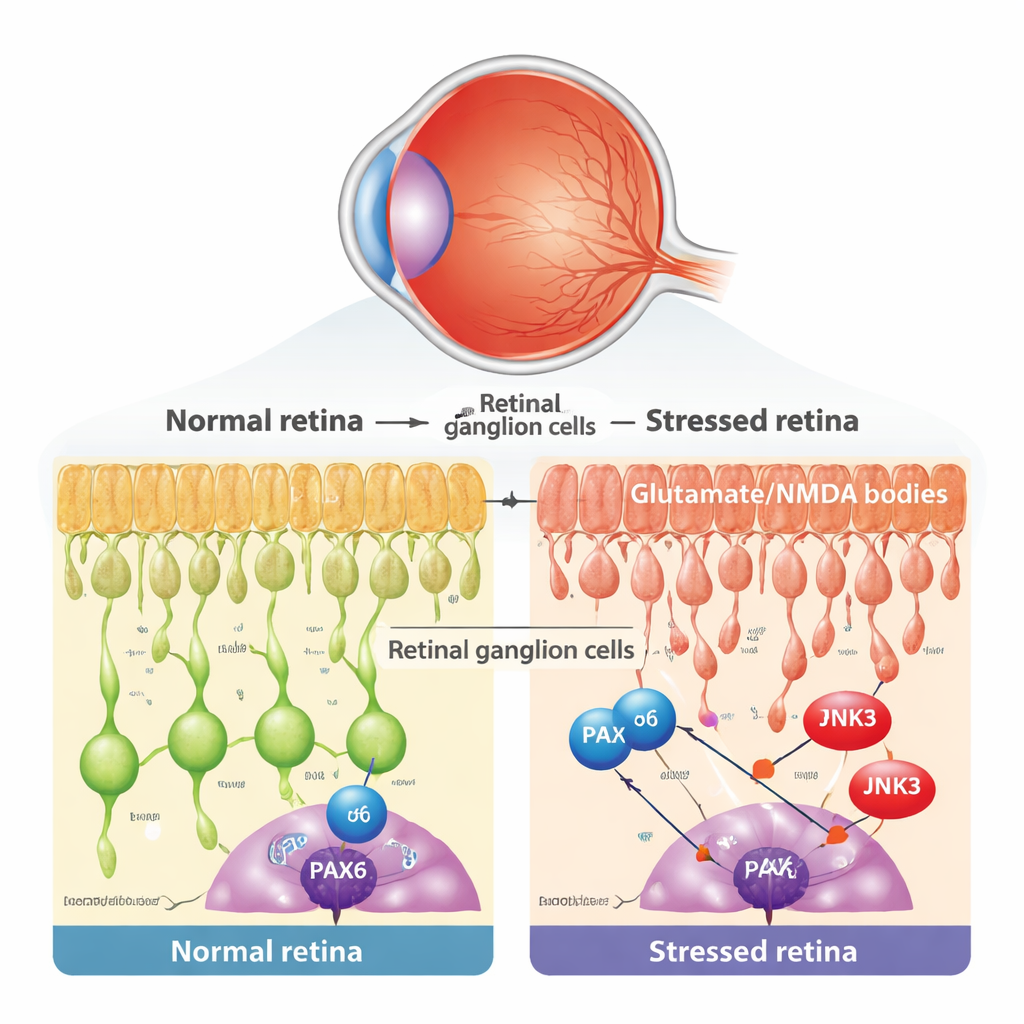
גן התפתחותי שסירב לפרוש
במהלך ההתפתחות המוקדמת, רגולטור גנים בשם PAX6 פועל כאדריכל ראשי של העין, ומנחה כיצד תאים רשתיתיים שונים נוצרים ומתארגנים. ההנחה המקובלת היא שתוכניות התפתחותיות כאלה נסגרות ברובן בבגרות. על ידי ניתוח חוזר של נתוני רצף-RNA חד-תאיים מרשתיות של עכבר ואדם, הצוות מצא כי PAX6 נשמר באופן חזק ובחירה בסוגי RGC בוגרים ובאינטרנוירונים מסוימים. באמצעות צביעות מיקרוסקופיות הם הראו שבשכבה שבה שוכנים ה-RGCs, PAX6 נמצא בעיקר בתאי הגנגליון ולא בתאי האמאקרים השכנים. ממצא זה העלה אפשרות מרתקת: בתחלואה בוגרת עשויה תוכנית התפתחות ישנה להיות מושאלת ולהיות נהפכת למניעת הירידה העצבית.
מאמפאיה למוציא להורג: PAX6 משנה תפקיד
כדי לבחון האם PAX6 מסייע ל-RGCs לשרוד או למות תחת לחץ, המדענים השתמשו בגישה הדומה לגנותרפיה. הם מסרו וקטור ויראלי הנושא RNA קטן שממקד ומדכא ספציפית את PAX6 ברשתית, ואז חשפו את העיניים ל-NMDA. בהשוואה לעיניים בטיפול ביקורת, רשתיות שבהן PAX6 דוכא הראו הרבה פחות RGCs אפופטוטיים ופחות נזק מיטוכונדריאלי, מה שמצביע על כך ש-PAX6 נדרש למוות תאי מלא במודל זה. רצף-RNA ברמת הגנום הראה כי גנים רבים המעודדים מוות, במיוחד אלה המעורבים בנזק מיטוכונדריאלי והפעלה של קאספאזות, הועלו חזק על ידי NMDA בעכברים רגילים אך נחלשו כאשר PAX6 הושתק. במילים אחרות, PAX6 מסייע להפעיל רשת גנים שמדחפת את ה-RGCs מעבר לקו.
קינאזת המתח שמחליפה את המתג של PAX6
איך מתח מפעיל את PAX6 בלי להגדיל את כמותו? הצוות התמקד ב-JNK3, אנזים רגיש מתח שנמצא בעיקר בנוירונים. תחת פגיעת NMDA, JNK3 היגר לגרעין ה-RGCs וקושר באופן פיזי את PAX6. ניסויים ביוכימיים במבחנה עם חלבונים מטוהרים הראו ש-JNK3 יכול להוסיף תגי פוספט ל-PAX6 ישירות, ותהליך זה נחסם על ידי מעכב JNK. בעכברים חסרי הגן Jnk3, NMDA כבר לא יצר את דפוס פוספורילציה של PAX6. מיפוי כרומטין (ChIP-seq) ובדיקות קשירה ממוקדות הראו שבתנאי מתח, PAX6 מפוספורל יחד עם JNK3 קשור בעוצמה מוגברת לאזורי בקרה של גנים פרו-אפופטוטיים מרכזיים כמו Bax ו-Gadd45a, ומגביר את פעילותם. כאשר או PAX6 הושתק או JNK3 הוסר גנטית, קשירה זו והפעלת הגנים הפרו-תאיים המקבילה ירדו באופן חד.
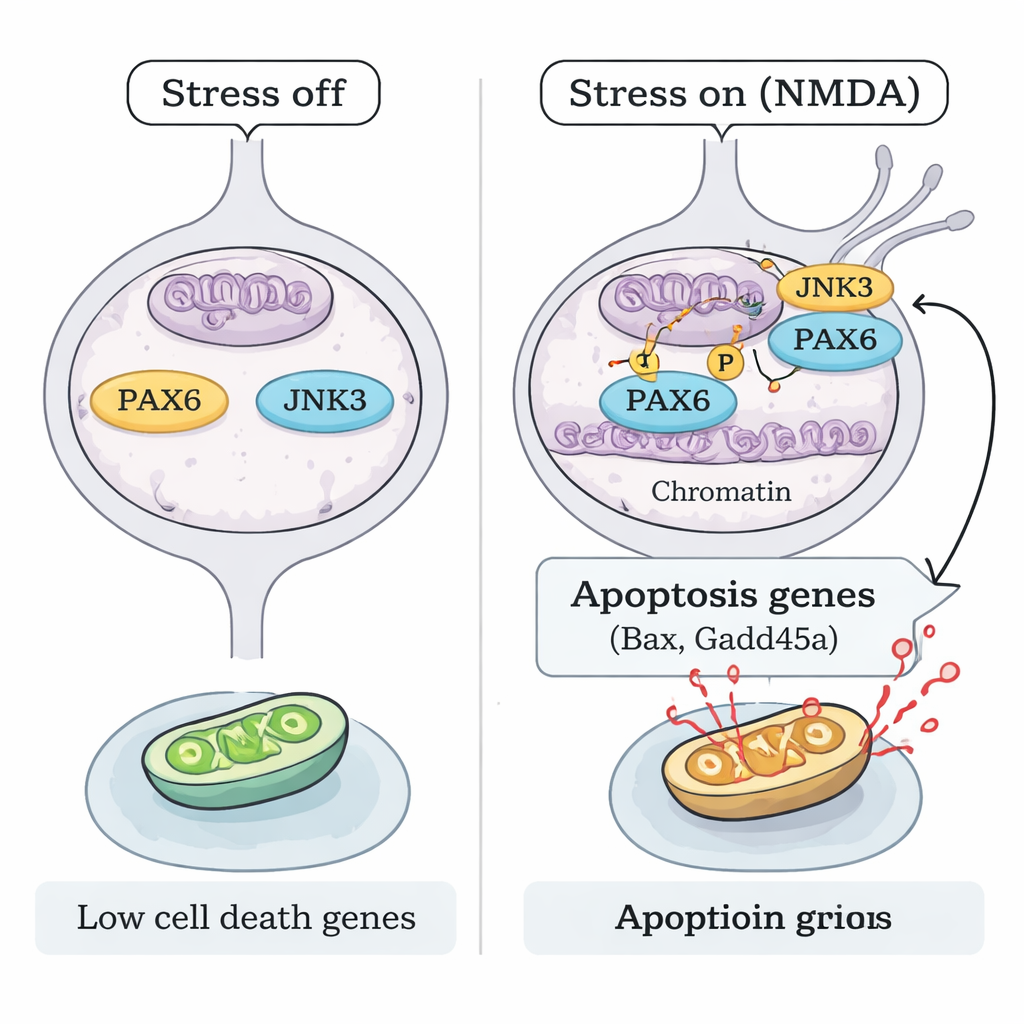
כיבוי תוכנית המוות לשמירה על הראייה
לבסוף בדקו החוקרים האם חסימת ציר JNK3–PAX6 מספיקה כדי להגן על תאים קריטיים לראייה. הן בעכברים שבהם PAX6 הושתק והן בעכברי חסרי JNK3, ה-RGCs נשמרו באופן משמעותי לאחר חשיפה ל-NMDA, עם פחות תאים מתים ומבנה רשתיתי בריא יותר. ממצא זה מצביע על מודל מכניסטי ברור: תחת מתח אקסיטוטוקסי, JNK3 מפוספורל את PAX6 שנשמר, מהופך אותו מבונה התפתחותי למפעיל עוצמתי של תוכנית גנים למוות בתאי RGC בוגרים. הפרעת הקשר הזה — על ידי השתקת PAX6 או נטרול JNK3 — שומרת על חיוניותם של רבים מהנוירונים האלה. עבור חולים, עבודה זו מרמזת שטיפולים עתידיים בגלאוקומה עשויים להתקדם מעבר להורדת הלחץ התוך-עיני ולמקד ישירות את המתגים הגנטיים שמחליטים האם תאי הרשתית יחיו או ימותו.
ציטוט: Kim, JY., An, MJ., Kim, J. et al. Aberrant maintenance of developmental transcription factor PAX6 promotes neuronal cell death via JNK3 signaling. Cell Death Dis 17, 161 (2026). https://doi.org/10.1038/s41419-026-08417-6
מילות מפתח: גלאוקומה, תאי גנגליון של הרשתית, PAX6, JNK3, נוירודגנרציה