Clear Sky Science · he
מיקוד ENO1 משכתב את פולריזציית המאקרופאגים כדי לעורר חיסון נגד גידול ומשפר את האפקט התרפואטי של הקרינה
הפיכת מגן הגידול למטרה
סרטן שורד לעתים קרובות לא רק על ידי גדילה מהירה, אלא על ידי נטרול שקט של ההגנות של הגוף. מחקר זה חוקר מולקולה מוסתרת על תאי הסרטן, הנקראת ENO1, שעוזרת לגידולים להתחמק ממערכת החיסון ולהיות עמידים לטיפולי קרינה. באמצעות פיתוח אנטי־גוף תרופתי חדש שמיועד ל־ENO1, החוקרים מגלים שניתן לרוקן את הגידול מהכימיקלים המגנים שלו, להעיר תאי חיסון ולהפוך את הקרינה ליעילה יותר במודלים של סרטן המעי הגס וסרטן השד המשולש־השלילי. 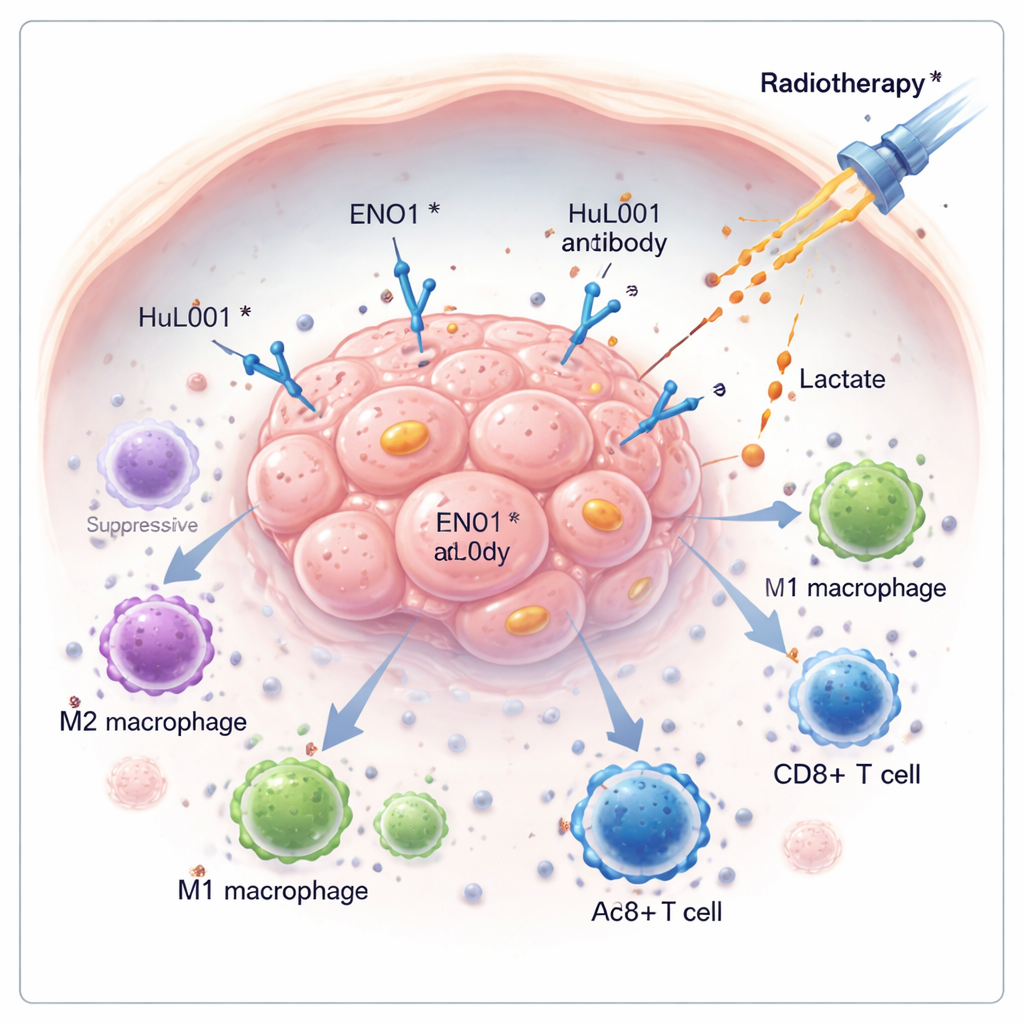
טריק מטבולי שמשתיק את החיסון
רבים מהגידולים משנים את הדרך שבה הם משתמשים באנרגיה, מפרקים סוכר בצורה שמייצרת כמויות גדולות של חומצת חלב גם כשהחמצן קיים. חומצת חלב זו מופרשת מתאי הסרטן ונבנית סביב הגידול, והופכת את הסביבה למקום חמור וחמוץ שמחליש את ההתקפה החיסונית. בעבודה זו, המחברים מתמקדים ב־ENO1, אנזים שמעורב בפרוק הסוכר ויכול להופיע גם על פני השטח של תאי סרטן. כשהוא נמצא על ממברנת התא, ENO1 משתף פעולה עם חלבון אחר, נשא בשם MCT4, כדי לסייע בהוצאת החומצה החלבית—מה שמזין סביבה המעדיפה את גדילת הגידול ומדכאת תאי חיסון.
איך הקרינה עלולה לחזור כבומרנג
תרפיית קרינה נועדה לפגוע ב‑DNA של הגידול ולהפעיל תגובות חיסוניות, אך יש לה גם השפעות לוואי במיקרו־סביבה של הגידול. הצוות גילה שאותות המופעלים על ידי מולקולה הנקראת TGFβ1, שמוגברים על ידי קרינה, מפעילים אנזים (PRMT5) שמבצע שינוי כימי ב־ENO1 ומעבירו לפני התא. ברגע שם, ENO1 מתקשר פיזית עם MCT4 כדי לייצב אותו ולקדם את יציאת החומצה החלבית. רמות גבוהות של ENO1 על פני התא נמצאו בחולים עם סרטן המעי הגס וסרטן השד המשולש־השלילי בשלבים מתקדמים וקושרו ליותר גרורות ולהישרדות פחות טובה, מה שמרמז שקרינה עלולה בטעות לחזק מגן מדכא חיסון מונע על ידי חומצת חלב סביב הגידולים.
שכתוב המאקרופאגים—חברים או אויבים
בהילה החמוצה סביב הגידולים, תאי חיסון הנקראים מאקרופאגים נדחפים למצב "מרפא" (שלעתים נקרא M2) שעוזר למעשה לגידולים על ידי דיכוי דלקת וסיוע בתיקון, במקום להרוס תאים סרטניים. החוקרים יצרו אנטי־גוף מזונן אנושי, HuL001, שמזהה את ENO1 גם על תאי סרטן של עכבר וגם של אדם. בתרביות תאים ובמודלים של עכברים, HuL001 שיבש את תמיכת ENO1 ב־MCT4, הקטין את שחרור החומצה החלבית ושינה את המאקרופאגים משלב M2 התומך בגידול לעבר מצב M1, שהוא תקיף יותר כלפי הסרטן וטוב יותר בבליעת תאים סרטניים. חשוב לציין ש־HuL001 לא הרג פשוט את המאקרופאגים; במקום זאת הוא חינך אותם מחדש תוך הגברה ישירה של מוות בתאי הסרטן.
לגרום לקרינה לעבוד חזק יותר
כאשר HuL001 שולב עם תרפיית קרינה במודלים של עכברים לסרטן המעי הגס ולסרטן השד המשולש־השלילי, הגידולים הצטמצמו יותר, גדלו חזרה יותר לאט ובחיות רבות נעלמו לחלוטין. 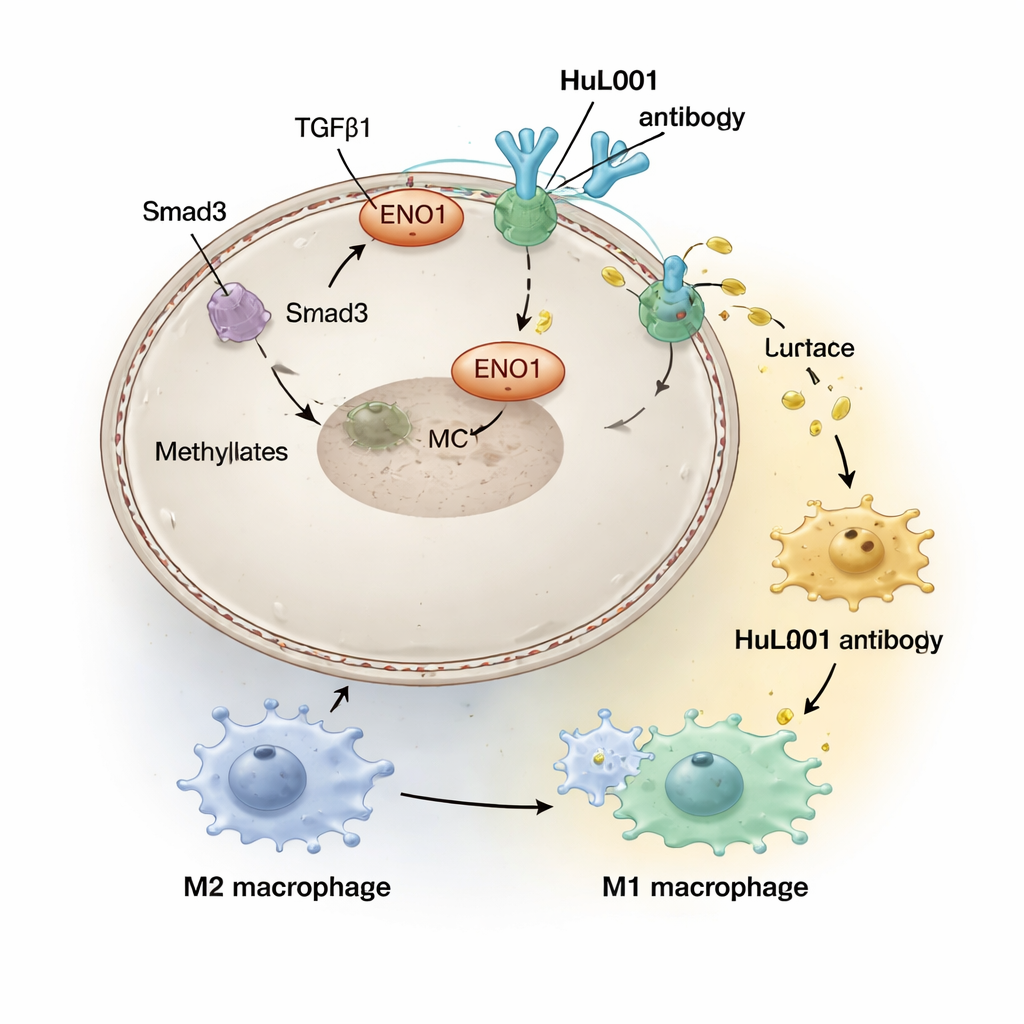
מנתיבים מורכבים להבטחה מעשית
ללא מומחיות מיוחדת, מסר המחקר הוא שכימיה של הגידול ושכונת תאי החיסון סביבו קשורים זה לזה עמוקות. ENO1 יושב בצומת: הוא מסייע לגידולים לשרוף סוכר, לייצא חומצת חלב ולגייס את סוג החיסון הלא נכון. על ידי חסימת ENO1 על פני השטח באמצעות אנטי־גוף ממוקד, החוקרים הצליחו להפחית הצטברות מזיקה של חומצת חלב, להפוך מאקרופאגים מעוזרים לגידול ללוחמים נגדו, ולהעצים את היעילות של הקרינה במודלים של סרטן שקשה לטפל בהם. אף ש־HuL001 עדיין אינו תרופה קלינית, העבודה מצביעה על כך שמיקוד בשומרי מטבוליזם כמו ENO1 עלול להפוך דרך עוצמתית להשתמש בהגנותיו של הגידול נגדו ולשפר טיפולים קיימים כגון תרפיית קרינה.
ציטוט: Lin, YS., Chang, HY., Hong, WZ. et al. Targeting ENO1 reprograms macrophage polarization to trigger antitumor immunity and improves the therapeutic effect of radiotherapy. Cell Death Dis 17, 194 (2026). https://doi.org/10.1038/s41419-026-08416-7
מילות מפתח: מטבוליזם הגידול, פולריזציית מאקרופאגים, תרפיית קרינה, אימונותרפיה, חומצת חלב