Clear Sky Science · he
מעבר לחילוף החומרים: חקירת ההשלכות הרגולטוריות והתרפויטיות של לקטט ול-לקטילציה במוות תאי המווסת על ידי סרטן
למה "תוצר פסולת" של סוכר חשוב בסרטן
עשורים רבים ראו בלקטט — החומר שגורם לשרירים עמוסים לבעור — כפסולת תאית. המאמר הסקירה הזה מראה שבסרטן לקטט רחוק מלהיות פסולת. הוא משמש כדלק, כאות כימי, ואפילו כמפסק שיכול לקבוע האם תאי הגידול יחיו או ימותו. הבנת התפקיד החבוי הזו עשויה לפתוח דרכים חדשות לגרום לתאי הסרטן להיכשל תוך שמירה על רקמות בריאות.
הקיצור הסוכרי שמשנה את תצורת תאי הסרטן
תאי סרטן ידועים ב"חיבה" שלהם לסוכר. גם כאשר חמצן זמין, הם מעדיפים לפרק גלוקוז במהירות ללקטט במקום לשרוף אותו במיטוכונדריה, שינוי הידוע כאפקט וורבורג. אסטרטגיה זו מאפשרת לגידולים לייצר אנרגיה ומרכיבי בנייה בקצב גבוה. הצפה של לקטט שמתקבלת נשאבת החוצה באמצעות נשאים ייעודיים, ויוצרת מיקרו-סביבה חומצית ועשירה במזון שתומכת בצמיחה ועוזרת לגידולים להתאים ללחצים כגון חוסר חמצן או כימותרפיה.
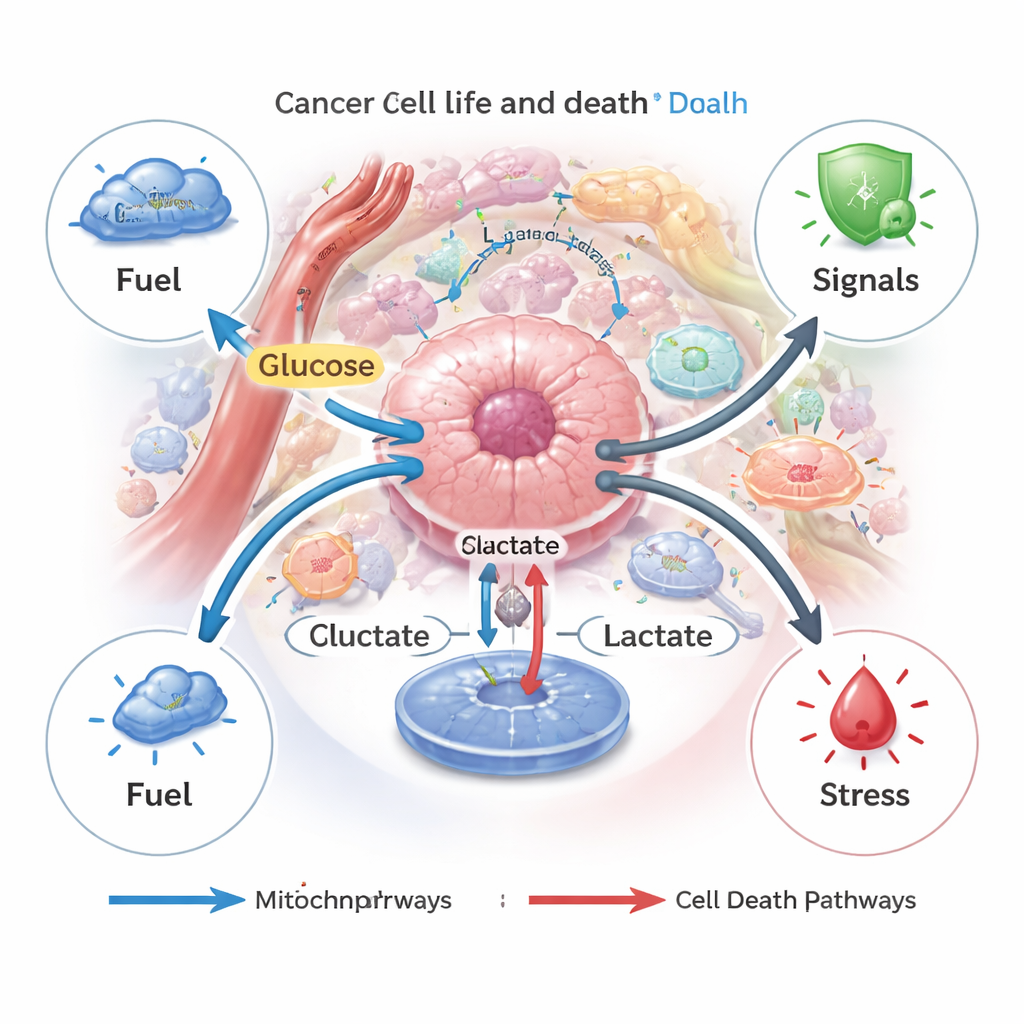
לקטט ככפתור לכיוונים שונים של מוות תאי
המוות התאי בגופנו נמצא בדרך כלל תחת שליטה הדוקה, ומסייע בהסרת תאים פגועים או מסוכנים. תאי סרטן לעתים קרובות בורחים מתכניות אלה. המחברים מתארים כיצד לקטט יכול גם לחסום וגם להפעיל מספר מסלולי מוות מווסתים — אפופטוזה ("התאבדות" תאי), אוטופאגיה (עיכול עצמי), פרוטופטוזה (נזק ממוקד לממברנה מונע על ידי ברזל), פיורופטוזה (פיצוץ דלקתי) וקופרופטוזה (התמוטטות מונעת על ידי נחושת). כאשר תאי סרטן מייצרים או מייבאים כמויות מתונות של לקטט, הם נוטים להשתמש בו כדלק ובאות הישרדות, ומפעילים מסלולים שמגינים מפני כימותרפיה, מחסור במזון או תרופות ממוקדות. אך כאשר לקטט מצטבר בתוך התאים, למשל אם יציאתו נחסמת, המתח החומצי והנזק המיטוכונדריאלי שעלולים להיווצר יכולים להפוך את המפסק ולדחוף את התאים לכיוון אפופטוזה או פרוטופטוזה.
לקטילציה: כאשר לקטט "כותב" על חלבונים
גילוי בולט לאחרונה הוא שלקטט יכול להיות מומר לתג כימי קטן ולהיות מצורף לרזידואי ליזין על חלבונים — שינוי הידוע כלקטילציה. אנזימים פועלים כ"כּוֹתְבִים" ו"מוחקים" של תגיות אלו, וקושטים הן היסטונים המקושרים ל-DNA והן חלבונים רבים אחרים. הסימנים האלה משנים אילו גנים מופעלים, כיצד אנזימים מתנהגים ואיך מייצבים רגולטורים מרכזיים. בסרטן, לקטילציה מכוונת עדינות את האיזון בין הישרדות להרס עצמי. היא יכולה, למשל, להגביר חלבונים שחוסמים אפופטוזה, להעלות מיחזור דרך אוטופאגיה, להגן מפני פרוטופטוזה על ידי הידוק בקרה על ברזל והגברה של מערכות נוגדות חמצון, או לשנות צורות חדשות של מוות כמו קופרופטוזה על ידי שינוי הטיפול בחלבונים רגישי-נחושת.
שיחה דו‑כיוונית בין מטבוליזם לתכניות מוות
הקשר אינו חד-צדדי: מסלולי המוות התאי מעצבים גם הם כיצד הגידולים משתמשים בסוכר ומייצרים לקטט. כאשר מיטוכונדריה ניזוקים בתחילת אפופטוזה או מיטופאגיה (הסרה סלקטיבית של מיטוכונדריות), תאים לעתים קרובות חוזרים לגליקוליזה מהירה, מה שמעלה את פליטת הלקטט. תאים תומכים בסביבה, כגון פיברובלסטים מקושרי-סרטן, יכולים לעבור כוונון דומה ולהפוך למפעלי לקטט שמזינים תאי גידול סמוכים. סוגים אחרים של מוות, כמו פרוטופטוזה, נוטים לדכא גליקוליזה ולכן להוריד רמות לקטט. התוצאה היא לולאת משוב דינמית שבה מטבוליזם ומנגנוני מוות מתאימים זה את זה בהתפתחות הגידול ובתגובה לטיפול.
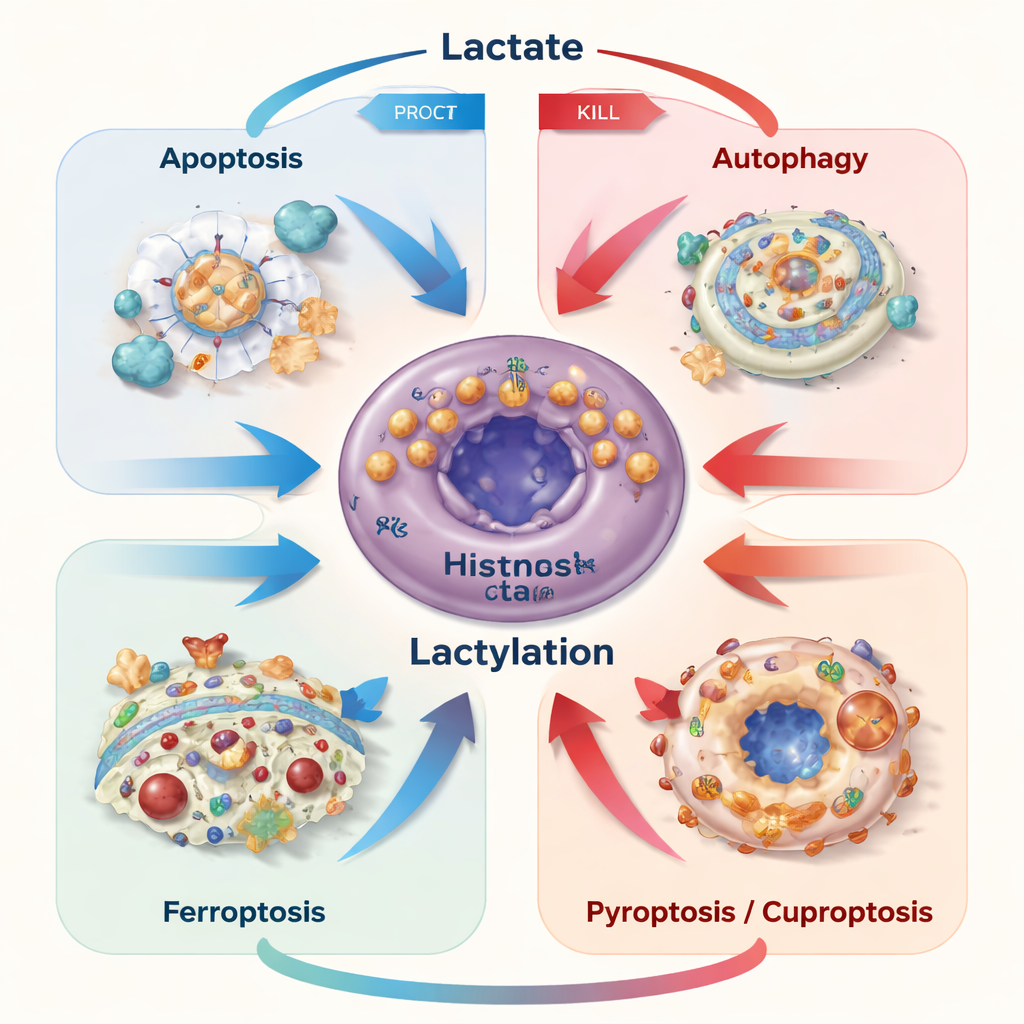
להפוך חולשה לאסטרטגיית טיפול
מכיוון שלקטט ול-לקטילציה יכולים להגן או להרוג תאי סרטן בהתאם להקשר, המחברים טוענים שטיפולים חייבים לעשות יותר מאשר רק לחסום את ייצור הלקטט. במקום זאת, טיפולים עתידיים עשויים לנתב מחדש באופן סלקטיבי את זרימת הלקטט, לשנות את נשאיו, או למקם בחוץ סימני לקטילציה ספציפיים כדי לדחוף את תאי הסרטן אל קצה בעוד שמשחזרים את פעילות תאי החיסון נגד הגידול שנעקבו על ידי הסביבה החומצית. מערכות אספקת תרופות חכמות וננודרוגות שמגיבות לרמות לקטט או pH מקומיות צצות כדרכים ליישם את הדיוק הזה. בפשטות, מסר המאמר הוא שמה שנראה פעם כפסולת מטבולית הוא למעשה כפתור שליטה רב-עוצמה על גורל התא הסרטני — ולמידה איך לסובב את הכפתור בדרך הנכונה עשויה להפוך טיפולים קיימים ליעילים בהרבה.
ציטוט: Chen, C., Lin, A., Zhao, J. et al. Beyond metabolism: exploring the regulatory and therapeutic implications of lactate and lactylation in cancer-regulated cell death. Cell Death Dis 17, 184 (2026). https://doi.org/10.1038/s41419-026-08410-z
מילות מפתח: לקטט, לקטילציה, מוות תאי בסרטן, חילוף חומרים בגידול, פרוטופטוזה (ferroptosis)