Clear Sky Science · he
PRMT6 נחוץ להתחלה ולהגברה של דלקת המושרת על ידי מקרופאגים בהתמצקות הטרוטופית על ידי הגברת ביטוי CCL2
כשהריפוי הולך רחוק מדי
לפעמים, לאחר פציעה קשה או ניתוח, הגוף משתדל לרפא כל כך חזק עד שבמקרה יוצר רקמת עצם חדשה במקום שבו לא אמורה להיות. מצב כואב זה, של צמיחת עצם לא רצויה ברקמות רכות, עלול לקבע מפרקים, לסבך קטיעות ולהקשות על תנועה יום‑יומית. הטיפולים הקיימים מוגבלים ולעתים קרובות אינם מצליחים למנוע חזרה של הבעיה. המחקר הזה חושף מתג מוקדם מרכזי במערכת החיסון שמקשר בין טראומה להיווצרות העצם החריגה—ומצביע על חלון קצר וחיוני שבו טיפול ממוקד עשוי לעצור את התהליך לפני שהוא מתחיל. 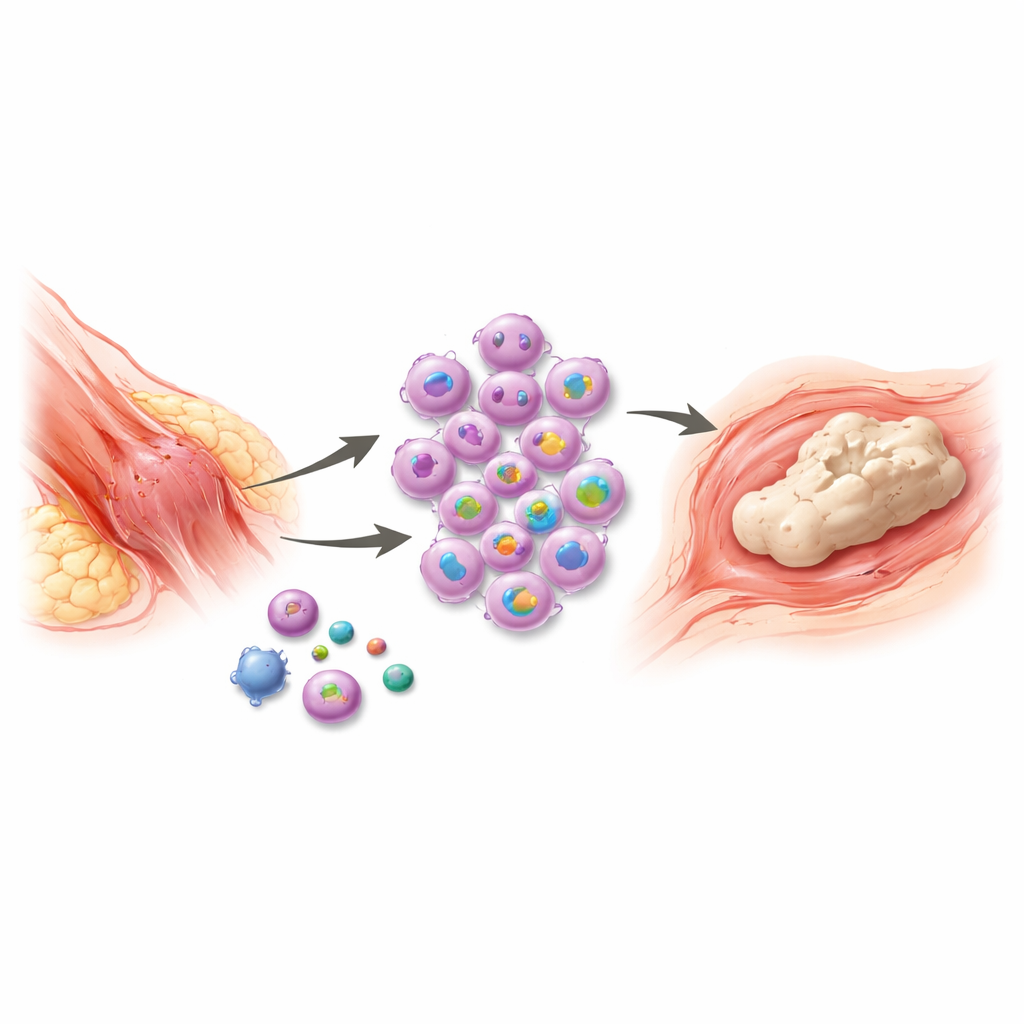
הבעיה של עצם במקום הלא נכון
לאחר טראומה גדולה, כגון כוויות, שברים או ניתוח אורתופדי, חלק מהמטופלים מפתחים אזורי עצם בתוך שרירים, גידים ורקמות רכות אחרות. העצם החדשה נוצרת בתהליך הדומה להתפתחות העצם הנורמלית, שמתחיל בדלקת ומסתיים ברקמה בוגרת ומינראליזטיבית. אף על פי שרופאים ידועים שמקרופאגים — תאי חיסון — הם מרכזיים בתגובה זו, השליטה שלב‑אחר‑שלב באופן שבו הם מדליקים ומתחזקים דלקת לא הייתה ברורה. בלי הבנה זו, טיפולים כמו תרופות נוגדות דלקת, קרינה או הסרה כירורגית מאוחרת מטפלים בעיקר בתוצאות ולא בגורם, והשכיחות לחזרה של המצב גבוהה.
המתווך המרכזי של הדלקת
באמצעות מודל עכבר שמשלב פגיעה בגיד עם כוויה—חיקוי קרוב של טראומה קשה בבני אדם—החוקרים עקבו אחרי מה שקורה באתר הפציעה לאורך זמן. הם ראו הצטברות מהירה של מקרופאגים בימים הראשונים לאחר הפציעה, ששרדו כאשר העצם החריגה נוצרה. כאשר הם הפחיתו תאים אלה, העצם העודפת כמעט ונעלמה, והרקמה הסובבת הראתה פחות שיבוש בכלי דם ותאי תמך. קריאת גנים מעמיקה מהרקמה הפצועה הדגישה מולקולה אחת במקרופאגים שבולטת במיוחד: PRMT6, אנזים שמשנה חלבונים ועוזר לשלוט אילו גנים דולקים.
כפתור עוצמה מולקולרי לדלקת
הצוות מצא שרמות PRMT6 במקרופאגים עלו במהירות לאחר פציעה ובתגובה לאותות סכנה ומרכיבים חיידקיים במעבדה. עכברים חסרי PRMT6, או עכברים שבהם PRMT6 הופחת בחירה רק במקרופאגים, הציגו הרבה פחות מקרופאגים באתר הפציעה ופיתחו הרבה פחות עצם חריגה. חשוב לציין שהגידים הפצועים בבעלי החיים האלה דווקא החלימו טוב יותר, עם סידור רקמתי מסודר פחות הצטלקות. זה מצביע על כך ש‑PRMT6 אינו דרוש לתיקון בריא, אלא פועל ככפתור עוצמה שמגביר דלקת מזיקה. כשהחוקרים חסמו את PRMT6 בתרופה, הטיפול עבד רק אם ניתן מוקדם—בשבועות הראשונים לאחר הפציעה. התחלת הטיפול מאוחר יותר כמעט ולא השפיעה, מה שמגלה חלון תרפי צר אך עוצמתי.
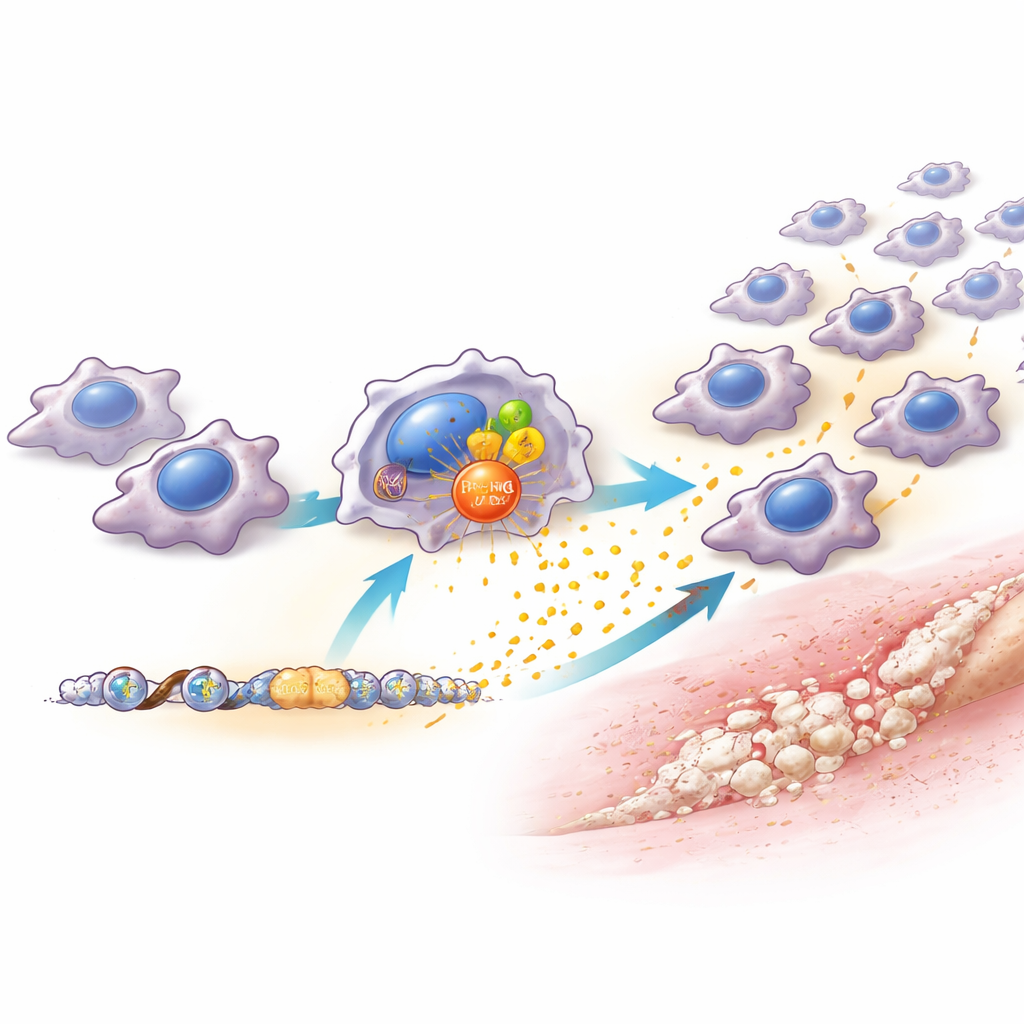
איך אות אחד מושך תאי חיסון רבים
כדי להבין איך PRMT6 מפעיל את האפקט הזה, המדענים חקרו מקרופאגים בפירוט. בהעדר PRMT6, תאים אלה ייצרו כמויות נמוכות הרבה יותר של מספר כימיקלים שמושכים תאים, ובמיוחד אחד שנקרא CCL2, שבדרך כלל מושך מונוציטים ומקרופאגים נוספים מהמחזור הדם אל רקמה פצועה. PRMT6 מסייע להפעיל את גן CCL2 בשתי דרכים: הוא משתף פעולה עם הבקר הדלקתי המוכר NF‑κB, והוא מסמן כימית חלבונים שעוטפים את ה‑DNA כדי להקל על קריאת הגן. כתוצאה מכך, מקרופאגים עם רמות גבוהות של PRMT6 משחררים יותר CCL2, מושכים מקרופאגים נוספים ויוצרים "מרכז דלקתי" שתומך בכלי דם ובתאי אב שמייצרים עצם. כאשר CCL2 הופחת באופן ספציפי רק במקרופאגים, התוצאה חקה במידה רבה את איבוד ה‑PRMT6—פחות מקרופאגים, אזורים דלקתיים חלשים יותר ופחות עצם עודפת. החזרת CCL2 החמיצה באופן חלקי את זרימת המקרופאגים וצמיחת העצם החריגה.
הזדמנות ממוקדת למניעת עצם לא רצויה
לסיכום, המחקר מראה ש‑PRMT6 במקרופאגים פועל כמגבר אפיגנטי מוקדם: הוא מייצב אות כימי מרכזי שמגייס עוד תאי חיסון, אשר בתורם דוחפים יצירת עצם במקום שלא שייך לה. מכיוון שחסימת PRMT6 רק בשלב הדלקתי המוקדם צמצמה באופן חד את העצם הלא רצויה בעוד שהיא השאירה את ריפוי הגידים התקין—ואף שיפרה את סידור הרקמה—המסלול הזה מציע אסטרטגיה חדשה וواعدה. למעשה, קורס קצר ומתוזמן היטב של טיפול ממוקד נגד PRMT6 לאחר טראומה קשה או ניתוח עשוי למנוע נכות לטווח הארוך בעקבות עצם אקטופית, בלי לפגוע ביכולת הטבעית של הגוף להתאוות.
ציטוט: Chu, W., Peng, W., Wu, Z. et al. PRMT6 is required for initiating and amplifying macrophage-induced inflammation in heterotopic ossification by increasing CCL2 expression. Bone Res 14, 29 (2026). https://doi.org/10.1038/s41413-026-00512-w
מילות מפתח: התמצקות הטרוטופית, מקרופאגים, דלקת, בקרה אפיגנטית, איתות CCL2