Clear Sky Science · he
היווצרות צלקת פיברוטית המושתתת על TGF-β מגבילה שיקום לאחר פגיעה בחוט השדרה
למה צלקות בחוט השדרה חשובות
כשחוט השדרה נפגע קשה, רבים נותרו עם שיתוק קבוע או אובדן תחושה כי סיבי עצב שניזוקו אינם מצליחים לצמוח מחדש. המחקר בוחן שאלה פשוטה אך קריטית: מה בעצם חוסם את הצמיחה הזו — והאם ניתן להסיר את המחסום באופן בטוח? על ידי גילוי איך סוג מסוים של צלקת נוצר בתוך החוט הפגוע, המחברים מצביעים על דרך חדשה לסייע למערכת העצבים לתקן את עצמה.
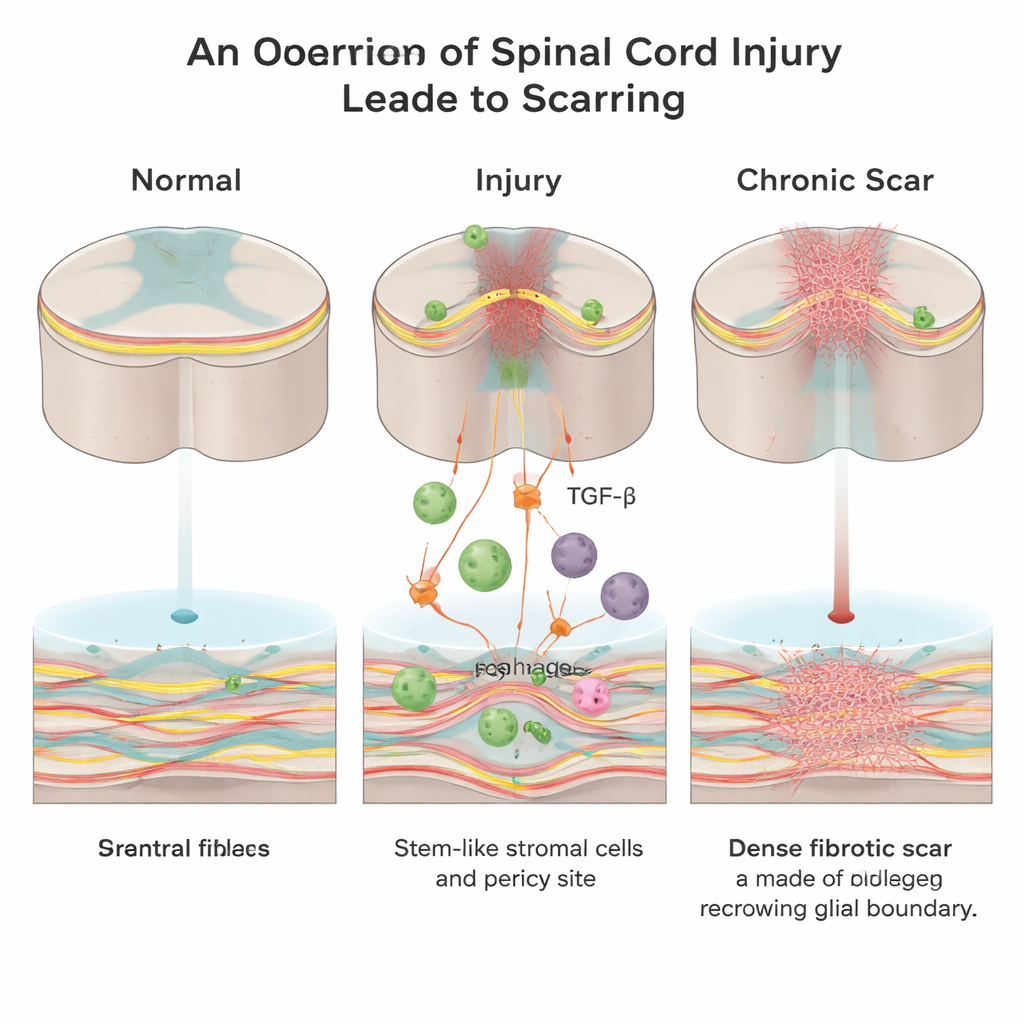
קיר מוסתר בתוך הפגיעה
לאחר פגיעה בחוט השדרה, הגוף ממהר לאטום את הפצע. נוצרים שני סוגים עיקריים של רקמת צלקת: צלקת גליאלית שנוצרת על ידי תאי תמיכה הנקראים אסטרוציטים, וצלקת פיברוטית העשירה בקולגן, פיברונקטין ותאי פיברובלסט. בעוד שלצלקת הגליאלית עשויים להיות תפקידים מגינים, הצלקת הפיברוטית יוצרת קיר צפוף — גם פיזי וגם כימי — שסיבי עצב צומחים מתקשים לעבור דרכו. עד כה המדענים ידעו פחות על אופן הופעת הליבה הפיברוטית ואילו אותות מניעים את היווצרותה.
תפקיד תאי המערכת החיסונית ואות רב עוצמה
בעבודה בעכברים בוגרים, החוקרים התרכזו במולקולת איתות הנקראת גורם צמיחה משנף-בטא (TGF‑β), המסייעת לתאם תיקון פצעים בכל הגוף ולעתים מוגזמת בפעילותה במחלות פיברוטיות. הם מצאו כי לאחר פגיעה בחוט השדרה, תאי מערכת החיסון הפולשים המכונים מקרופאגים הופכים למקור עיקרי של TGF‑β1 פעיל באתר הנגע. עלייה זו ב‑TGF‑β1 מגייסת תאי מזנכימה סטרומאליים/גזעיים מקומיים ותאים קשורים לכלי דם המכונים פריציטים ודוחפת אותם להפוך לפיברובלסטים — אותם תאים שמפרישים את הרקמה העשירה בקולגן שיוצרת את הצלקת הפיברוטית.
החלשת האות כדי לפתוח מסלול
כדי לבדוק האם מסלול זה באמת גורם לצלקת מזיקה, הצוות השתמש במספר תחבולות גנטיות בעכברים. כאשר הסירו מקרופאגים, או מחקו את גן TGF‑β1 רק בתאי שושלת המקרופאג, כמות הרקמה הפיברוטית בחוט הפגוע ירדה באופן חד, ויותר סיבי עצב ונתיבים המכילים סרוטונין הצליחו לחצות את אזור הפגיעה. בדומה לכך, מחיקה של קולטן ה‑TGF‑β באופן ספציפי בפריציטים צמצמה את תגובתם ל‑TGF‑β, הובילה לפחות הצטברות קולגן ושיפרה תנועה ותחושה במבחני התנהגות. חשובה מכך, פריציטים ותאים דמויי‑גזע קשורים עדיין התקיימו אך היו פחות נוטים להפוך לפיברובלסטים היוצרים צלקת.
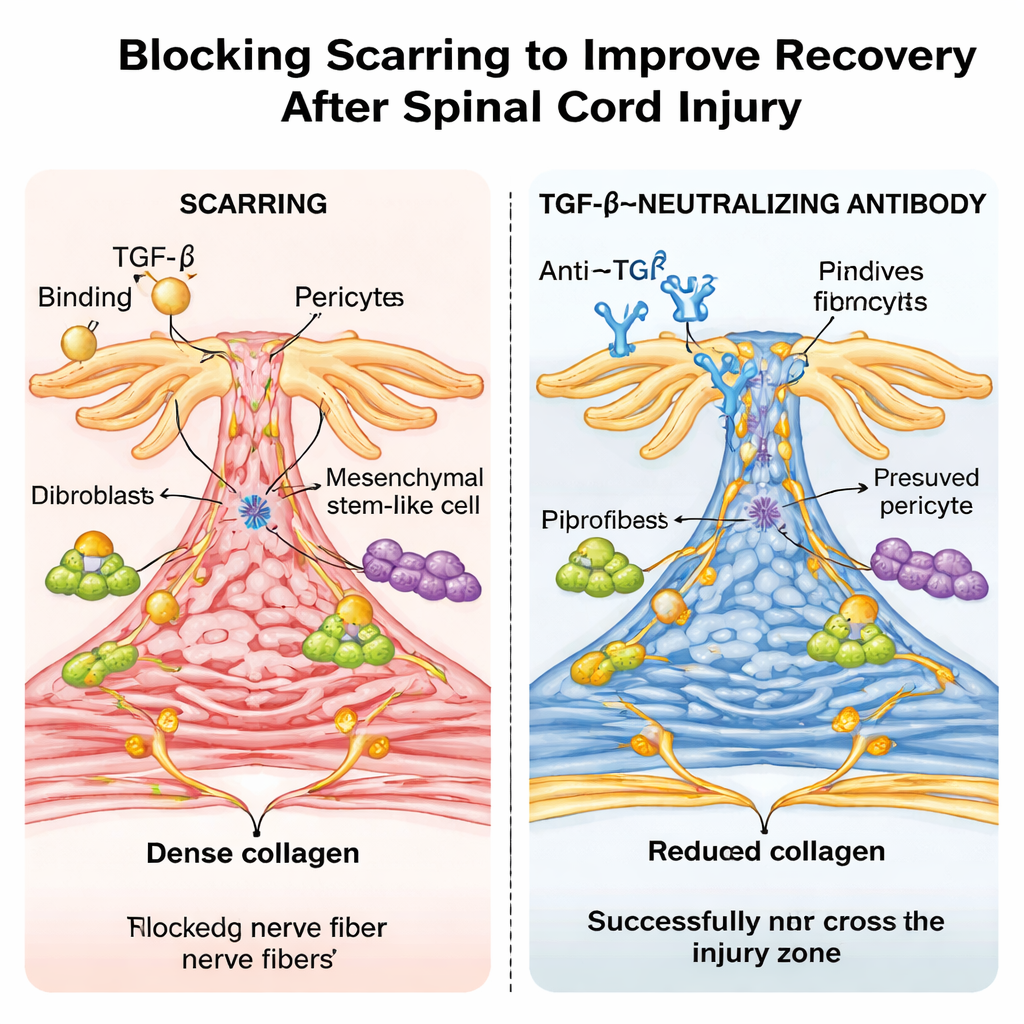
נוגדן בדמוי‑תרופה ואפקט גיל מלא הפתעה
החוקרים ניסו אז גישה הרלוונטית יותר קלינית: טיפול בעכברים רגילים בנוגדן מעבדתי שמנטרל את TGF‑β. מינונים חוזרים לאחר הפגיעה הורידו רמות של TGF‑β פעילות בדם ובחוט השדרה, הקטינו את הצלקת הפיברוטית ואיפשרו לסיבי עצב לגשר על הנגע ביעילות רבה יותר, עם שיפורים בולטים בהליכה ובתפקוד החושי. רצף ה‑RNA בתא בודד אישר כי גנים רגישים ל‑TGF‑β היו פעילים מאוד בסוגי התאים יוצרי‑הצלקת בעכברים שלא טופלו ונדכאו על ידי הנוגדן. באופן בולט, כאשר ביצעו את אותו סוג של מעיכה בחוט השדרה בעכברי ניו‑בורן, בעלי החיים החלימו כמעט ללא צלקת פיברוטית, לא הראו הפעלת TGF‑β ניתנת לזיהוי באתר הפגיעה, והתאוששו לתנועה כמעט‑נורמלית — בדומה לתיקון נטול צלקת הנצפה בחלק מהחיות שאינן יונקות.
מה המשמעות של זה לטיפול עתידי
ביחד, הממצאים מציעים שהפעלה מופרזת של TGF‑β לאחר פגיעה בחוט השדרה מסיטה תאים מועילים לתיקון לבניית קיר פיברוטי נוקשה החוסם צמיחת עצבים ושיקום תפקודי. על ידי מניעת הפעלה זו — בין אם באמצעות מטרה על ייצור ה‑TGF‑β במקרופאגים, חסימת הקולטנים שלו בפריציטים ותאים סטרומאליים, או שימוש בנוגדן מנטרל — ייתכן שניתן יהיה לצמצם את הצלקת המזיקה תוך שמירה או אפילו חיזוק של תגובות רקמה מועילות יותר. למרות שהעברה של אסטרטגיות אלה לאדם תדרוש מחקר זהיר כדי להימנע מתופעות לוואי, עבודה זו מדגישה את ההצטלקות הפיברוטית המונעת על‑ידי TGF‑β כמחסום מרכזי, ושניתן לשקול אותו כמטרה לטיפול בחוט השדרה.
ציטוט: Pan, D., Wu, P., Noller, K. et al. TGF-β-induced fibrotic scar formation limits recovery of spinal cord injury. Bone Res 14, 27 (2026). https://doi.org/10.1038/s41413-026-00507-7
מילות מפתח: פציעה של חוט השדרה, צלקת פיברוטית, TGF-בטא, מקרופאגים, שחזור עצבי