Clear Sky Science · he
HIF-1α ו-BMAL1 בהתחדשות עצם: דיאלוג בין תגובת היפוקסיה למשבצת הצירקרדיאנית
למה שברים מחלימים טוב יותר משחשבתם
כשהעצם נשברת או כששולפים שן, גופנו שוקע בשקט בפרויקט תיקון מתואם להפליא. עמוק באזור הפגוע רמות החמצן צונחות והשעון הביולוגי הפנימי ממשיך לתקתק. מאמר זה בוחן כיצד שני מפסקים ראשיים — HIF‑1α, החיישן לחוסר חמצן, ו‑BMAL1, חלבון מרכזי של השעון — פועלים יחד כדי להנחות את תאי העצם דרך דלקת, צמיחת רקמה חדשה והשבת חוזק סופי. הבנת השותפות הזו עשויה לשפר טיפולים לשברים, אוסטאופורוזיס, דלקת מפרקים ואפילו שתלים דנטליים.
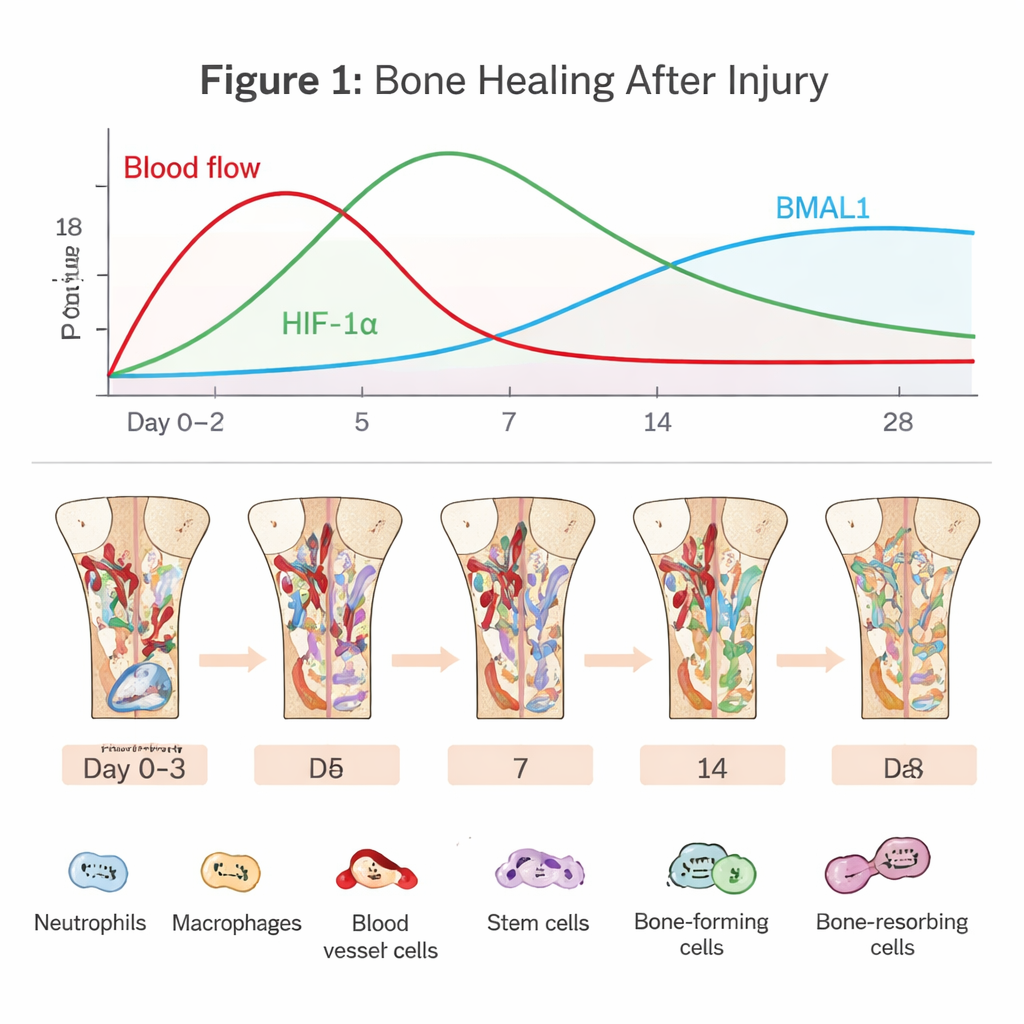
הדרמה הנסתרת בתוך עצם מתרפאת
התחדשות העצם מתחילה מהרגע בו כלי דם נקרעים. נוצר קריש דם שמנתק חלק גדול מאספקת החמצן ויוצר כיס קשה של חוסר חמצן. תאי חיסון כגון נויטרופילים ומקרופאג’ים ממהרים לנקות שברי רקמה ולהדוף מיקרוביים. במקביל מגויסים תאי גזע במח העצם ותאי כלי דם כדי לבנות מחדש את האזור. שלב הדלקת המוקדם הזה הוא חרב פיפיות: פרץ קצר ומתוזמן היטב של דלקת מניע את התיקון, אך אם הוא נמשך מדי או קיצוני מדי, ההחלמה עלולה להיתקע או לכשל. המאמר מדגיש שהניווט בשביל הצר הזה תלוי במידה רבה באופן שבו התאים חשים חמצן וזמן.
כיצד תאים מנצלים חוסר חמצן לטובתם
במרחב השבר העני בחמצן, החלבון HIF‑1α מייצב את עצמו ומפעיל גנים המסייעים לתאים להסתגל. הוא דוחף תאי אנדותל לשגשג ולצמוח כלי דם חדשים, כדי להבטיח אספקת חמצן ומזון לאזור הפגוע. הוא גם מרפרם את המטבוליזם התאי לכיוון גליקוליזה, דרך ליצירת אנרגיה שעובדת גם כשהחמצן דל. עבור תאי גזע וּאוסטאובלסטים (תאי בניית העצם), הפעלה מתונה של HIF‑1α יכולה להגביר התרבות, נדידה וצמיחת עצם, בחלקה על ידי הגדלת גורמים כמו VEGF שמקשרים בין היווצרות כלי דם ליצירת עצם חדשה. אך אם ההיפוקסיה חמורה מדי או ממושכת, מולקולות לחץ ומינים רעילים של חמצן (ROS) מצטברים, מה שמטה את האוסטאובלסטים לעבר מוות ומשפעל אוסטאוקלסטים שממגרדים עצם. אות ההיפוקסיה הזה יכול אפוא לתמוך או לחבל בהחלמה, בהתאם לעוצמה ומשך הזמן שלו.
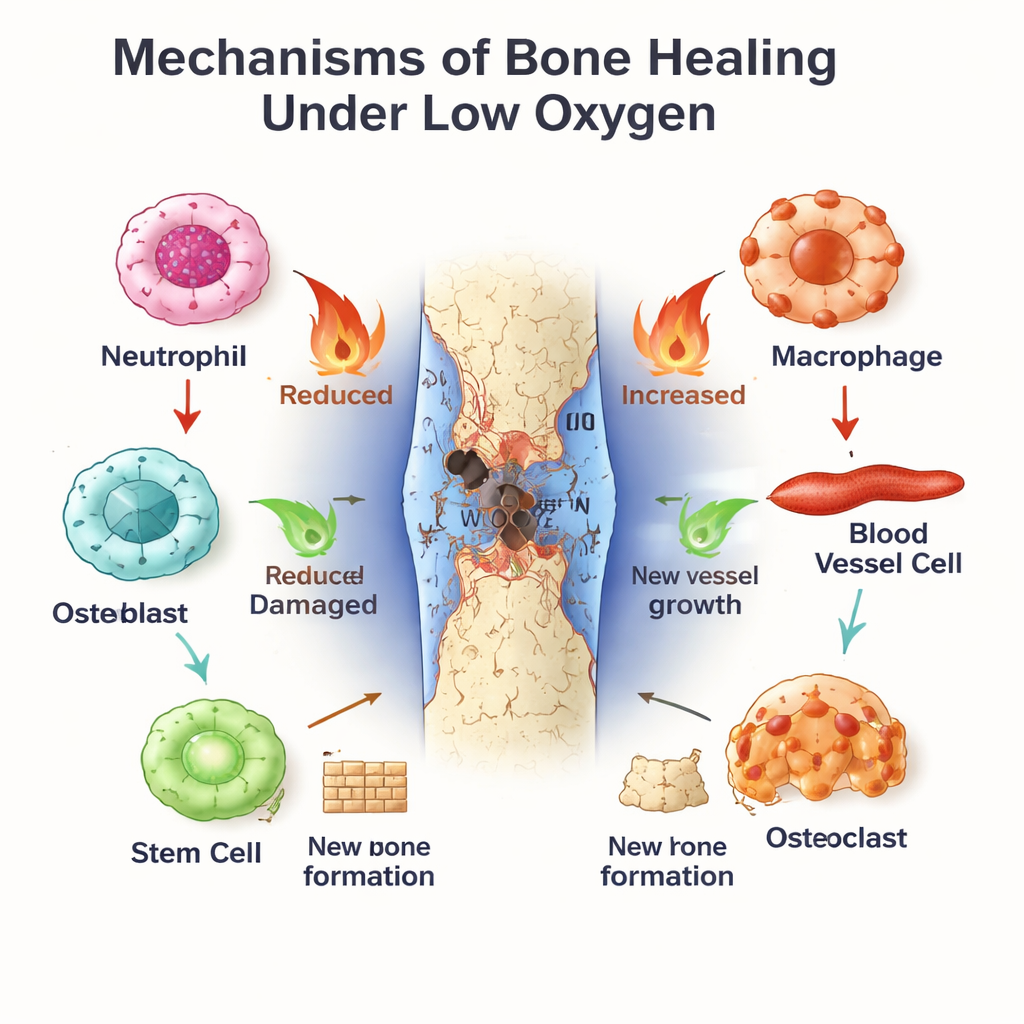
השעון הפנימי של הגוף כמנהל תיקון העצם
פועל במקביל השעון הצירקדיאני, שמירה מולקולרית של זמן שנמצאת כמעט בכל תא. BMAL1, אחד הרכיבים המרכזיים שלו, מסייע לקבוע קצבי יום-לילה בפעילות החיסונית, בהתנהגות כלי הדם ובהתמיינות תאי הגזע. נויטרופילים ומקרופאג’ים מציגים הבדלי זמן-יום בעוצמת התגובה לפגיעה ובמהירות שבה הם מזדקנים או עוברים ממצב דלקתי (בצורת M1) למצב מרפא (בצורת M2). בתאי כלי דם ובתאי גזע מח העצם, BMAL1 מקדם התרבות בריאה ויצירת עצם מסודרת, בחלקה על ידי עדכון מסלולים של גדילה כמו Wnt ו‑TGF‑β/SMAD. כאשר BMAL1 מופרע — על ידי פגמים גנטיים, עבודה במשמרות או מחלות מטבוליות — העצמות נוטות לאבד מסתן, תאי הגזע מתעייפים והאיזון בין יצירת עצם והתמוטטותה נוטה לאובדן.
שיחה בין חישת חמצן לשעון הגוף
ליבת הסקירה היא ה”דיאלוג” המתהווה בין HIF‑1α ו‑BMAL1. שני החלבונים הללו חולקים מבנים דומים ויכולים להתקשר פיזית, אף ליצור זוגות מעורבים שקושרים DNA ושולטים במערכי גנים חופפים. כל אחד מהם יכול להשפיע על ייצורו ויציבותו של האחר, וליצור לולאות משוב שקושרות את תזמון המחזור יום‑לילה לאופן שבו תאים מגיבים להיפוקסיה. יחד הם מנהלים גם את מאזן הרדוקס התאי — כמה מיני חמצן תגובתיים מזיקים נוצרים מול כמות היכולת האנטי‑אוקסידנטית הזמינה — והם מווסתים במשותף אנזימים מרכזיים שמכריעים האם התאים נשענים יותר על נשימה תלויה חמצן או על גליקוליזה חופשית חמצן. שליטה משותפת זו מסייעת לקבוע האם סביבת השבר תעדיף בנייה שיקומית או דלקת מוגזמת וספיגת עצם.
מה משמעות הדבר למחלה וטיפול
אותה שותפות HIF‑1α–BMAL1 מופיעה במצבים רבים הקשורים לעצם. בעובדי משמרות, שינה מופרעת ותאורה מעוותת סביר שיעקרו את BMAL1, יגבירו לחץ חמצוני ויתקלו בהכוונת התיקון על‑ידי HIF‑1α, מה שתורם לאוסטאופורוזיס. בסוכרת, רמות סוכר גבוהות מחלישות גם את תפקוד השעון וגם את איתות ההיפוקסיה, פוגעות בצמיחת כלי דם וביצירת עצם מונעת על‑ידי תאי גזע. באוסטאוארתריטיס, איבוד BMAL1 בתאי הסחוס משבש את קצבם ואת יחסיהם המגינים עם HIF‑1α, ומאיץ את התפוררות הסחוס. סביב שתלים טיטניום, היפוקסיה מבוקרת ופעילות צירקדיאנית בריאה נראות תומכות באוסאואינטגרציה טובה יותר, מה שמרמז כי ציפויים עתידיים לשתלים עשויים לעודד בעדינות הן HIF‑1α והן BMAL1. בסך הכל מסקנת המאמר היא שהתחדשות עצם מוצלחת תלויה לא רק באילו תאים נוכחים, אלא במהירות שבה הם קוראים חמצן וזמן — ולפיכך מיקוד בדיאלוג הזה עשוי לפתוח דרכים חדשות להחלמה מהירה וחזקה יותר.
ציטוט: Weng, Y., Xiong, J., Zhao, Q. et al. HIF-1α and BMAL1 in bone regeneration: crosstalk between hypoxia response and circadian rhythm. Bone Res 14, 25 (2026). https://doi.org/10.1038/s41413-026-00506-8
מילות מפתח: התחלבות עצם, קצב יומי (צירקדיאני), היפוקסיה, אוסטאופורוזיס, החלמת שברים