Clear Sky Science · he
שינויים מבניים גנומיים תורמים לאינפורמציה פרוגנוסטית בחולים עם לוקמיה מיאלואידית חריפה ציטוגנטית-נורמלית
מדוע שינויים זעירים ב‑DNA חשובים לחולי לוקמיה
מבוגרים שאובחנו עם לוקמיה מיאלואידית חריפה (AML) עוברים יותר ויותר בדיקות גנטיות כדי לחזות עד כמה הטיפול צפוי להצליח. עם זאת, כמעט למחצית מהחולים בדיקות הכרומוזומים הסטנדרטיות נראות "נורמליות", ותחזית העתיד שלהם נשארת קשה להערכה. מחקר זה מראה ששחזורים זעירים ב‑DNA — קטנים מדי כדי להיראות במיקרוסקופ — יכולים להבחין באופן חד בצוות חולים שלמחלתם אופי הרבה יותר תוקפני ממה שכלים קיימים מצביעים עליו.
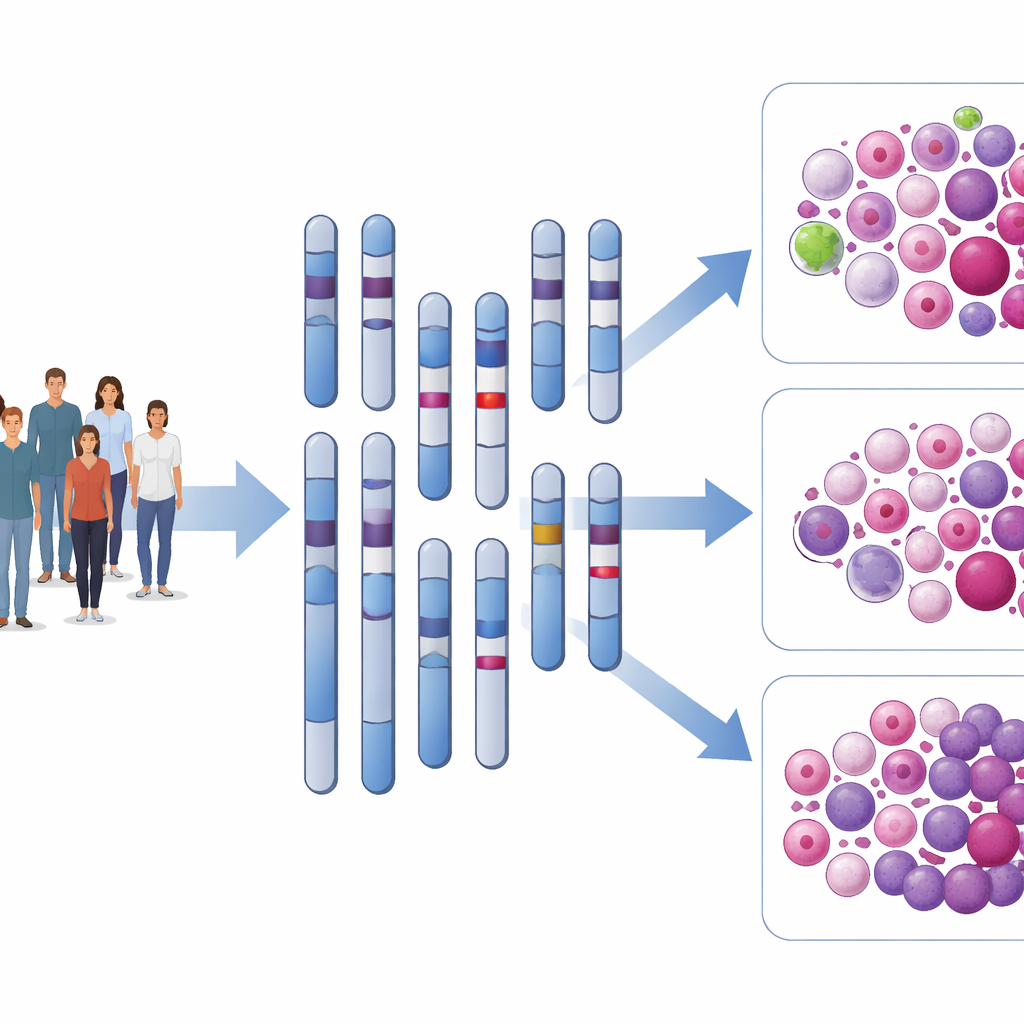
לראות מעבר לכרומוזומים שנראים תקינים
AML היא סרטן דם שבו תאי דם לבנים לא בשלים תופסים מקום מתאים בתאי המח העצם. רופאים בודקים שגרתי כרומוזומים ומוטציות גנטיות ידועות כדי למיין חולים לקבוצות סיכון נוחות, בינוניות או בעייתיות, שמנחות החלטות כגון האם להציע השתלת תאי גזע מוקדם. עם זאת, כ‑45% מהחולים מראים AML "ציטוגנטית‑נורמלית" — כלומר כרומוזומיהם נראים שלמים — אף על פי שהתוצאות שלהם נעות בין הישרדות לטווח ארוך להישנות מהירה. החוקרים שיערו ששחזורים תת‑נראים, המכונים שינויים מבניים, עשויים להסביר את המגוון החבוי הזה.
שימוש בריצוף בטווח ארוך כמקדם הגדלה גנטי
לחיפוש אחרי שינויים חבויים אלה השתמש הצוות בריצוף גנומי מלא בטווח ארוך, טכנולוגיה הקוראת מקטעי DNA ארוכים ומתאימה לזיהוי החדרות, חסרות ושחזורים אחרים. הם יישמו אותה על תאי לוקמיה מ‑162 מבוגרים שטופלו אינטנסיבית והשתתפו בשני ניסויים קליניים, ובאמצעות סינון קפדני להסרת וריאנטים תורשתיים וארטיפקטים טכניים צמצמו יותר מאלפיים ממצאים גולמיים ל‑118 שינויים מבניים אמינים המפוזרים בעצמיות. ברובם היו החדרות או חסרות קטנות הממוקמות באזורים לא‑מקודדים של הגנום, כגון אינטרונים ואזורים רגולטוריים, ולא בתוך רצפי קידוד חלבון ישירים.
חמישה שינויים קטנים מגדירים קבוצה בסיכון גבוה מאוד
החוקרים בדקו אילו מתוך 118 השינויים האלה קשורים לאורך החיים של החולים ולמשך הזמן חופשי מאירועים כמו הישנות או כישלון בתגובה לטיפול. באמצעות למידת מכונה ומודלים של הישרדות זיהו הם חמישה שינויים מבניים ספציפיים שסימנו באופן בלתי תלוי תוצאות גרועות בהרבה. חולים שנשאפו לפחות אחד מה"שינויים בסיכון גבוה" האלה — כ‑13–15% מהנבדקים — היו בעלי סיכויים נמוכים יותר להגיע לרמיסיה מלאה, חוו יותר הישנויות, והיה להם משך חיים קצר בהרבה, בדרך‑כלל פחות משנה. ההשפעות נשמרו גם לאחר התחשבות במוטציות ידועות כמו FLT3 ו‑NPM1 והישארו מובהקות בקבוצת אימות של 149 חולים נוספים שנבדקו באמצעות בדיקות ממוקדות.
שיפור מדדי הסיכון הקיימים והסבר מנגנוני
הנחיות אירופיות נוכחיות ממקמות את כל החולים הציטוגנטית‑נורמליים לקטגוריות רחבות על סמך מוטציות מסוימות, אך לעתים אינן מצליחות להפריד בבירור בין סיכון בינוני לבעייתי. בהוספת הנוכחות של כל אחד מחמשת השינויים בסיכון גבוה כקטגוריה חדשה של "סיכון מאוד גרוע" יצרו המחברים סכמה חדשה בעלת ארבע רמות. ניקוד זה משופר חזה טוב יותר הישרדות כוללת והישרדות חופשית מאירוע לעומת המודל הסטנדרטי, במיוחד עבור חולים עם מוטציות NPM1, שבדרך‑כלל מסווגים כנוחים אך הופיעו עם תוצאות רעות מאוד כשהיו גם נושאים את השינויים המבניים האלה. ניסויים במעבדה תמכו בבסיס ביולוגי: השינויים בסיכון גבוה נקשרו לשינויים בפעילות גנים סמוכים, ושינוי ניסיוני של רמות חלק מהגנים הללו במודלים תאיים פגע בצמיחת תאים ובבקרת מחזור התא, תכונות התואמות להתנהגות לוקמיה תוקפנית יותר.
משמעות הדבר עבור חולים וטיפול
במונחים יום‑יומיים, עבודה זו מציעה שחלק מהחולים ב‑AML שלכרומוזומיהם נראים תקינים ושמצוינים כיום כ"בינוניים" או אפילו "נוחים" עלולים, בפועל, להסתיר צורה הרבה יותר מסוכנת של המחלה. קבוצה קטנה של שחזורים זעירים ב‑DNA — אפשרית לזיהוי באמצעות ריצוף מודרני או בדיקות מעקב ממוקדות — יכולה לזהות חולים אלה מוקדם. הכרה בקבוצת הסיכון הגבוהה החבויה הזו עשויה לסייע לרופאים לכוון אותם לטיפולים אינטנסיביים יותר או לניסיוניים ומעקב צמוד יותר, במטרה לשפר תוצאות שנמצא כיום כי הן גרועות מאוד.
ציטוט: Bartalucci, N., Mannelli, F., Tarantino, D. et al. Genomic structural variations contribute to inform prognosis in patients with cytogenetically normal acute myeloid leukemia. Blood Cancer J. 16, 37 (2026). https://doi.org/10.1038/s41408-026-01465-3
מילות מפתח: לוקמיה מיאלואידית חריפה, שינוי מבני, סיווג סיכון גנומי, ריצוף בטווח ארוך, מוטציית NPM1