Clear Sky Science · he
מיקרוRNA-132/212 מדכא באופן שלילי את התגמול האופיואידי על ידי מטרה של משאבת הדופמין באיזור הטגמנטלי הוונטרלי
מדוע המחקר הזה חשוב לחיים היומיומיים
משככי כאבים אופיואידיים ותרופות קשורות יכולים להעניק הקלה אך גם נושאים סיכון חמור להתמכרות. מחקר זה בוחן את מערכת התגמול של המוח כדי לזהות מתגי גנטיים זעירים המשפיעים על עוצמת התחושה התגמולית של האופיואידים. על ידי הבנת מתגים אלה, מדענים מקווים לעצב טיפולים חכמים יותר שמקלים על הכאב או מצמצמים תלות מבלי להשתלט על מעגלי העונג של המוח.
מולקולות קטנות, השפעה גדולה
המוח שלנו מסתמך על מוליך כימי בשם דופמין כדי לאותת הנאה ולמנוע אותנו לשוב אחרי חוויות מתגמלות, מאוכל טעים ועד סמים ממכרים. עוצמתו ומשך האות נשלטים בחלקם על ידי חלבון שנקרא משאבת הדופמין, שפועלת כמו שואב אבק — שואבת דופמין חזרה לתוך התאים העצביים. המחברים התמקדו בשני מקטעים גנטיים קטנטנים, מיקרוRNA-132 ומיקרוRNA-212, שיכולים להנמיך את הייצור של חלבונים ספציפיים. עבודות קודמות קישרו מיקרוRNA אלה לשימוש בקוקאין ולמענה למתח. כאן, הצוות בדק האם הם גם מעצבים את תגובת המוח לתרופות אופיואידיות, ובפרט מורפין.
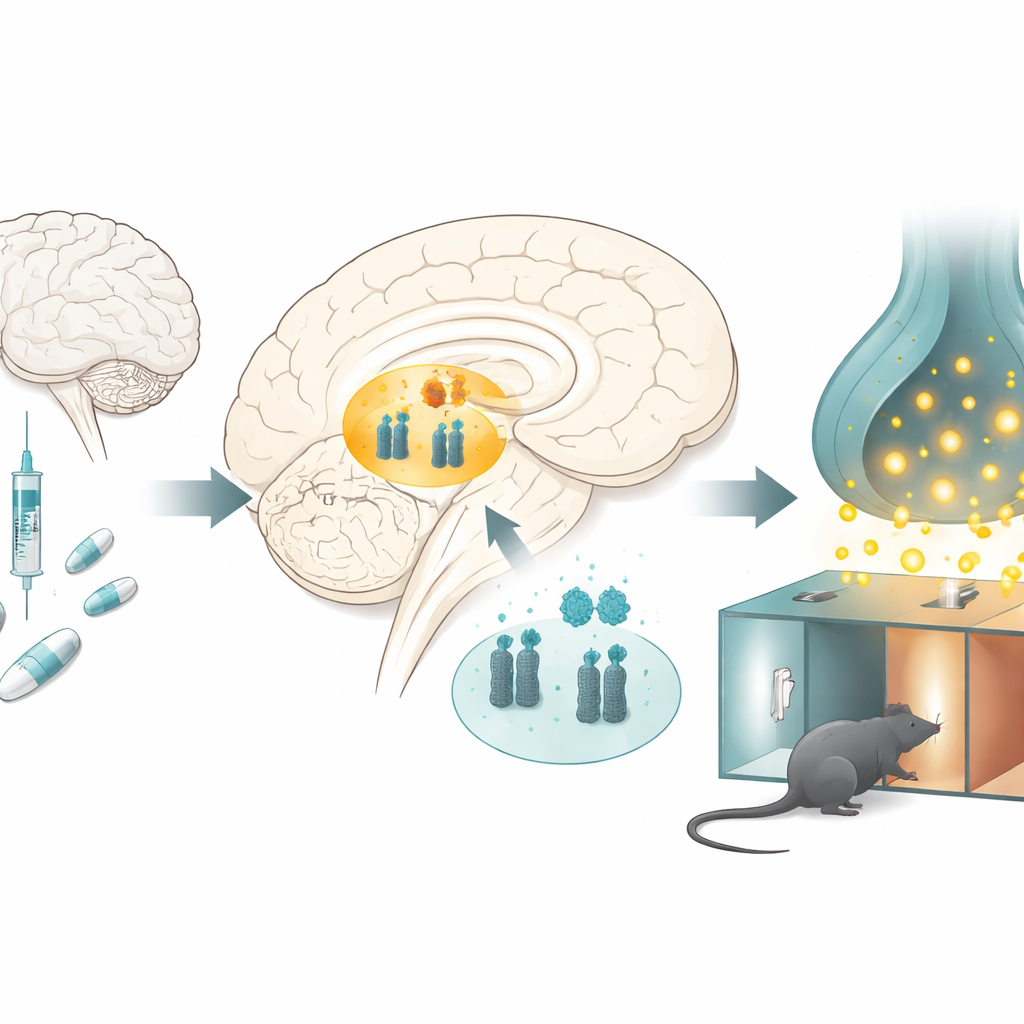
כיצד אופיואידים משנים את מרכז התגמול במוח
החוקרים חקרו חולדות שקיבלו מנות חוזרות של מורפין בבדיקה קלאסית של תגמול סם, שבה החיות לומדות להעדיף חדר המשויך לסם. לאחר מספר ימים, החולדות שטופלו במורפין בילו יותר זמן בחדר המשויך למורפין, מה שמראה שהסם הפך למתגמל. כאשר המדענים בדקו אזור מפתח של התגמול עמוק במוח הנקרא האזור הטגמנטלי הוונטרלי, הם מצאו דפוס בולט: רמות מיקרוRNA-132 ומיקרוRNA-212 ירדו, בעוד שרמות משאבת הדופמין עלו. שינויים דומים הופיעו גם כאשר חולדות קיבלו מורפין בלי משימת רכישת המקום, מה שמרמז כי חשיפה כרונית לסם сама משנה את האיזון המולקולרי הזה.
זיהוי קישור מולקולרי ישיר
כדי לבדוק האם המיקרוRNA האלה אכן שולטים במשאבת הדופמין, הצוות פנה לתאי עצב דמויי־אנוש במעבדה. על ידי הגברה מלאכותית של מיקרוRNA-132 או מיקרוRNA-212 הם ראו ירידה הן במסר הגנטי והן בחלבון של המשאבה. חסימת המיקרוRNA נתנה את ההשפעה ההפוכה. לאחר מכן הם מהנדסים קונסטרוקט של דיווח שבו אנזים מייצר־אור היה מקושר לזנב הרגולטורי של המשאבה. הוספת המיקרוRNA העמימה את אות האור, אך השפעה זו נעלמה כאשר מספר בסיסים מפתח באתר הקשירה עברו מוטציה. יחד, ניסויים אלה הראו שמיקרוRNA-132 ומיקרוRNA-212 נקשרים ישירות למסרי המשאבה ומדכאים את ייצורה.
ממולקולות לרמות דופמין והתנהגות
בהמשך שאלו החוקרים כיצד בקרת מולקולות זו באה לידי ביטוי בתאי מוח חיים. בתאים עצביים בתרבית, העלאת המיקרוRNA הפחיתה את קליטת הדופמין, בעוד שחסימתם שיפרה את ניקיון הדופמין. כאשר הם הגדילו או הקטינו באופן מלאכותי את רמות משאבת הדופמין, השפעת המיקרוRNA עלתה או ירדה בהתאם, מה שאישר שהמשאבה היא הצד השלישי העיקרי. בעכברים חיים, הגברה של מיקרוRNA-132 באזור הטגמנטלי הוונטרלי העלתה את רמות הדופמין שדלגו לאזורים מחוברים, מה שמעיד על פעילות משאבה חלשה יותר. ברמה ההתנהגותית, שימוש בכלים ויראליים לספוח ("ספוג") מיקרוRNA-132 או מיקרוRNA-212 באזור המוח הזה גרם לחולדות לפתח העדפה חזקה יותר למורפין, יחד עם רמות משאבה גבוהות יותר. בניגוד לכך, הזרקה כפויה של מיקרוRNA-132 נוסף לאותו אזור הורידה את רמות המשאבה וטשטשה את העדפת המורפין בזכרים, בנקבות ובחיות מתבגרות, מבלי להשפיע על התנועה או על ההנאה ממערכות טבעיות כמו מי סוכר.
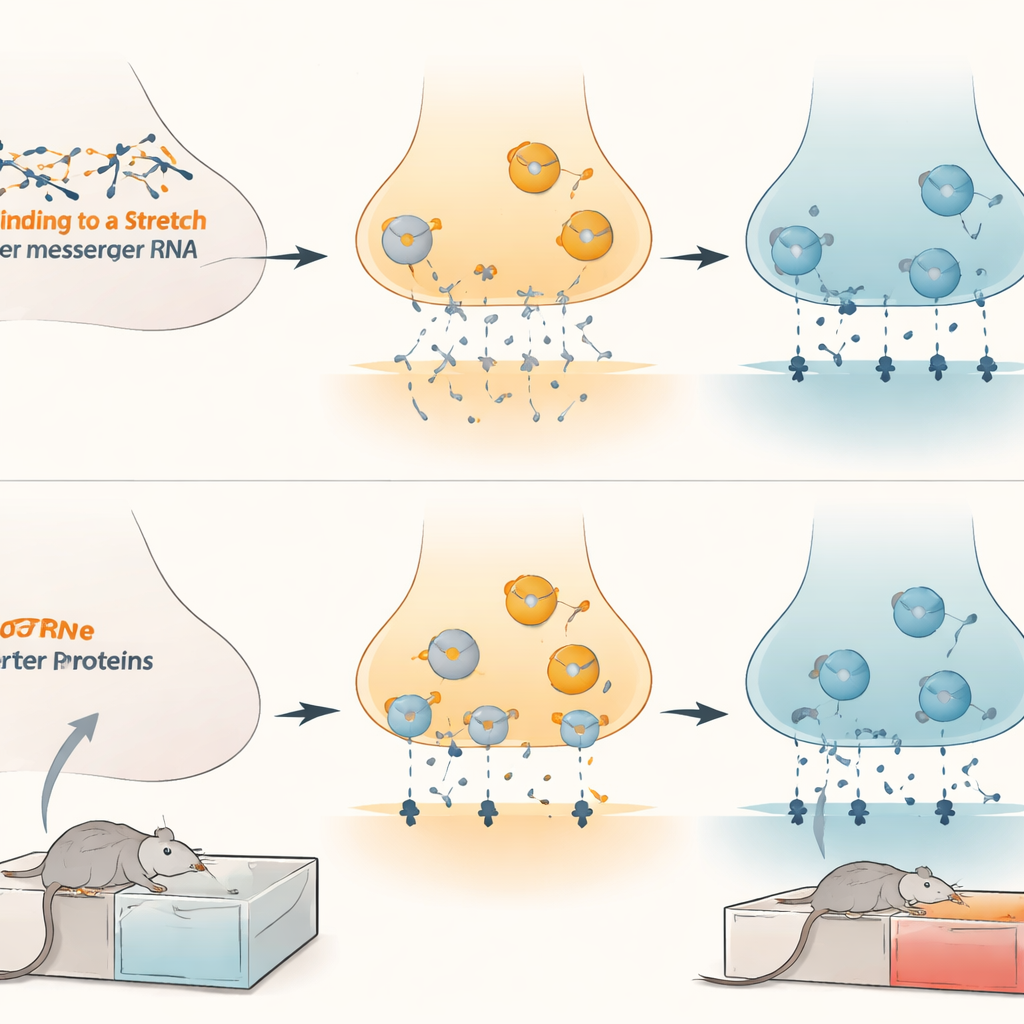
משמעויות לטיפול בהתמכרות לאופיואידים
ממצאים אלה חושפים מערכת בלימה עדינה בתוך מעגלי התגמול של המוח: מיקרוRNA-132 ומיקרוRNA-212 שומרים על משאבת הדופמין במעקב, ועיצובם קובע עד כמה חזק חוויית האופיואידים נתפסת כמתגמלת. מורפין כרוני נראה כמרים את הבלם הזה על ידי הורדת המיקרוRNA, מה שמאפשר לרמות המשאבה לעלות ותורם להמצקת אותות תגמול הקשורים לסם. על ידי שיחזור או חיקוי הפעולה של מיקרוRNA אלה באופן ממוקד באזור הטגמנטלי הוונטרלי, יתכן שניתן להחליש את אחיזתו של תגמול האופיואידים מבלי לנטרל עונג או תנועה באופן רחב. אף שדרוש עוד הרבה עבודה לפני שניתן יהיה לבדוק אסטרטגיות כאלה בבני אדם, המחקר מצביע על נתיב חדש וממוקד לטיפולים עתידיים המתמודדים עם התמכרות ברמת הכפתורים המולקולריים של המוח.
ציטוט: Meng, J., Li, Z., Zhang, Y. et al. MicroRNA-132/212 negatively modulates opioid reward by targeting dopamine transporter in the ventral tegmental area. Transl Psychiatry 16, 152 (2026). https://doi.org/10.1038/s41398-026-03915-9
מילות מפתח: התמכרות לאופיואידים, משאבת דופמין, מיקרוRNA-132, איזור טגמנטלי וונטרלי, תגמול מורפין