Clear Sky Science · he
שינויים m6A בתיווך METTL3 מווסתים את CDKN1A וממתנים פגיעה קוגניטיבית ותמותת נוירונים ברק כרוני של חסר שינה בעכברים
מדוע לילות ללא שינה עלולים לפגוע בזיכרון
אנשים רבים מתייחסים לחוסר שינה כרוני כחלק נורמלי של החיים המודרניים, אך המדע מראה שחוסר שינה עלול לפגוע בעדינות באזורים במוח התומכים בלמידה ובזיכרון. המחקר הזה בעכברים חופר לרמת המולקולות בתוך נוירונים בהיפוקמפוס ומזהה מתג כימי ספציפי — בשם METTL3 — שנראה כמגן על תאי המוח מההשפעות המזיקות של חסר שינה כרוני. הבנת מתג זה עשויה בסופו של דבר להצביע על דרכים חדשות לשמירה על הזיכרון אצל אנשים שאינם יכולים להימנע מאובדן שינה בקלות, כגון עובדים במשמרות, מטפלים וחולי הפרעות שינה.
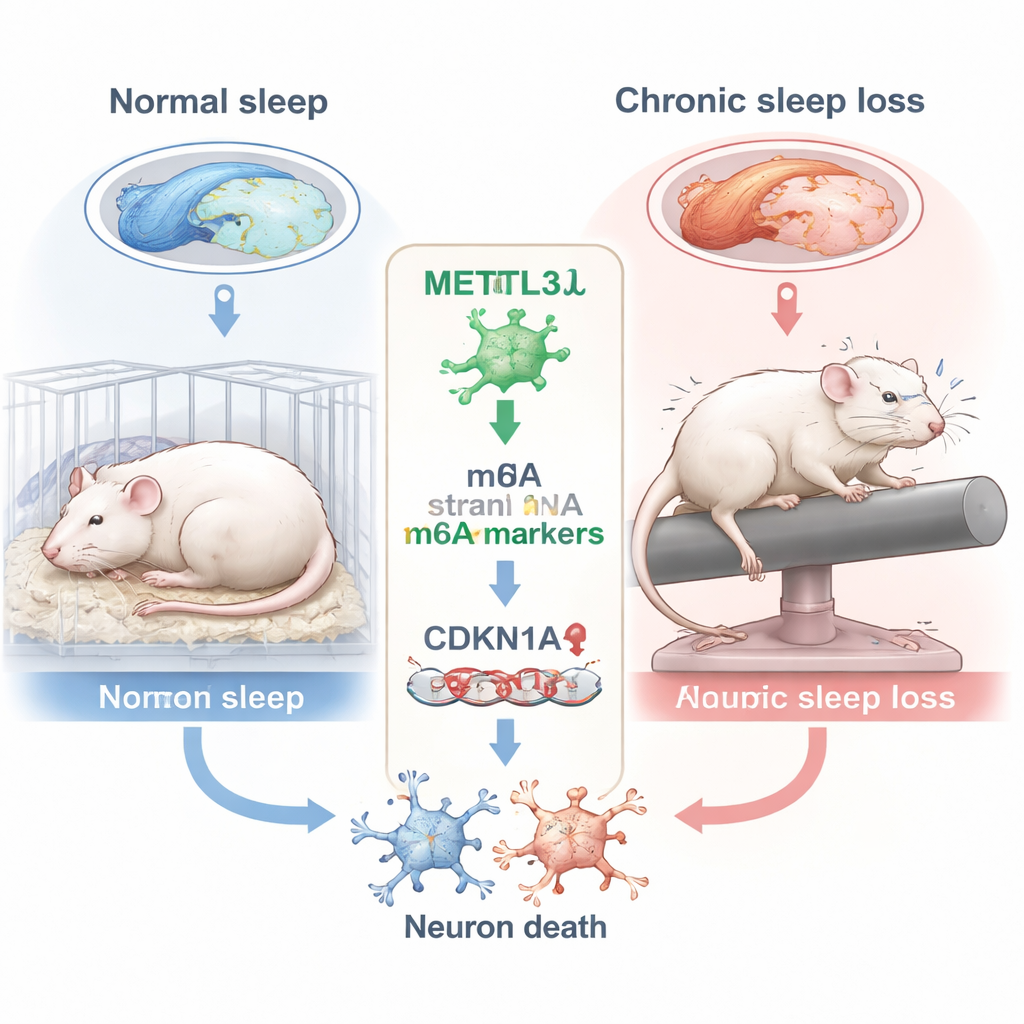
כיצד חוסר שינה ממושך מפגע במרכז הזיכרון
החוקרים התמקדו בהיפוקמפוס, אזור מוח בצורת פרסה החיוני ליצירת זיכרונות חדשים. בתוך ההיפוקמפוס הם התמקדו בתת-אזור שנקרא CA3, המסייע לקידוד ולשליפת מידע מרחבי — מיומנויות שנבדקות במטלות כמו מציאת פלטפורמה מוסתרת במים. העכברים נשמרו ערים 10 שעות ביום במשך שישה שבועות באמצעות מוט מסתובב עדין שניעץ אותם משינה שוב ושוב. במבחן המוכר של מבוך המים של מוריס, עכברים חסרי שינה נטו לקחת מסלולים פחות ישירים, חצו את מיקום הפלטפורמה הקודם פחות פעמים ובילו פחות זמן ברביע המטרה — סימנים לפגיעה בזיכרון המרחבי לעומת בעלי חיים שנמנעו מחוסר שינה.
סימון כימי על ה-RNA שנעלם
כדי להבין מה קורה בתוך נוירוני CA3, הצוות ניתח סימון כימי על RNA שנקרא m6A, אחד הסימונים הפנימיים הנפוצים על RNA שליח. סימונים אלה מסייעים לווסת כמה זמן מולקולות ה-RNA שורדות וכמה יעילה השימוש בהן לייצור חלבונים. אנזים מרכזי שמוסיף סימני m6A הוא METTL3. באמצעות ריצוף m6A בקנה מידה רחב וניתוח ביטוי גנים, המדענים מצאו שחריגות שינה כרונית הפחיתו משמעותית את METTL3 באזור CA3. הירידה זו אוששה הן ברמת ה-RNA והן ברמת החלבון. דפוסי הגנים המושפעים הצביעו על שיבושים בבקרת מחזור התא ותגובת סטרס, מרמזים שחוסר שינה עלול לדחוף את הנוירונים למצב לא בריא.
מהשינוי המולקולרי למות הנוירון
כדי לראות כיצד ירידה ב-METTL3 עשויה להשפיע ישירות על נוירונים, החוקרים פנו לתאים היפוקמפאליים של עכברים שגדלו במנות. כאשר השתמשו ב-RNA קטנים מתערבים כדי להשתיק את METTL3, התאים הפכו פגיעים הרבה יותר לטיפול מזיק ברפאמיצין, תרופה שמייצרת עומס על הנוירונים. בתאים חסרי METTL3 נצפו רמות גבוהות יותר של חלבונים אופייניים ל"התאבדות תאית" כמו Bax ו-caspase-3 המפורק, וכמות גדולה יותר של תאים סומנה כאפופטוטיים בעזרת ציטומטריית זרימה. ניתוחים מעמיקים של RNA הצביעו על גן אחד מרכזי, CDKN1A (המקודד לחלבון p21), כשחקן מכריע: כאשר METTL3 הושתק, רמות CDKN1A עלו בצורה חדה.
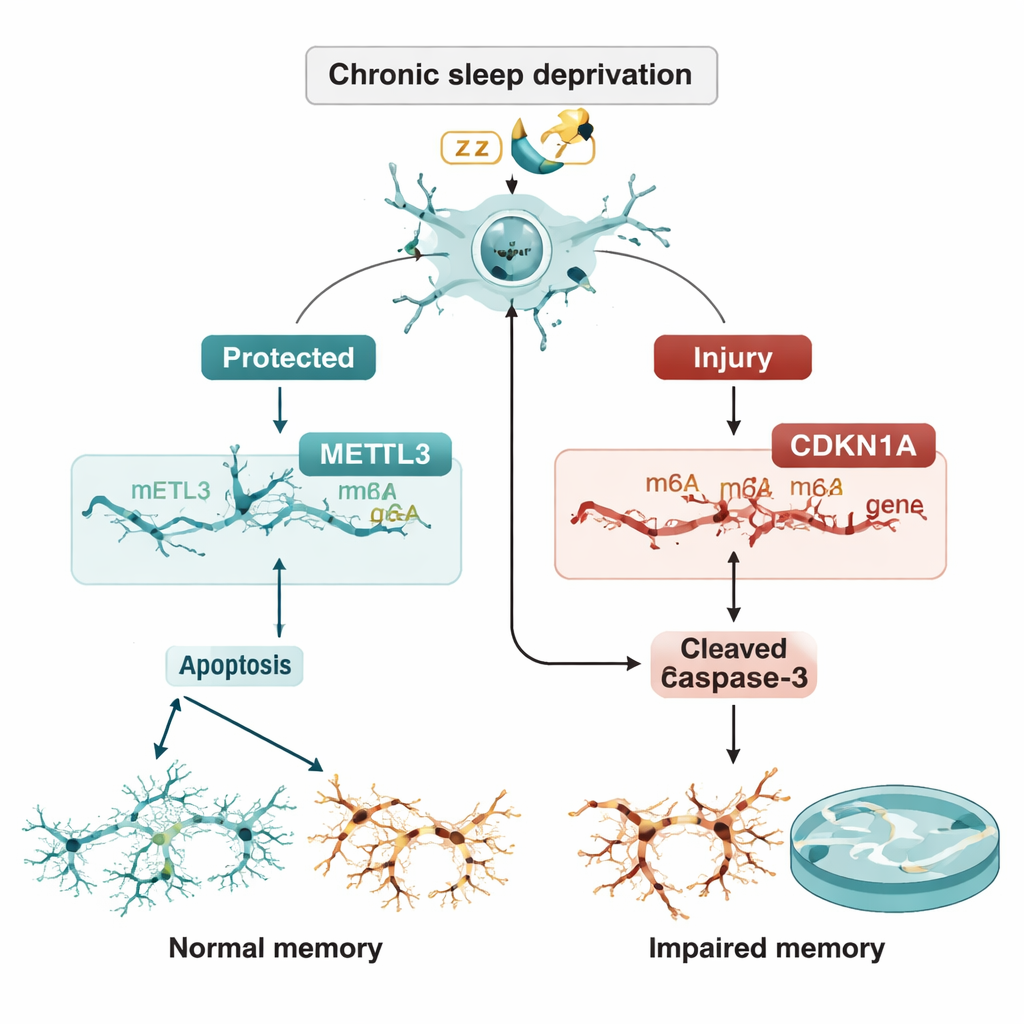
איזון שברירי בין הגנה להרס עצמי
הצוות שאל האם METTL3 שולט ב-CDKN1A באמצעות סימון m6A. הם הראו שהפחתת METTL3 הורידה את סימני ה-m6A על RNA של CDKN1A והפכה את ה-RNA הזה ליציב יותר, כך שרמותיו הצטברו במקום להישבר. עלייה ב-CDKN1A, בתורה, דחפה את הנוירונים לעבר אפופטוזה. באופן קריטי, כאשר גם CDKN1A הושתק, מוות התאים המוסף שנגרם מאובדן METTL3 הועבר באופן ניכר. בעכברים חיים, הזרקת METTL3 נוספת ישירות לאזור CA3 באמצעות וקטור ויראלי הפחיתה את רמות CDKN1A, הורידה את השפע של חלבוני אפופטוזה, שמרה על מבנה הנוירונים בצביעות רקמה ושיפרה ביצועים במבוך המים למרות המשך חוסר השינה.
מה זה אומר לאנשים שאינם ישנים מספיק
פשוטו כמשמעו, חסר שינה כרוני נראה כמכה על אנזים מגן, METTL3, במעגל זיכרון קריטי במוח. כשה-METTL3 יורד, הוא כבר אינו מסמן כראוי כמה מולקולות RNA, במיוחד זו המקודדת ל-CDKN1A. ה-RNA הזה מצטבר, ודוחף נוירונים לעבר מוות מתוכנת ותורם לבעיות זיכרון. על ידי שיקום METTL3, החוקרים יכלו להנמיך את CDKN1A, להפחית אובדן נוירונים ולהציל את הזיכרון בעכברים חסרי שינה. אמנם עבודה זו עדיין נמצאת בשלב בעלי החיים, היא מזהה את מסלול METTL3–CDKN1A כמטרה מבטיחה לתרופות עתידיות שמטרתן להגן על המוח מהנזקים הקוגניטיביים של חסר שינה כרוני.
ציטוט: Xing, F., Shi, XS., Gu, HW. et al. METTL3-mediated m6A modification regulates CDKN1A to attenuate chronic sleep deprivation-induced cognitive impairment and neuronal apoptosis in rats. Transl Psychiatry 16, 96 (2026). https://doi.org/10.1038/s41398-026-03855-4
מילות מפתח: חסר שינה כרוני, היפוקמפוס, מתילציה של RNA, אפופטוזה של נוירונים, פגיעה בזיכרון