Clear Sky Science · he
עיכוב ייצור האנרגיה המיטוכונדריאלי על ידי פפטיד קופרדוקסין חיידקי פוטוסינתטי מעכב גדילת גידולים
להפוך חיידקים ללוחמי סרטן
תאי סרטן רעבים לאנרגיה. הם נשענים על "תחנות כוח" פנימיות זעירות שנקראות מיטוכונדריות כדי להפיק את האנרגיה הדרושה להם לגדילה, פיזור ולעמידות בטיפול. המחקר הזה בוחן בעל־ברית בלתי צפוי במאבק בסרטן: מקטע קצר של חלבון שמקורו בחיידקים פוטוסינתטיים. החוקרים מראים כי הפפטיד המותאם הזה מסוגל להיכנס לתאי סרטן, לכבות את אספקת האנרגיה שלהם במקור שלה, ולהפוך את טיפול הקרינה ליעיל בהרבה — תוך השארת תאים רגילים ברובם ללא פגיעה משמעותית.
פפטיד קטן עם משימה גדולה
הצוות התחיל מגילוי קודם שמחלבון חיידקי בשם אזורין (azurin) יכול להאט גדילת גידולים על ידי פעולה על החלבון מדכאי הגידול המפורסם p53. לאחר מכן הם חיפשו חיידקים החיים בסביבת גידולים אנושיים, והתמקדו במיקרובים פוטוסינתטיים המשתמשים באור לייצור אנרגיה. חיידקים אלה נושאים משפחה קשורה של חלבונים שנקראת קופרדוקסינים. על ידי השוואת המבנים וההיסטוריה האבולוציונית שלהם, החוקרים זיהו קופרדוקסין ספציפי, אוראצ'נין B, וגזרו ממנו קטע קצר של 28 חומצות אמינו שכינו aurB. מקטע זה מסיס במים, יכול לעבור דרך ממברנות התא, ויש לו צורה שהרמזה שהוא עשוי ליצור אינטראקציה עם מכונות מרכזיות להפקת אנרגיה בתוך התאים.
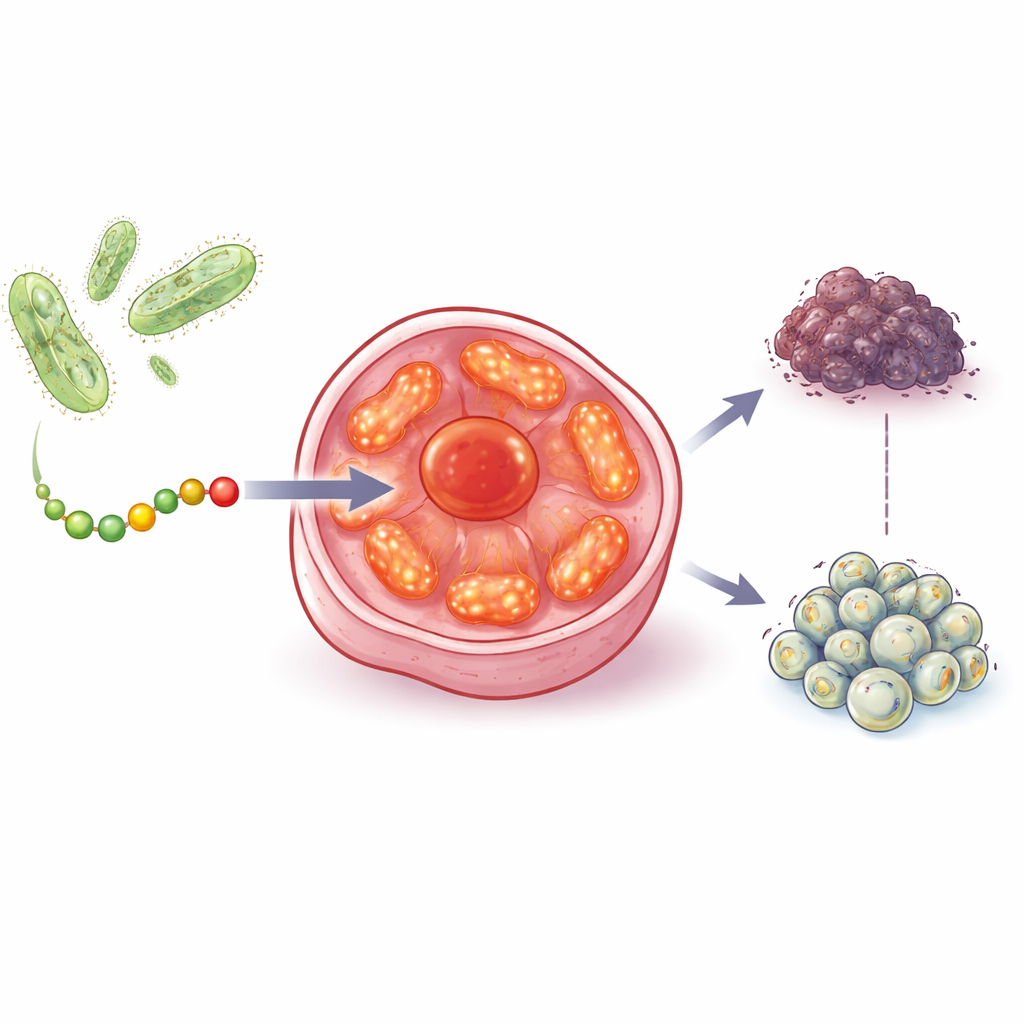
למצוא ולהכות את תחנות הכוח של הסרטן
במבחנים מעבדתיים, aurB הקטין את הישרדותן של שורות תאי סרטן בשד, בערמונית, במעי הגס ובשחלות, אפילו כאשר תאים אלה היו חסרי p53 פעיל או קולטנים הורמונליים שרבים מהתרופות הנוכחיות דורשות. חשוב לציין של־aurB היו השפעות חלשות בהרבה על תאי ערמונית, לב ושריר תקינים, אף על פי שתאים בריאים אלה עשירים במיטוכונדריות. ניסויים בדימות הראו כי aurB נכנס באופן מועדף לתאי סרטן ואז ריכז עצמו בתוך המיטוכונדריות שלהם. מיקרוסקופיה אלקטרונית, שבה השתמשו ב־aurB קשור למוטות זהב זעירות כ"יד חזותית", אישרה שהפפטיד אכן הצטבר בתוך האברונים הללו.
לחתוך את אספקת האנרגיה
ברגע שנכנס למיטוכונדריות, aurB התקשר לרכיב מסוים של סינתאזת ה‑ATP — הטורבינה המולקולרית שמייצרת ATP, המטבע האנרגטי המרכזי של התא. ניסויי משיכה ביוכימיים ומסות ספקטרומטריה זיהו שותף זה כ־ATP5C, חלק מהליבה המרכזית של האנזים. מדידות של תהודה פלזמונית משטח הראו כי aurB קשור ל‑ATP5C בעוצמה מתונה ובשחרור איטי, תואם לאינטראקציה יציבה. במבדקים פונקציונליים התברר מה עושה הקשירה הזו: aurB הוריד בחדות את רמות ה‑ATP המיטוכונדריאלי בתאי סרטן של הערמונית, האט את קצב צריכת החמצן שלהם, וחסם גם את הנשימה וגם את מסלול הגליקוליזה המחליף. עם התמוטטות ייצור האנרגיה, תאי הסרטן הציגו מאפיינים של מוות מתוכנת מונע על‑ידי קספאז‑3, אנזים מבצע מרכזי.
חסימת גידולים והגברה של קרינה
החוקרים בחנו לאחר מכן את aurB במודלים של עכברים לסרטן ערמונית אגרסיבי. בחיות ששאבו גידולים אנושיים של הערמונית מתחת לעור, הזרקות קבועות של aurB הקטינו את גדילת הגידולים בכ־שני שלישים, בדומה או טוב יותר מתרופת הכימותרפיה פאציטקסל, אך ללא ירידה במשקל או מצוקה נראית לעין. דגימות גידולים מהעכברים המטופלים הכילו תאים מחלקים פחות ותאים מתים רבים יותר. במודל שני המדמה גרורות לעצם — אתר שכיח וממאר של התפשטות סרטן הערמונית — aurB לבדו האט את התפשטות הגידול בעצם הרגל והקטין את מספר הגרורות בריאות. יחד עם מנה מתונה של קרינה, לעומת זאת, ההשפעה הייתה דרמטית: הגידולים בגפה המטופלת כמעט נכחדו, וגרורות ריאה ירדו ביותר מ‑90 אחוזים בהשוואה לביקורות.
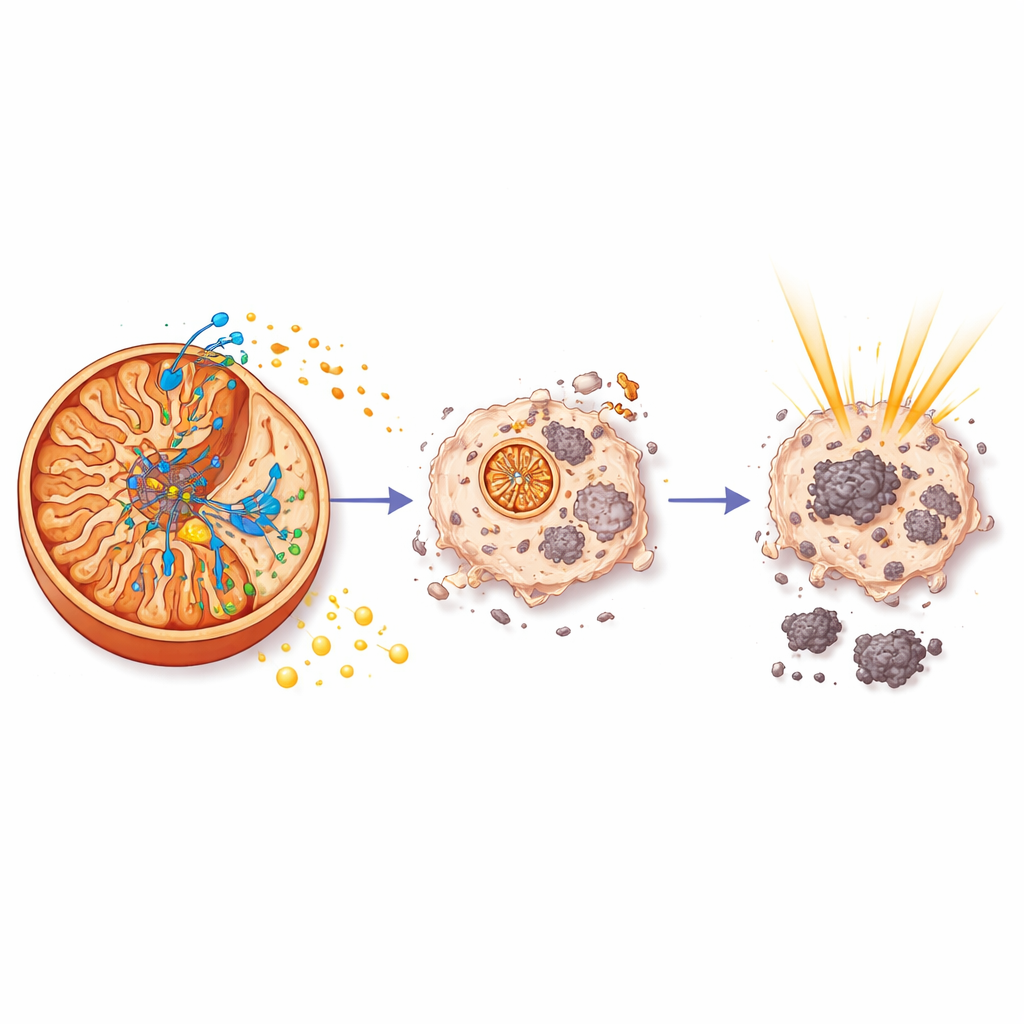
מדוע אנרגיה חשובה לקרינה
כדי להבין מדוע aurB מייעל את יעילות הקרינה, הצוות בחן פעילות גנים בגידולים של העכברים המטופלים. הם מצאו ש‑aurB, אך לא הקרינה לבדה, דיכא רשת גנים הנשלטת על‑ידי HIF‑1, רגולטור מרכזי המסייע לתאי סרטן להסתגל לחוסר חמצן ומזין עמידות לטיפול. בתנאי מחסור באנרגיה שנוצרו על‑ידי aurB, מסלולי הצמיחה וההישרדות המרכזיים המונעים על‑ידי PI3K ו‑c‑Myc נחלשו, וגם המכונה הגליקוליטית שמאפשרת לגידולים לשגשג בסביבות קשות הושתקה. במהותו, על‑ידי סחרור ייצור ה‑ATP ישירות בטורבינת המיטוכונדריה, aurB דחף את תאי הסרטן למשבר אנרגטי שהשאיר אותם פגיעים בהרבה לנזקי הקרינה.
מחלקה חדשה של חוסמי אנרגיה מדויקים
עבודה זו מציגה אסטרטגיה חדשה לטיפול בסרטן: עיצוב פפטידים קטנים המושפעים מחיידקים הפונים למערכות אנרגיה מיטוכונדריאליות ששונו בגידולים. AurB, שמקורו בחלבון חיידקי פוטוסינתטי, מטרתו באופן סלקטיבי רכיב של סינתאזת ה‑ATP שלרוב פעיל יתר על המידה בסרטנים כגון ערמונית, שד, שחלות ומוח. על‑ידי הרעבת תאי הסרטן ישירות מאנרגיה והחלשת ההגנות שלהם, במיוחד מול קרינה, פפטידים מסוג זה עשויים להשלים טיפולים קיימים ולספק אפשרויות במקומות שבהם גישות מבוססות חיסון נכשלים. למרות שעבודת פיתוח מרובה נדרשת לפני שהרעיון הזה יגיע לקליניקה, המחקר מצביע שפרוטאינים עתיקים של אנרגיית חיידקים ניתנים להפיכה לכלי אנטי‑סרטני מודרני וממוקד מאוד.
ציטוט: Naffouje, S.A., Tran, D.B., Rademacher, D.J. et al. Suppression of mitochondrial energy production by a photosynthetic bacterial cupredoxin peptide inhibits tumor growth. Sig Transduct Target Ther 11, 124 (2026). https://doi.org/10.1038/s41392-026-02703-7
מילות מפתח: סינתאזת ATP מיטוכונדריאלית, מטבוליזם של סרטן, פפטידים תרופתיים, סרטן הערמונית, רגישות לקרינה