Clear Sky Science · he
אותות הגואנוזין מונופוספט מחזורי‑פרוטאין קינאז G מפחיתים קלציפיקציה של המסתם האאורטלי דרך אוטופגיה מתווכת ULK1
למה ה"חלודה" במסתם הלב חשובה
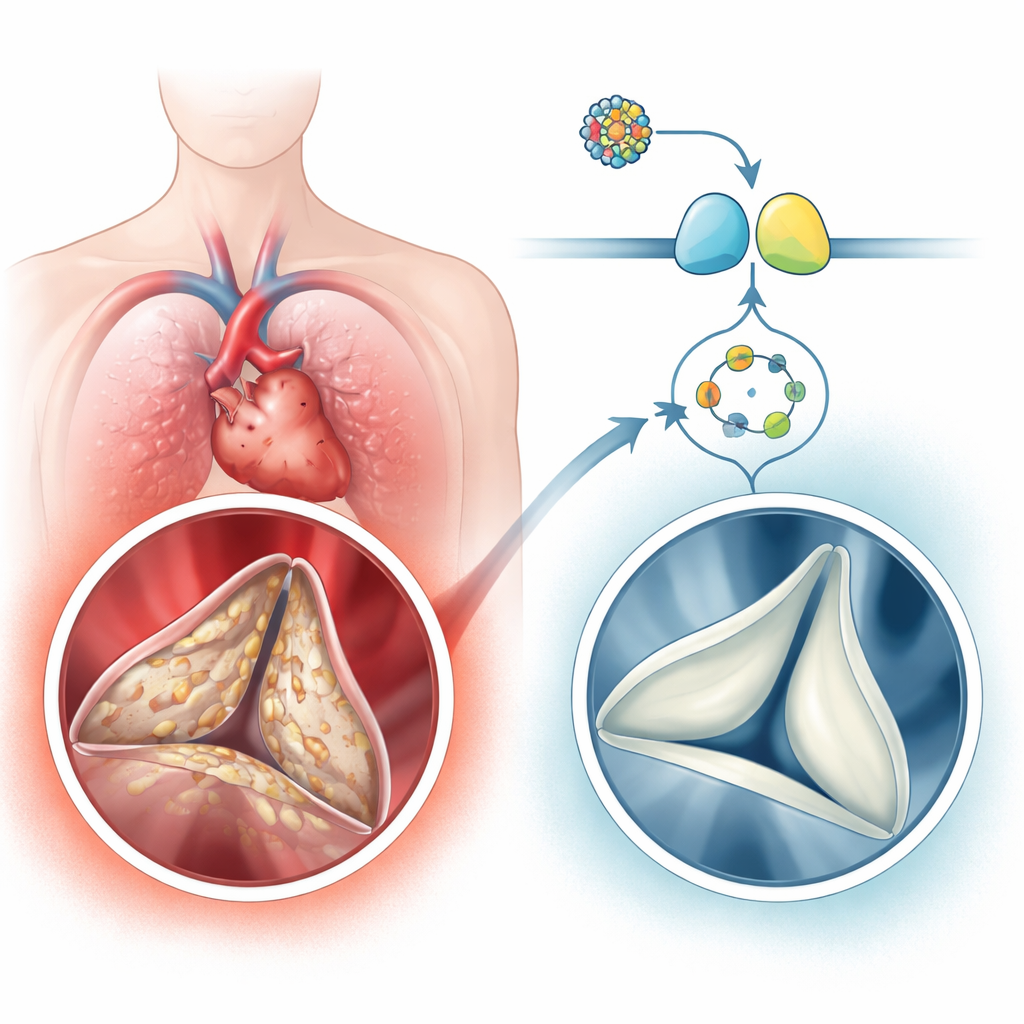
ככל שאנשים מתבגרים, המסתם האאורטלי — שער היציאה הראשי של הלב — עלול להתקשח ולאסוף משקעים של סידן, מצב הנקרא מחלת המסתם האאורטלי הקלציפית. ה"התקשחות" הזו מאלצת את הלב לשאוב בעוצמה רבה יותר ועלולה לגרום לכאבים בחזה, לאובדן הכרה, לאי‑ספיקת לב או לצורך בניתוח להחלפת המסתם. כיום אין תרופה שמאטה את התהליך הזה באופן מהימן; הרופאים יכולים רק להמתין עד שהמסתם ייפגע קשה ואז לנתח. המחקר הזה בוחן מסלול תאי פנימי שנראה כמגן מפני קלציפיקציה, ובודק תרופת אי‑ספיקת לב מודרנית כאמצעי פוטנציאלי להחזיר את ההגנה הזו לפעולה.
בעיה לבבית שכיחה אך שלא זוכה להתייחסות מספקת
מחלת המסתם האאורטלי הקלציפית שכיחה באופן מפתיע במבוגרים מבוגרים, ומשפיעה על אחוזים בודדים בקרב בני 65 ומעלה ועד לאחד מכל עשרה בני 75 ומעלה. המחלה אינה רק "בלאי" פסיבי. במקום זאת, תאי החיבור הרכים במסתם, המכונים תאי הביניים של המסתם (valvular interstitial cells), משתנים למצב של ריפוי פצעים ולמצב דמוי עצם. הם מייצרים קולגן עודף ואז משקיעים סידן, מה שהופך את עלי המסתם הגמישים לפתקים קשים, דמויי סלע. החוקרים ניתחו רקמות מסתם אנושיות ומאגרי נתונים של הבעה גנטית גדולים ומצאו שהמסלול הסיגנלי סביב מולקולה קטנה בשם cGMP ובאנזים שותף שלה פרוטאין קינאז G (PKG) מדוכא בהקביעות במסתמים קלציפיים, בעוד שגנים וחלבונים המקושרים ליצירת עצם מגבירים את פעילותם. אנשים עם קלציפיקציה חמורה של המסתם גם הראו רמות נמוכות יותר של cGMP בדם, שנכחו בקשר לחומרת ההיצרות והחסימה של המסתם שלהם.
אות מגן שנעלם
כדי לבחון סיבה ותוצאה, הצוות השתמש בעכברים ובתאי מסתם אנושיים בתרבית. עכברים שהונדסו לייצר פחות PKG מפתחים עלי מסתם עבים ומקלציפיים יותר לאחר פגיעה מבוקרת במסתם האאורטלי, ובמסתמיהם נרשמו רמות גבוהות יותר של חלבון שבקרת יצירת עצם. בתאי מסתם אנושיים שגדלו בצלחת בתנאים המעודדים הצטברות סידן, דיכוי PKG בכלים גנטיים האיץ את השינוי הדמוי‑עצם. תוצאות אלה מרמזות שהאות cGMP‑PKG פועל בדרך כלל כבלם על רה‑תכנות התאי השמור על המסתם — וכאשר הבלם הזה נחלש, הקלציפיקציה מואצת.
ממצאים על שימוש חוזר בתרופת אי‑ספיקת לב
החוקרים שאלו האם הגברה של המסלול הזה יכולה להאט או להחזיר את הקלציפיקציה. הם בחנו שלוש תרופות שמעלות cGMP בדרכים שונות, כולל וריציגואט, תרופה מאושרת לחלק מחולי אי‑ספיקת לב. בתאי מסתם אנושיים כל שלוש התרופות הפחיתו משקעים של סידן וסמנים של שינוי דמוי‑עצם, כאשר לוריציגואט היה האפקט החזק ביותר. וריציגואט גם הקטין את הקלציפיקציה בפרוטזות קטנות של רקמות מסתם אנושיות שנשמרו בחי מחוץ לגוף. בשני דגמי עכבר — אחד הנגרם מתזונה גבוהה כולסטרול ואחד מפגיעה מכנית במסתם — טיפול יומי בוריציגואט הוביל לעלי מסתם דקים ופחות קלציפיים וזרימת דם טובה יותר דרך המסתם, מבלי להחליש את עוצמת השאיבה של הלב. עם זאת, כאשר PKG הוקטן באופן גנטי, וריציגואט איבד במידה רבה את היתרונות שלו, מה שמעיד ש‑PKG הוא השחקן המרכזי במטה המסלול.
ניקיון תאי — מסתמים בריאים יותר
בהעמקה נוספת, הצוות מצא שוריציגואט ו‑PKG הגנו על תחנות הכוח הקטנות של התאים — המיטוכונדריה. בתנאי קלציפיקציה, תאים הצטברו ברדיקלים חופשיים מזיקים, איבדו פוטנציאל ממברנת מיטוכונדריה וייצרו פחות אנרגיה. וריציגואט שיקם את ביצועי המיטוכונדריה והפחית את הלחץ החמצוני. מיפוי רחב של חלבונים ותיוגי זרחון פנה אותם לעבר האוטופגיה — מערכת הניקיון והמחזור התוך‑תאית. במסתמים אנושיים קלציפיים, דימות מיקרוסקופי וסמנים חלבוניים הראו הקטנה ביצירה ובפעילות של אוטופאגוזומים, ה"שקיות האשפה" של האוטופגיה. בניתוח תאי‑יחיד, מספר תת‑סוגים של תאי מסתם ממסתמים חולים הציגו דיכוי רחב של תכניות הקשורות לאוטופגיה. בתאים בתרבית, חסימת האוטופגיה ביטלה את השפעת ההגנה של הפעלת PKG, מה שמרמז ש‑PKG פועל במידה רבה על ידי החייאת מערכת הניקיון הזו.
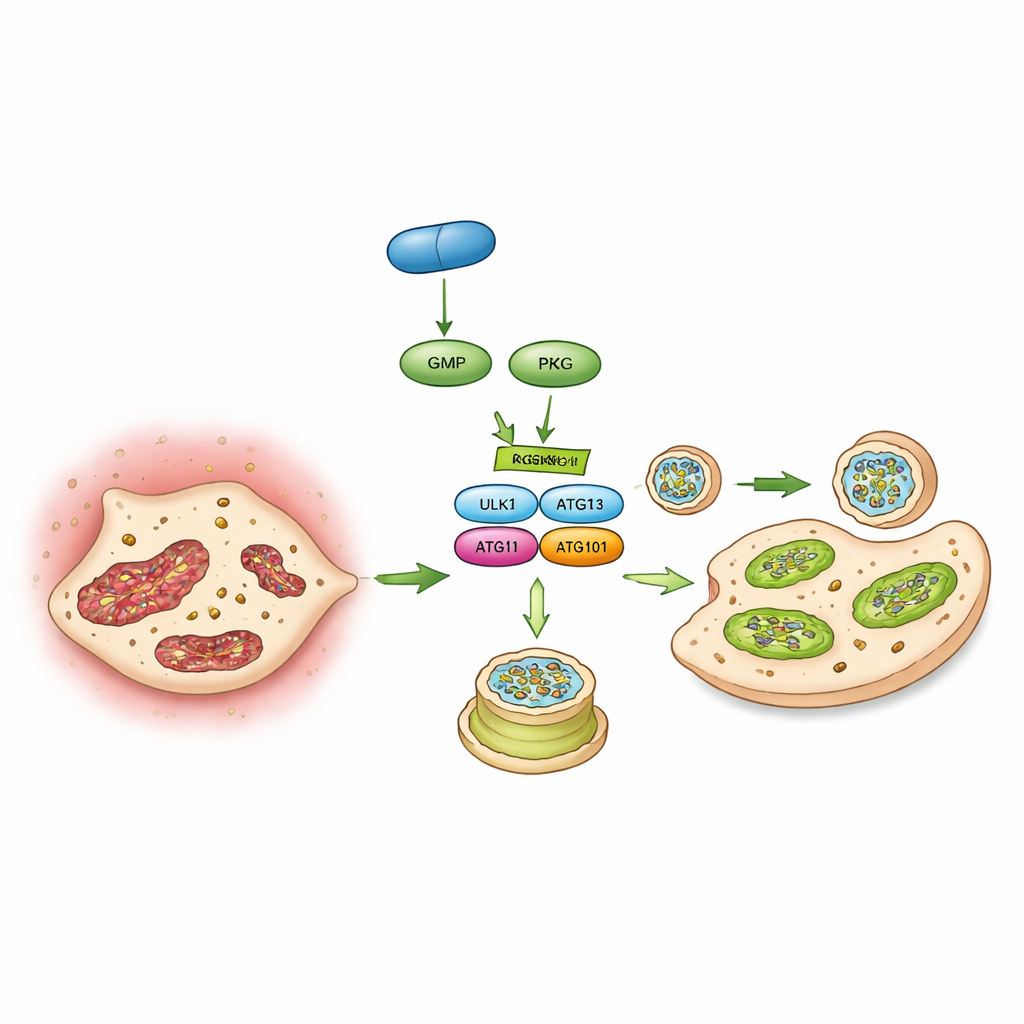
הפיכת מתג מולקולרי
לבסוף, המחברים זיהו מתג מולקולרי ספציפי שמקשר את PKG לאוטופגיה: חלבון בשם ULK1 שמניע את תחילת יצירת האוטופאגוזומים. באמצעות פוספופרוטאומיקה, מחקרי אינטראקציה ומבחני קינאז בצינור מבחנה, הם הראו ש‑PKG מצמיד ישירות קבוצת זרחן ל‑ULK1 באתר מסוים (חומצת אמינו בשם סרין 556). כאשר אתר זה הושנה כך שלא יכול עוד לעבור זרחון, PKG לא יכל עוד להגביר את האוטופגיה או לחסום קלציפיקציה בתאי המסתם. בעכברים, הבעה מודרכת של מוטנט ULK1 שאינו מגיב בתאי המסתם גם נטרלה את יכולת ההגנה של וריציגואט. יחד, הממצאים מסמנים שרשרת אירועים: וריציגואט ממריץ cGMP, שמפעיל PKG, שמדלג על מתג ULK1, שמחייה את האוטופגיה, ששומרת על המיטוכונדריה ומונעת מתאי המסתם להפוך לתאים מייצרי עצם.
ממה זה יכול להידרש לחולים
עבודה זו מציבה את הציר cGMP–PKG–ULK1–אוטופגיה כמערכת הגנה טבעית נגד "החלדה" של המסתם האאורטלי. במחלת המסתם הקלציפית, ההגנה הזו מוחלשת, מה שמאפשר לתאים לצבור נזק ולהסתובב לעבר זהות דמוי‑עצם. על‑ידי שיקום האות בצורה פרמקולוגית עם תרופה שכבר בשימוש במרפאות אי‑ספיקת לב, החוקרים האטו את הקלציפיקציה בכמה מודלים ניסיוניים. אף כי יידרשו ניסויים קליניים בבני אדם עם מחלת מסתמים, המאמר מציע רעיון ברור ובדוק: הגברה מדודה של מסלול הניקיון התאי הזה עשויה יום אחד לעכב או להפחית את הצורך בניתוחי החלפת מסתם במבוגרים בסיכון להיצרות אאורתלית.
ציטוט: Wang, Y., Xu, F., Song, C. et al. Cyclic guanosine monophosphate-protein kinase G signaling attenuates aortic valve calcification through ULK1-mediated autophagy. Sig Transduct Target Ther 11, 90 (2026). https://doi.org/10.1038/s41392-026-02624-5
מילות מפתח: מחלת מסתם אאורטלי קלציפית, אותות cGMP‑PKG, וריציגואט, אוטופגיה, קלציפיקציה של מסתמי הלב