Clear Sky Science · he
יעילות והשפעה אימונומודולטורית של תאי CAR-T מצופים IL-7/XCL1 הספציפיים ל-Claudin18.2 בסרטן דרכי העיכול: ניתוח פרהקליני וקליני
להפנות את המערכת החיסונית נגד סרטן דרכי העיכול
סרטן הקיבה והלבלב הם בין הגידולים הקטלניים ביותר, בחלקם משום שהם לעתים קרובות עמידים בפני ניתוח, כימותרפיה וקרינה. המחקר הזה בוחן דרך חדשה להילחם במחלות אלה על ידי חיזוק תאי החיסון של הגוף כך שיוכלו להיכנס לגידולים מוצקים, לשרוד שם ולקרוא להגנה נוספת. בעיצוב מחדש של תאי T לוחמים לשחרר אותות חיסוניים מועילים, החוקרים שואפים לא רק לתקוף ישירות את הגידולים אלא גם להעיר את שאר המערכת החיסונית בתוך הסביבה העוינת של הגידול.
למה גידולים מוצקים קשים לטיפול
טיפולים תאים מודרניים בשם CAR-T הראו תוצאות דרמטיות בסרטן הדם, וריפאו חלק מהחולים שלא נותרו להם חלופות. אבל גידולים מוצקים כמו אלה בדרכי העיכול מציבים אתגרים נוספים. התאים שלהם משתנים ממקום למקום, פנים הגידול מוצף במחסור בחומרים מזינים ובחמצן, ותערובת של תאים וסיגנלים מדכאים מפחיתה את היעילות של התקפות חיסוניות. דורות מוקדמים של תאי CAR-T יכלו לזהות מולקולות ממוקדות על תאי סרטן דרכי העיכול, אך לעתים נכשלו להתרחב, להישאר פעילים ולתפקד בסביבה הקשה הזו, מה שמנע השפעה משמעותית במציאות הקלינית.
עיצוב חכם יותר לתאי T מהונדסים
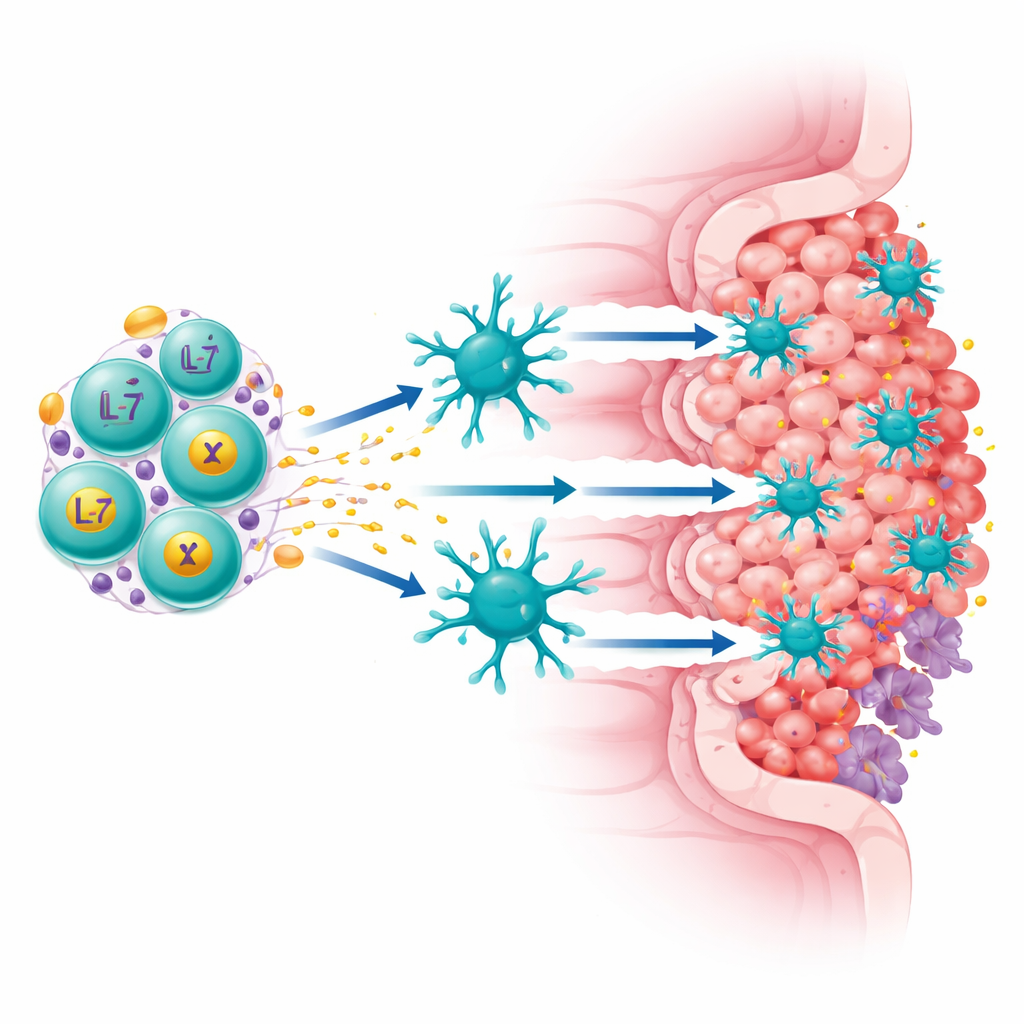
הצוות התמקד בחלבון הנקרא Claudin18.2, הנמצא ברמות גבוהות על תאי סרטן קיבה ולבלב רבים אך נפוץ במידה מועטה ברקמות תקינות. הם בנו תא CAR-T מדור "רביעי" שמבצע שתי משימות בו זמנית: הוא מזהה את Claudin18.2 על תאי הגידול ומפריש ללא הרף שני גורמי חיסון מחזקים, IL-7 ו-XCL1. IL-7 מסייע לתאי T לשרוד ולשמר מצב דמוי-גזע ארוך-טווח, בעוד XCL1 פועל כמקשר שמושך סוג נדיר אך חזק של תאים חיסוניים הנקראים cDC1, אשר מצטיינים בהפעלת תאי קילר. תאים משודרגים אלה, המכונים ExCAR-T או RD07, מתוכננים לא רק להרוג את מה שהם רואים אלא גם לעצב מחדש את הנוף החיסוני של הגידול.
שליטה עוצמתית בגידול במודלים פרהקליניים
במודלים של עכבר לסרטני דרכי העיכול, תאי ExCAR-T התעלו על תאי CAR-T קונבנציונליים שחסרו IL-7 ו-XCL1. במעבדה, התאים המהונדסים הרגו תאי סרטן בקצב גבוה יותר והכילו יותר תאי T בעלי זיכרון ארוך-טווח. בחיות שנשאו גידולים חיוביים ל-Claudin18.2, טיפול ב-ExCAR-T הקטין את הגידולים באופן עמוק יותר והאריך את ההישרדות לעומת CAR-T סטנדרטיים. התאים המוגברים התרבו טוב יותר בדם ויזמו פעילות חיסונית רחבה יותר, כולל אותות שמגייסים תאים חיסוניים נוספים תוך הפחתה של גורמים הקשורים להתפשטות הגידול. באופן בולט, עכברים שנרפאו בעזרת ExCAR-T דחו מבחן חוזר עם תאי סרטן שאיבדו את היעד Claudin18.2, מה שמעיד כי הטיפול הצית זיכרון חיסוני עמיד על-רוב הגידול במקום תגובה צרה המכוונת ליעד יחיד.
תוצאות ראשוניות מניסוי קליני בחולים
בעידוד מהנתונים הללו, החוקרים יזמו ניסוי ראשון-בני-אדם של RD07 ב-12 אנשים עם סרטן קיבה מתקדם, גידול בחיבור הוושט-קיבה, או סרטן לבלב שכשלו בטיפולים סטנדרטיים. תופעות הלוואי היו בדרך כלל ניתנות לניהול: רוב הבעיות החמורות נבעו מירידות בספירת הדם בעקבות הכימותרפיה שלפני ההשפעה, ורק תגובות קלות של שחרור ציטוקינים נצפו; לא תועדו רעילות מוחית חמורה. מבין 10 חולים שניתן להעריך, ל-7 נצפתה הקטנה מדידה של הגידול ו-2 השיגו תגובות חלקיות. חולים שלגידוליהם היו רמות בינוניות עד גבוהות של Claudin18.2 עשו במיוחד טוב, כאשר כל חולה בקבוצה זו חווה לפחות יציבות במחלה וכמה חיו חודשים רבים יותר מהצפוי. אצל המגיבים, תאי T המותאמים התרחבו בעוצמה גבוהה יותר בדם, ורמות IL-7 ו-XCL1 בדם עלו בהתאם לעיצוב הטיפול.
מציצים לתוך השכונה החיסונית של הגידול
כדי להבין כיצד RD07 פועל בבני אדם, הצוות בחן דגימות גידול ברזולוציה של תא בודד לפני ואחרי הטיפול. הם ראו כי החלק של תאי סרטן החיוביים ל-Claudin18.2 ירד במטופלים מגיבים, מאשר שהטיפול פגע ביעד המיועד. במקביל נרשם פרץ במגוון קלוני של תאי T, כולל תאי קילר פעילים ותאי זיכרון שוהים-רקמה, מה שמרמז שהגוף מפעיל מתקפת חיסון רחבה יותר. תאי דנדריט מיוחדים הראו סימני פעילות מוגברת ואינטראקציות חזקות יותר עם תאי T מתרבים, תואם להשפעת XCL1 שמושכת אותם אל הגידול. בדיקות דימות של חתך גידול של מטופל אחד חשפו פחות תאים של הגידול ותאי מיאלואיד מדכאים אחרי הטיפול, עם יותר תאי T ו-B וסידור מחודש של הרקמה לאזורים עשירים בחיסון—מאפיינים של מיקרוסביבה "חמה" ומדוללת.
מה זה עשוי לעמוד עבור טיפול בסרטן בעתיד
במבט כולל, הממצאים הפרהקליניים והקליניים המוקדמים מרמזים כי RD07 עושה יותר מאשר להוסיף תרופה ממוקדת נוספת לארסנל הטיפולי. על-ידי שילוב זיהוי הגידול עם תמיכה חיסונית מובנית, תאים מהונדסים אלה יכולים לשרוד זמן רב יותר, לגייס תאי שותף מרכזיים ולעזור לאמן את מערכת החיסון של המטופל לשמור על הגידול תחת שליטה, גם כאשר היעד המקורי אובד. למרות שהניסוי היה קטן ונערך בחולים שעברו טיפולים רבים, ההצטמצמות הקבועה של הגידול, הבטיחות המקובלת והשינוי העמוק במערכת החיסון מעודדים. אם יאוששו במחקרים גדולים יותר, גישה זו עלולה לפתוח פרק חדש בטיפול בגידולי דרכי העיכול, שבו העצמת המערכת החיסונית בתוך הגידול תהיה חשובה כמו הפגיעה ההתחלתית בתאי הסרטן עצמם.
ציטוט: Zhao, X., Liu, J., Zhang, Z. et al. Efficacy and immunomodulatory effect of Claudin18.2-specific IL-7/XCL1 armored CAR-T cells in digestive tract cancer: preclinical and clinical analysis. Sig Transduct Target Ther 11, 87 (2026). https://doi.org/10.1038/s41392-026-02621-8
מילות מפתח: טיפול בתאי CAR-T, סרטן דרכי העיכול, מיקרוסביבת הגידול, Claudin18.2, אימונותרפיה