Clear Sky Science · he
חלבון דמוי-Visinin 1 מחריג הומאוסטזיס של סידן ומקדם פרפור פרוזדורים במודלים אנושיים ובמכרסמים
מדוע הסיפור הזה על קצב הלב חשוב
פרפור פרוזדורים הוא בעיית קצב לב שכיחה שמעלה את הסיכון לשבץ ולתשישות לב. רבים חיים איתה, ועדיין רופאים מתקשים למנוע אותה או למנוע חזרה לאחר טיפול. המחקר הזה חושף חלבון שזכה להתעלמות עד כה בתאי הלב, הנקרא VILIP-1, הפועל כמו מתג סידן פגום ותורם לפרפור פרוזדורים בבני אדם ובחיות. על ידי זיהוי המתג הזה והדגמה כי תרופות קיימות יכולות לדכא אותו, העבודה פותחת מסלול חדש לעבר טיפולים בטוחים וממוקדים יותר.
מבט מקרוב על פעימה כאוטית
בלב בריא, גליוּת חשמלית מתפשטת באופן מסודר בחללים העליונים, הפרוזדורים, ומכוונת כל פעימת לב. הסדר הזה תלוי במידה רבה בסידן, מינרל טעון שנכנס ויוצא מתאי הלב כדי לתאם כיווץ והרפיה. בפרפור פרוזדורים תנועת הסידן הופכת לאי־סדירה: דליפות נוספות ותנודות ברמות הסידן מעוררות אותות חשמליים משוטטים שיכולים להתפתח לקצבים מהירים ולא סדירים. רופאים ידעו לאורך זמן שמחסור בשליטה על סידן הוא מרכזי בהפרעה זו, אך הטריגרים המקדימים שמתחילים את הכאוס נשארו מטושטשים.
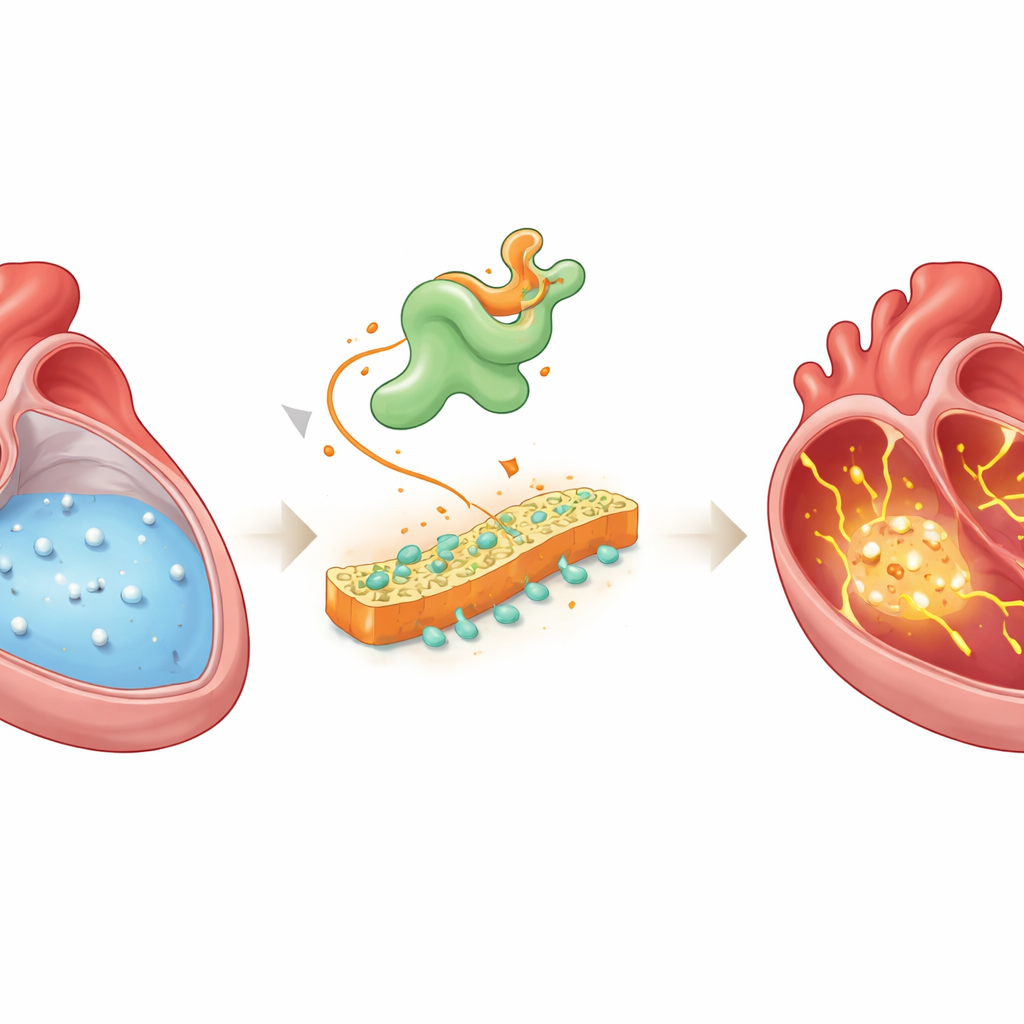
מוצאים מטריד מוסתר
החוקרים שילבו מספר שיטות מתקדמות כדי לחפש מולקולות שמקשרות בין ניהול סידן מופרע לבין פרפור פרוזדורים. הם הקליטו אותות סידן ממאות תאי פרוזדור בודדים בעכברים עם פרפור פרוזדורים שהועלה בקוצב, ואז רקמו את מערך הגנים הפעילים באותם תאים. הם גם השוו פעילות גנטית ברקמת פרוזדור של חולים עם פרפור פרוזדורים לזו של חולים עם קצב תקין. כאשר הניחו את מערכי הנתונים האלה זה על גבי זה ועקבו כיצד התאים משתנים מהמצב הבריא לחולה, גן אחד בלט שוב ושוב: Vsnl1, שמקודד לחלבון VILIP-1, מולקולת חישת סידן שלמדו עליה בעיקר במוח ולבלב, ולא בלב.
כיצד VILIP-1 מבלבל את מאזן הסידן
ברקמת פרוזדור הן של מטופלים והן של מודלים חייתיים, רמות VILIP-1 היו גבוהות משמעותית, והחלבון הצטבר במעטפת התא. כדי לבדוק האם שינוי זה היה רק לוואי או מניע, הצוות אילץ תאי פרוזדור בעכברים לייצר VILIP-1 נוסף. עכברים אלה לא הראו נזק מבני בולט ללב, אך הפרוזדורים שלהם הפכו לקלים בהרבה לגרום להם לפרפור במהלך קוצב חשמלי. הקלטות חשמליות מפורטות הראו יותר דיכוי לאחר דה-פולריזציות—פרצים חריגים לאחר כל פעימה—ואלטרנטיביות בצליל הפוטנציאל הפעולה בין פעימה לפעימה, חתימות קלאסיות להתנהגות חשמלית לא יציבה הקשורה לעומס סידן. הדמיית סידן ברזולוציה גבוהה אישרה גלים ספונטניים תכופים של סידן ומאגרי סידן פנימיים מודלדלים, מה שמעיד על דליפה פנימית חמורה בתאים.
שותף קריטי על פני הממברנה
כדי להבין כיצד VILIP-1 גורם להפרעה הזאת, המדענים מיפו אילו חלבונים מתקשרים עמו בתוך תאי הלב. באמצעות שתי שיטות משלימות—משיכת שותפים נקשרים מרקמת פרוזדור ותיוג חלבונים סמוכים ב"הילת ביוטין" בתאים חיים—הם צמצמו את החיפוש ל-NCX-1, מחליף הנתרן–סידן העיקרי בממברנת פני התא של הלב. מחליף זה בדרך כלל מסייע להוצאת סידן בתמורה לנתרן, אך בתנאים מסוימים הוא יכול לפעול בהיפוך ולהביא סידן לתוך התא. המחקר הראה ש-VILIP-1 נקשר פיזית ל-NCX-1 ומגביר את מספר מולקולות NCX-1 המוטמעות בממברנה מבלי להעלות את ייצור ה-NCX-1 הכולל. כתוצאה מכך, הזרמים של המחליף התעצמו, וחסימת NCX-1 בעזרת מעכב סלקטיבי הפחיתה גלי סידן והקשתה על הפעלת פרפור פרוזדורים בעכברים עם עודף VILIP-1.
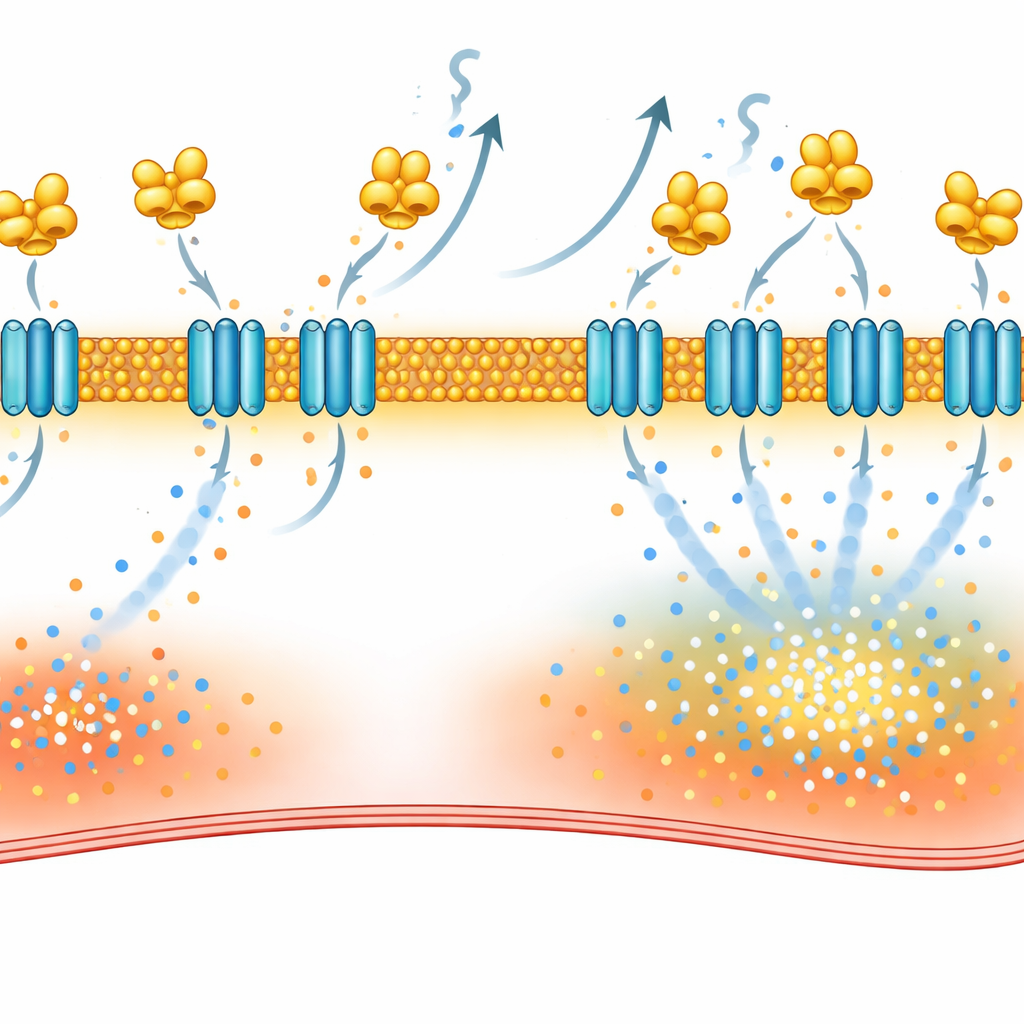
כיבוי המתג הפגום בעזרת תרופות קיימות
VILIP-1 עוגן לממברנות דרך תיוג שומני הנקרא מייריסטואיל, שנחשף כאשר סידן נקשר לחלבון. הצוות השתמש בדסלורטדין, שהודגם קודם שהוא מפריע לשלב תיוג זה, ומצא שהוא הוריד את NCX-1 על פני הממברנה, הנרמל את זרמי המחליף, הקטין גלי סידן וקיצץ את פרקי פרפור הפרוזדורים במודלי חולדות. הם גם בדקו רפגליניד, תרופת סוכרת הידועה בקיבוע לחיישני סידן קשורים. בדיקות ביו־פיזיקליות אישרו שרפגליניד נקשר ישירות ל-VILIP-1. בעכברים שמקבלים קוצב ובברקמות פרוזדור של חולים עם פרפור פרוזדורים, טיפול ברפגליניד הקטין את ריכוז NCX-1 בממברנה, הרגיע דליפת סידן בתאים בודדים והוריד משמעותית את הנטייה להשריש פרפור פרוזדורים.
מה משמעות הדבר עבור אנשים עם קצב לב לא סדיר
בסך הכול, המחקר מתאר לולאה מחזקת עצמית: עלייה בריכוזי הסידן מגייסת VILIP-1 למעטפת התא, שם הוא מגדיל את NCX-1, מה שיוצר עוד עומס סידן ומכין את הקרקע לפרפור פרוזדורים. על ידי הפרעת הלולאה ברמת VILIP-1—או על ידי חסימת העוגן השומני שלו או על ידי קישור לגרעין חיישן הסידן שלו—תרופות קיימות יכולות להשיב איזון סידן יציב יותר ולהפחית פגיעות באריתמיה ברקמות לב אנושיות ובמכרסמים. אמנם דרוש עוד מחקר כדי לשפר את הספציפיות של התרופות ולבחון את האסטרטגיות במודלים חייתיים גדולים ובניסויים קליניים, VILIP-1 עולה כעת כמטרה מבטיחה למניעה וטיפול בהפרעת קצב לב נפוצה ולעתים עיקשת זו.
ציטוט: Xiong, K., Wang, G., Li, D. et al. Visinin-like protein 1 disrupts calcium homeostasis and promotes atrial fibrillation in human and rodent models. Sig Transduct Target Ther 11, 105 (2026). https://doi.org/10.1038/s41392-026-02615-6
מילות מפתח: פרפור פרוזדורים, אותות סידן, אריתמיה לבבית, מחליף נתרן–סידן, יעדי טיפוליים