Clear Sky Science · he
סינרגיה כימו‑פוטותרמית מציתה חיסון אנטי‑גידולי דרך פרוטוזיס ברזל
הפיכת החום והאור של הגוף ללוחם בסרטן
תרופות כימותרפיות יכולות לצמצם גידולים, אך לעתים קרובות מלוות בתופעות לוואי קשות וללא יכולת תמידית למנוע חזרת המחלה. מחקר זה חוקר דרך חדשה להעצים ולמקד תרופה קיימת, דוקסטקסל, על ידי אריזתה בחלקיקים זעירים הרגישים לחום והפעלתם באמצעות אור תת‑אדום סמוך. המטרה היא לא רק להרוג תאי גידול בדיוק גבוה יותר, אלא גם לעורר את המערכת החיסונית כך שתזהה ותרדוף את הסרטן בגוף כולו ותמנע הישנות בעתיד. 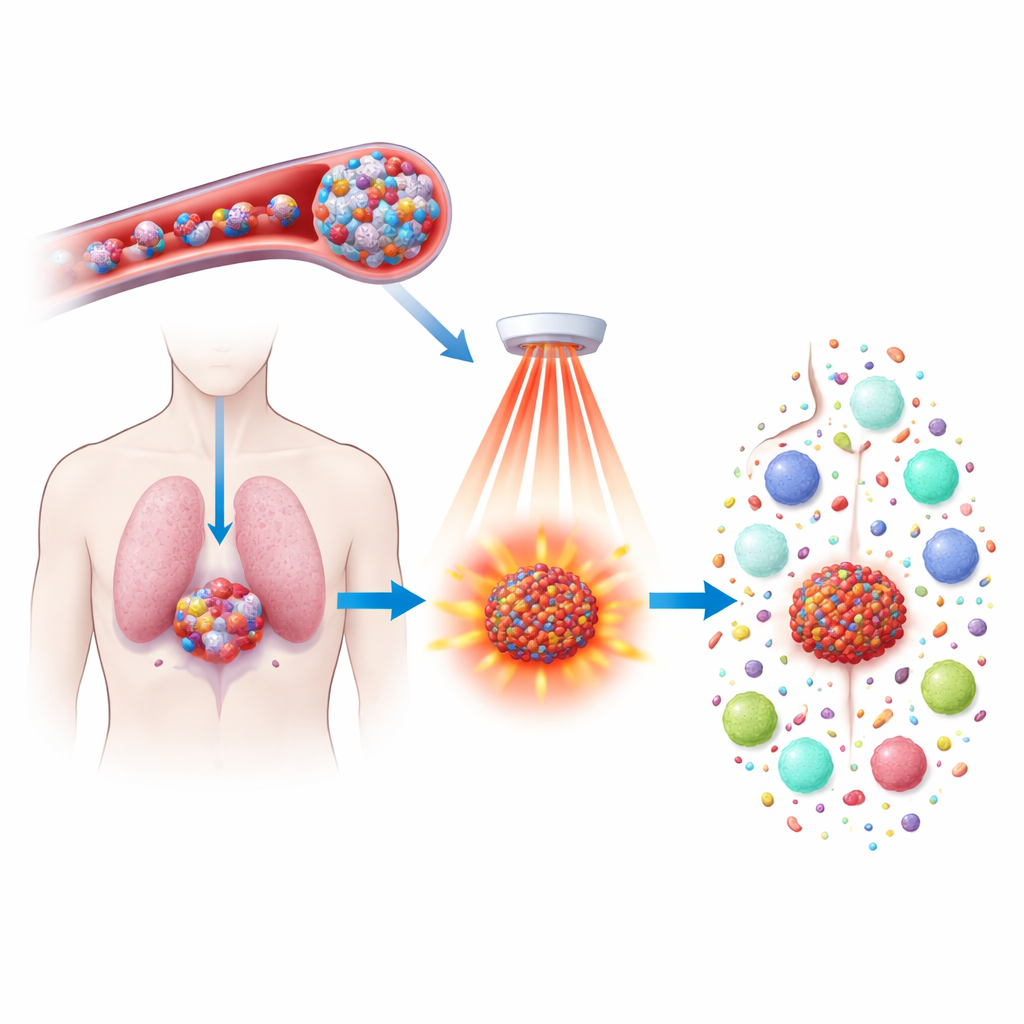
שליחים זעירים שיודעים לאן להגיע
החוקרים בנו סוג חדש של ננוחלקיקים מפולימר המכיל פררוצן, מולקולה שמעבירה ברזל והגיבה בחוזקה עם מי חמצן — מחמצן שנמצא בכמויות גבוהות יותר בתוך גידולים מאשר ברקמות תקינות. פולימרים אלה מתארגנים עצמונית לכדורים הידרופיליים שיכולים לשאת הן דוקסטקסל והן צבע סופג‑אור בשם IR808. לאחר הזרקה למחזור הדם, החלקיקים קטנים ויציבים מספיק כדי להסתובב ולזלוג אל תוך הגידולים, שם כלי הדם הדולפים ורמות המי חמצן הגבוהות מתחילים להחליש את החלקיקים ולשחרר לאט את המטען שלהם. העיצוב הזה מרוכז את הטיפול בגידולים בעודו מצמצם נזק לאיברים בריאים.
שימוש באור כדי להגביר נזק מקומי
אור תת‑אדום סמוך, שיכול לחדור רקמות בבטחה, מכוון לאזור הגידול. ה‑IR808 שבתוך הננוחלקיקים סופג את האור והופך אותו לחום ובו בזמן מייצר מינים פעילים חמצוניים. השילוב של מי החמצן המיוצרים בגידול והתחמוצות המונעת באור גורם לחלקיקים להתפרק מהר יותר ולשפוך את מטען התרופה בדיוק במקום שבו הוא דרוש. במקביל, הברזל בחלק הפררוצני מסייע להפוך את המתחמצנים לצורות במיוחד אגרסיביות שנלחמות ברכיבים השומניים של ממברנות התאים. המתקפה הכימית והתרמית הממוקדת הזו מגדילה בצורה חדה את כוח ההריגה בהשוואה לדוקסטקסל או לטיפול באור לבדם. 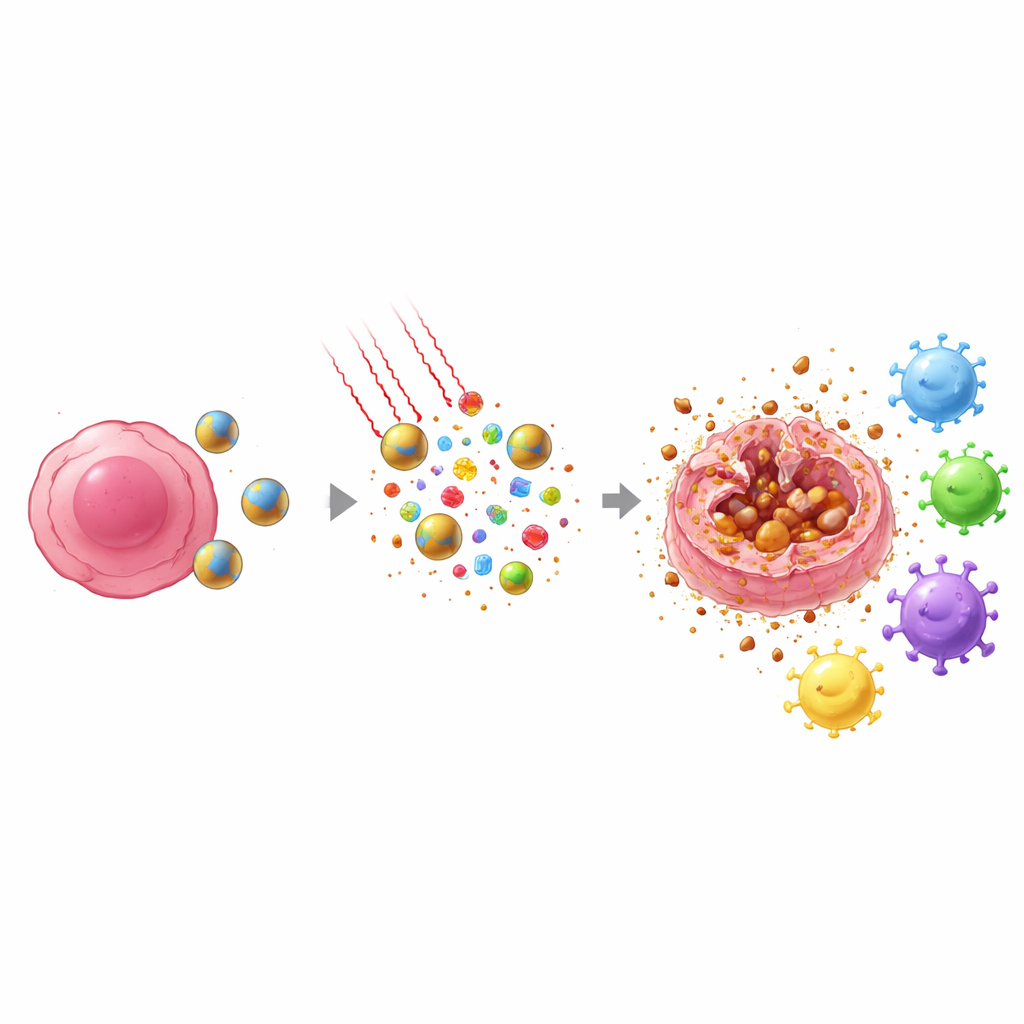
בעירה מבוקרת שמשדרת אות למערכת החיסון
חשוב לציין שהאופן שבו תאי הגידול מתים בטיפול זה שונה מכימותרפיה רגילה. במקום להתפרק בשקט לחתיכות מסודרות, רבים מהתאים עוברים תהליך הנקרא פרוטוזיס (ferroptosis), צורת מוות מודעת מונעת‑ברזל שפוגעת בשומנים ושבה הממברנה החיצונית נשברת. כאשר זה קורה, התאים משפכים אותות אזעקה פנימיים וקטעי אנטיגן ספציפיים לגידול לסביבה. במקביל, דוקסטקסל דוחף חלבון גרעיני מרכזי, HMGB1, לעבר קצה התא ומכין אותו לשחרור. יחדיו, החום, המתחמצנים ופעולת התרופה יוצרים גל של אותות סכנה ואנטיגן ששומרים חיסוניים סמוכים — תאי דנדריטים — יכולים לזהות ולהוביל אל קשרי הלימפה.
מהתקפה מקומית להגנה גוף‑שלם
בדגמי גידול בחולדות/בעכברים, הטיפול המשולב כימו‑פוטותרמי לא רק הקטין את הגידולים שהוחמו ישירות בצורה יעילה יותר מכל רכיב בודד, אלא גם שינה את הנוף החיסוני. הגידולים הראו יותר תאי דנדריט בוגרים ומספרים גדולים יותר של תאי T קטלניים, הן בתוך הגידול והן בקשרי הלימפה הניקוזים. בכמה עכברים עם מערכת חיסון תקינה, הגידולים הראשוניים נעלמו לאחר שני מחזורי טיפול בלבד. כאשר המדענים שתלו לאחר מכן גידולים חדשים באתרים מרוחקים או בצד הנגדי של הגוף, גידולים שניוניים אלה האטו או הושתקו, מה שמרמז שהחיות פיתחו צורת זיכרון חיסוני ספציפי לסרטן. הוספת נוגדן שחוסם נקודות בקרה שמונע תשישות תאי‑T הפחיתה עוד יותר גרורות בריאה והאריכה הישרדות, מה שמעיד שניתן לשלב טיפול מקומי זה עם אימונותרפיות מודרניות.
מדוע זה חשוב לטיפול העתידי בסרטן
לקורא שאינו מומחה, המסקנה המרכזית היא שהגישה הזו הופכת את הדוקסטקסל מרעל מערכתי גס לחלק מאסטרטגיה חכמה רב‑שלבית נגד סרטן. על ידי אריזה של התרופה בננוחלקיקים המכילים ברזל ומופעלים באור שמגיבים לכימיה של הגידול עצמו, הטיפול מספק יותר נזק בתוך הגידולים תוך שמירה על רקמות בריאות. דפוס המוות התאי שהוא מעורר פועל בדומה לחיסון מתוך הגידול — הוא מלמד את המערכת החיסונית לזהות ולהזכיר את הסרטן. אם ממצאים אלה יתורגמו לבני אדם, מערכות כימו‑פוטותרמיות כאלה עשויות לסייע בהמרת גידולים עמידים "קרים" ל"חמים" שיתנו תגובה טובה יותר לטיפולים מבוססי חיסון, עם הפחתת הישנות ושיפור בשליטה ארוכת‑טווח.
ציטוט: Lin, J., Yang, H., Zou, Z. et al. Chemo-photothermal synergy ignites antitumor immunity via ferroptosis. Sig Transduct Target Ther 11, 98 (2026). https://doi.org/10.1038/s41392-026-02608-5
מילות מפתח: ננו‑רפואה בסרטן, טיפול פוטותרמי, פרוטוזיס (ferroptosis), אימונותרפיה נגד סרטן, העברת דוקסטקסל