Clear Sky Science · he
פרודרוג נאוזים קואורדינטיבי מוליך מפעיל מדויקת פיירופטוזיס, קופרוטוזיס ופררוטוזיס לחיסון נגד סרטן באתר
להפוך גידולים לחיסונים נגד עצמם
טיפול בסרטן בדרך כלל שואף להרוג תאי גידול ישירות, אבל מה אם אפשר להפוך את הגידול לחיסון נגד עצמו? המחקר הזה מתאר "פרודרוג" ננו־חלקיק חכם שנודד בבטחה בגוף, נדלק רק בתוך הגידולים, ואז מכריח את תאי הסרטן למות בצורה שמפעילה בעוצמה את המערכת החיסונית. התוצאה היא לא רק כיווץ הגידולים הראשוניים, אלא גם אימון הגוף לצוד גידולים מרוחקים ומטסטזות.
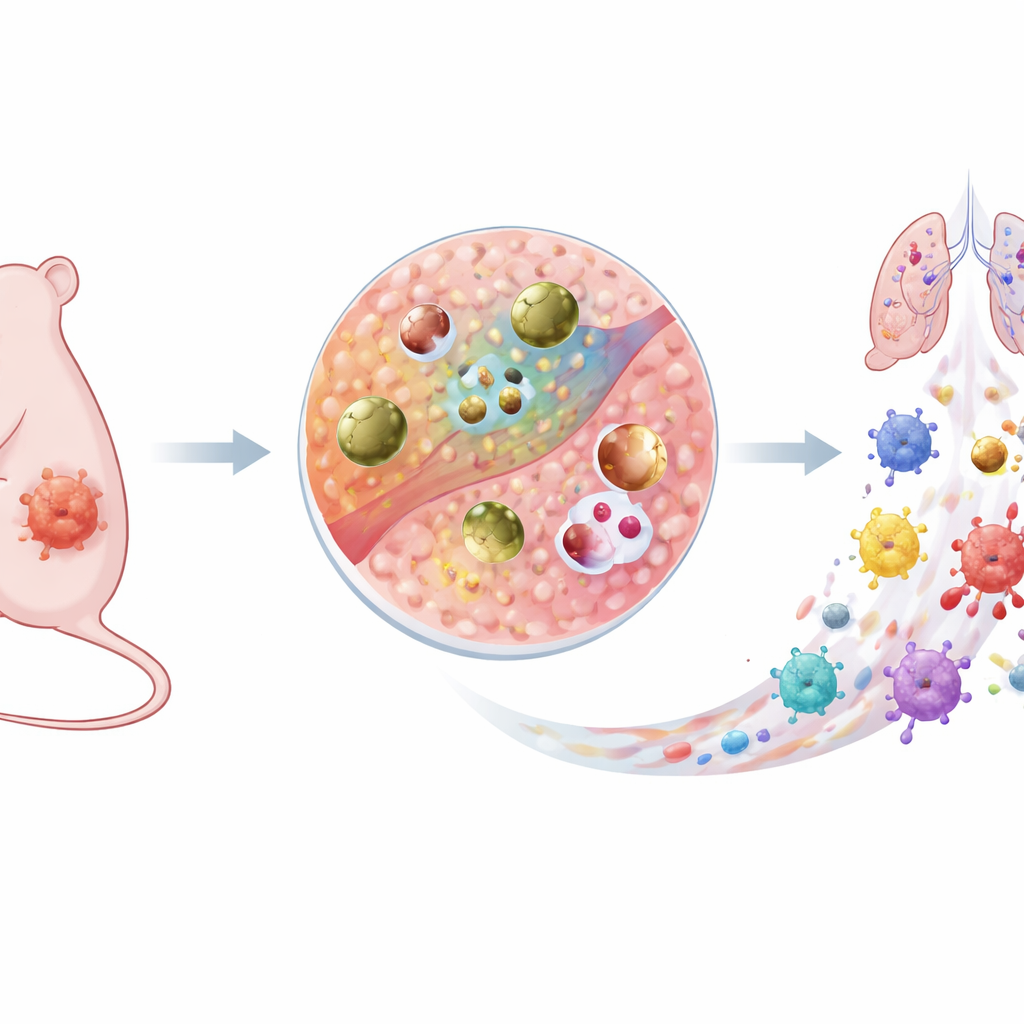
סוג חדש של נשק חכם נגד סרטן
החוקרים בנו חלקיק נחושת זעיר הנקרא Cu–DHN שמתנהג כמו תרופה רדומה בזמן ההסתובבות בדם וכוח תוקף ברגע שהוא מגיע לגידול. הוא מורכב מיונים של נחושת, מולקולת קדם־חומר בלתי מזיקה (1,5־דיהידרוקסי־נפתאלן, או DHN) וחומצת האמינו ציסטאין. יחד הם יוצרים רשת קואורדינטיבית מוליכה, כלומר אלקטרונים יכולים לנוע בקלות דרך החלקיק. "כביש האלקטרונים" הפנימי הזה מאפשר לכל הננו־חלקיק, לא רק לפני השטח שלו, להשתתף בריאקציות כימיות. באופן קריטי, ה‑Cu–DHN מתוכנן להגיב רק לכימיה החריגה של המיקרו‑סביבה הגידולית, שם הגלוטתיון האנטי־חמצוני ומימן הפרוקסיד נמצאים ברמות חריגות גבוהות.
איך הכימיה של הגידול מדליקה את המתג
בתוך הגידולים, Cu–DHN פועל כמו אנזים מלאכותי. בנוכחות גלוטתיון ומימן פרוקסיד ביחד, הוא קודם כל משתמש בגלוטתיון כדי לאפס את יוני הנחושת למצב ריאקטיבי מאוד ולאחר מכן משתמש במימן הפרוקסיד כדי לייצר פרץ מתמשך של חמצנים תוקפניים במיוחד (רדיקלים של הידרוקסיל). חמצנים אלה מבצעים פעולה כפולה: הם פוגעים ברכיבים תאיים וממירים את ה‑DHN הבלתי מזיק הכלוא בתוך החלקיק ליוגלון, תרכובת אנטי־סרטן חזקה. היוגלון, בתורו, מדכא את המנגנונים האנטי־חמצוניים של הגידול ומגביר עוד יותר את רמות מימן הפרוקסיד, ויוצר לולאת חיזוק עצמי של מתח חמצוני שנשארת מוגבלת לגידול, משום שרק הגידולים מספקים את הקלטים הכימיים המתאימים להתחלת המחזור.
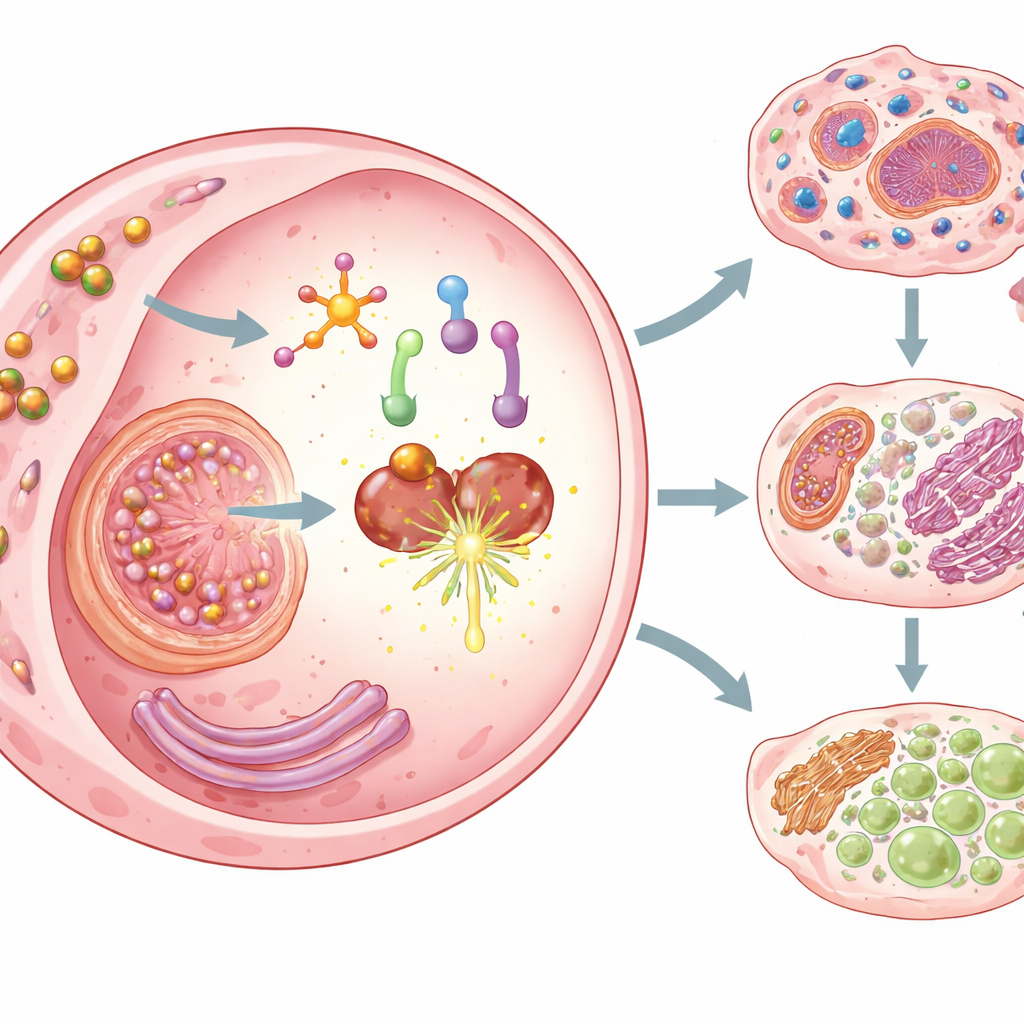
הפעלת שלוש צורות של מוות תאי סרטני
ברגע שמופעל, Cu–DHN עושה יותר מרק להרוג תאי סרטן באופן הרעיל. הוא מפעיל שלוש צורות מות תא מוסדרות שהן במיוחד בולטות לעיני המערכת החיסונית. ראשית, היוגלון הופך שתק אפיגנטי של חלבון יוצר נקבוביות בשם גזדרמין D ומפעיל קומפלקס חיישן דלקתי, כך שהתאים עוברים פיירופטוזיס — צורת מוות דרמטית ודלקתית שמפוצצת את הממברנה ומשפכה תכולה פנימית. שנית, הנחושת שנשאת על ידי הננו־חלקיקים, שנקלטת ביעילות על ידי תאי הסרטן, דוחפת קופרוטוזיס, צורת מוות הקשורה לצבירה רעילה של נחושת במכונות מטבוליות מרכזיות. שלישית, על‑ידי שפיכת גלוטתיון ונטריקת אנזים מגן (GPX4), Cu–DHN מקדם פררוטוזיס — מוות המונע על ידי פרוקסידציה של ליפידים. ביחד, מצבי המוות האלה מבטיחים שתאי הסרטן לא רק נהרגים ביעילות אלא גם מתים באופן שמגרה חיסוניות.
ממתקפה מקומית להגנה בכל הגוף
הפיירופטוזיס והנזק החמצוני הנלווה גורמים לתאי הגידול לשחרר שיטפון של אותות אזעקה: אנטיגנים משויכים לגידול, מולקולות סכנה כמו ATP ו‑HMGB1, וסימני לחץ על פני השטח שלהם. במודלים של עכברים עם סרטן שד אגרסיבי, הזרקה בודדת של Cu–DHN לגידולים הראשוניים הובילה להפעיל חזק של תאי דנדריט בקשריות הלימפה הקרובות ולגל פריצת CD8 ציידי גידול. תאי חיסון אלה אז נדדו לגידולים לא מטופלים בצד הנגדי של הגוף ולריאות, שם האטו או כמעט מנעו את גדילת גידולים חדשים וצברי גרורתיים. חסימת תאי CD8 הסירה ברובה את ההגנה הזו, ואישור ש‑Cu–DHN הופך את הגידול הראשוני לחיסון אתר־מקומי שמלמד את המערכת החיסונית לזהות ולהשמיד סרטן במקומות אחרים.
השפעות חזקות עם פרופיל בטיחות טוב יותר
חשש חשוב בטיפולים שמבוססים על פיירופטוזיס הוא הסיכון לפגוע ברקמות בריאות, שגם הן נושאות את אותם חלבוני יצירת הנקבוביות. כאשר היוגלון ניתן ישירות בצורה הפעילה שלו, עכברים סובלים מרעילות משמעותית לכבד, לכליות ולדם. לעומת זאת, Cu–DHN נשאר לא פעיל ברקמות בריאות, כי הן חסרות את שילוב הטריגרים הכימיים הדרושים להפעיל את החלקיק. בעכברים, Cu–DHN השיג את כוח ההריגה של הגידול ואת הפעילות האנטי־מטרסטטית של היוגלון הפעיל תוך הימנעות מנזק לאיברים, הפרעות בדם וירידה במשקל. במילים פשוטות, העבודה הזו מראה כיצד ננו־חלקיק מוליך חכם יכול להישאר שקט בגוף, להתעורר רק בתוך גידולים, לכפות על תאי סרטן למות בצורה שמניעה את המערכת החיסונית, ובכך לשמש כפלטפורמת חיסון מדויקת ועצמית נגד סרטן.
ציטוט: Wang, Y., Zhao, H., Sun, K. et al. Conductive coordination nanozyme prodrugs precisely trigger pyroptosis, cuproptosis and ferroptosis for in situ cancer vaccination. Sig Transduct Target Ther 11, 96 (2026). https://doi.org/10.1038/s41392-026-02607-6
מילות מפתח: אימונותרפיה של סרטן, ננו־רפואה, פיירופטוזיס, חיסוני סרטן, מיקרו־סביבה של הגידול