Clear Sky Science · he
השמדת DUSP6 משחזרת את היכולת של תאי CAR T שנפגעו מאובדן CD58 בגידול באמצעות התעוררות אותות AP-1
מדוע חשוב להעצים את תאי הלחימה בסרטן
תאי חיסון מהונדסים, ידועים כ־CAR T, שינו את מהלך הטיפול בסוגים מסוימים של סרטן הדם, אך עדיין רבים מהחולים חוזרים למחלה משום שהגידולים לומדים להימנע מהתקפה. המחקר הנוכחי חושף חולשה נסתרת בכמה גידולים שמנטרלת שקטה את תאי ה‑CAR T מבפנים — ומראה כיצד שינוי גנטי מדויק יכול להשיב לתאים אלה את הסיבולת, אספקת האנרגיה וכוח ההרג שלהם. לקורא זהו מבט על האופן שבו טיפולי תאים מדור הבא עשויים להפוך לעמידים ויעילים יותר עבור יותר אנשים.
אחיזת יד חסרה על תאי הגידול
תאי CAR T זקוקים לאחיזה יציבה במטרתם כדי לפעול היטב. תאים רבים של גידול מציגים על המשטח המולקולה CD58 שממלאת תפקיד של "ידית" עבור תאי החיסון, ועוזרת להם להיאחז וליצור אזור מגע הדוק. מחקרים קודמים הראו שכאשר הסרטן מאבד CD58, תאי CAR T מתקשים ליצור את המגע הזה והופכים לפחות יעילים. במחקר זה בדקו החוקרים שאלה עמוקה יותר: מעבר לבעיה המכנית של האחיזה, כיצד אובדן CD58 מחדש את הביולוגיה הפנימית של תאי CAR T וכך מחליש את ביצועיהם לאורך זמן?
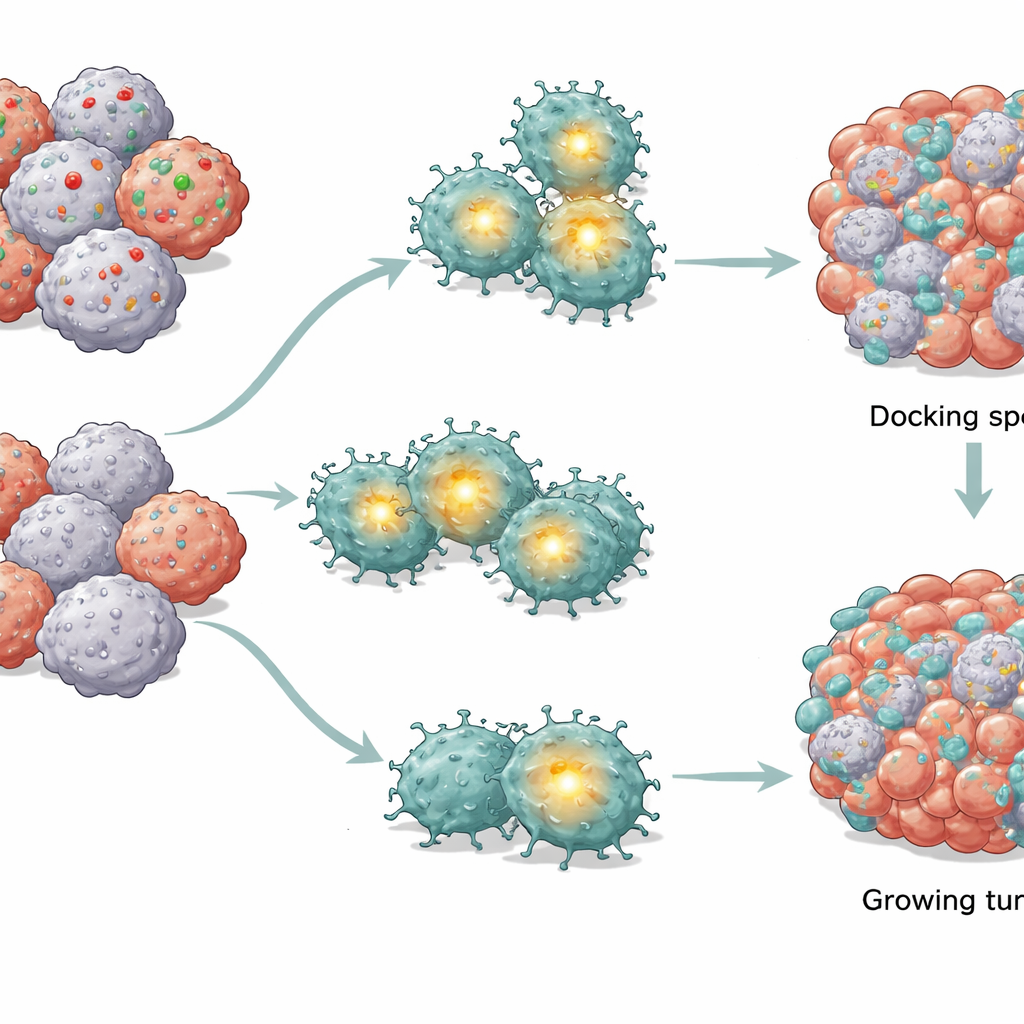
חיווט מקוצר בתוך תאי CAR T
בהשוואת תאי CAR T שנחשפו לגידולים תקינים לאלה שניצבו מול גידולים חסרי CD58, הצוות מצא כי מרכז בקרה פנימי מפתח בתאי ה‑T — שנקרא AP‑1 — עומד מוחלש באופן סלקטיבי, בעוד שדרכים מרכזיות אחרות של איתות נותרו ברובן שלמות. AP‑1 הוא קבוצה של חלבונים שמפעילים גנים המעורבים בהפעלה ובהישרדות. כשהפעילות של AP‑1 נחלשה, תאי CAR T הראו סימני משבר אנרגטי פנימי מובהקים: פחות מיטוכונדריות וקטנות מהרגיל (תחנות הכוח שלהם), יכולת מופחתת לצרוך חמצן ולעבד סוכרים, ואובדן המתח החשמלי על פני קרומי המיטוכונדריה. במקביל הצטברו מולקולות תגובתיות חמצוניות מזיקות. שינויים אלה דחפו יחד את תאי CAR T לתוכנית השמדה עצמית המבוססת על נזק במיטוכונדריה שלהם, אף בלי קיומם של אותות מוות חיצוניים.
כיבוי הבלם הפנימי
כדי להבין מדוע AP‑1 נחלש כל כך, חיפשו החוקרים מעלה מולקולרי — "בלמים" שעשויים להיות פעילים מדי. הם מצאו כי תאי CAR T המתמודדים עם גידולים שליליים ל‑CD58 הגדילו את הפעילות של מספר פוספטאזות — אנזימים שמכביקים מסלולי איתות — ובמיוחד אחת שנקראת DUSP6. באמצעות תרופות ולאחר מכן עריכה גנטית מדויקת לחסימת אנזימים אלה, גילו החוקרים שהסרת DUSP6 היא שתחזיק בעוצמה הגדולה ביותר לשחזור פעילות AP‑1. תאי CAR T שעברו עריכה של DUSP6 התרבו טוב יותר, יצרו יותר מיטוכונדריות, שרפו דלק ביעילות גבוהה יותר, ייצרו יותר מולקולות ההרג של הסרטן והיו פחות מועדים לאפפטוזה, בעיקר כאשר נתקלו בחזרה מול תאים גידוליים חסרי CD58.
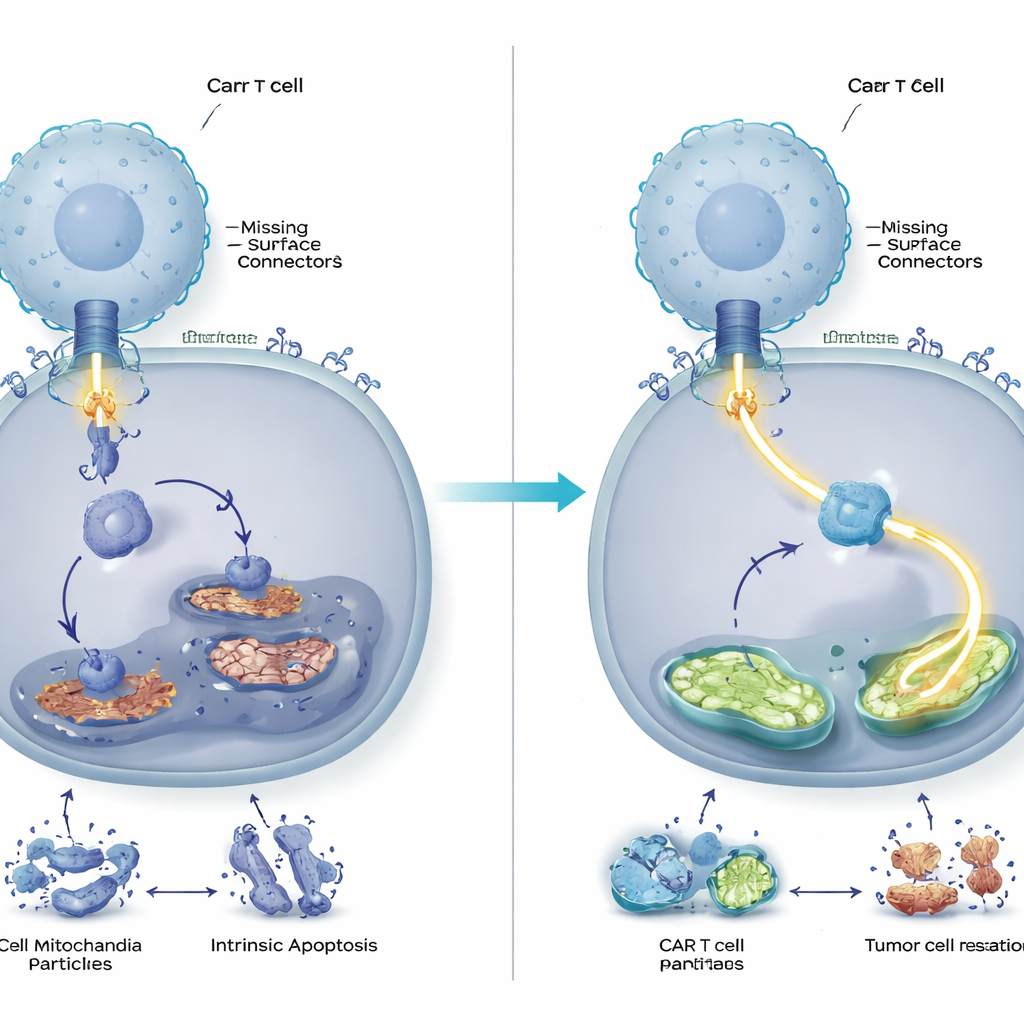
שליטה חזקה וארוכת טווח בגידול בחיות
הצוות בדק לאחר מכן האם כוונון מולקולרי זה באמת משנה במערכות חיות. בעכברים נשאים של תאים אנושיים של סרטן דם, שהיו או חסרי CD58 או בעלי CD58, תאי CAR T חסרי DUSP6 נקו את הגידולים ביתר יעילות ושמרו עליהם מושלטים זמן ארוך יותר מתאי CAR T רגילים. התאים המהונדסים התרבו בעוצמה רבה יותר, הראו פחות סימני תשישות והפרישו רמות גבוהות יותר של מסרים חיסוניים מרכזיים. ראוי לציין שהיתרונות של הסרת DUSP6 נראו לא רק במקרה בו הגידולים איבדו CD58 אלא גם כששמרו עליה, מה שמרמז כי שינוי זה עשוי לשפר באופן כללי טיפולי CAR T במקום להיות תיקון צר לתת‑סוג נדיר של גידול.
רמזים מנתוני מטופלים
כדי לבחון רלוונטיות בבני אדם, בחנו החוקרים נתוני ביטוי גנים מאנשים שטופלו בתאי CAR T או בתרופות חוסמות ציר נקודת ביקורת חיסונית. בחולים עם לימפומה זלגית גדולה B שהקבלו טיפול CAR T דו‑מטרתי, רמות DUSP6 נמוכות יותר בתאי CD8 לפני או זמן קצר אחרי ההזרקה היו מקושרות לשיעורי תגובה מלאה גבוהים יותר. בקוהורט נפרדת של סרטן העור שטופלה בנוגדנים נגד PD‑1, תאי CD8 מותשים של חולים שלא הגיבו נטו לבטא יותר DUSP6 מאשר אלה של מגיבים. יחד, תצפיות אלה מציעות ש‑DUSP6 פועל כסמן שלילי של כושר תאי T במגוון אימונותרפיות וכי הורדתו עשויה לשפר תוצאות.
מה משמעות הדבר לטיפולי סרטן עתידיים
לקריא מן השורה: חלק מהגידולים מתחמקים מהתקפת תאי CAR T לא רק על ידי הסתרה מזיהוי אלא על ידי סאבטאז׳ למנועי הפנים של התאים. איבוד "ידית" CD58 על תאי הגידול מוריד בשקט את אותות AP‑1 בתאי CAR T, מרוקן את המיטוכונדריות שלהם, מעלה תוצרי לוואי רעילים ודוחף אותם לעבר מוות מוקדם. בהסרת הבלם DUSP6, המדענים יכולים לשחזר את האיתות האבוד הזה, לתקן את בריאות המיטוכונדריה ולהעניק לתאי CAR T סיבולת וכוח הרג גדולים יותר, גם מול גידולים עמידים. אמנם נדרשים עוד מבחני בטיחות וקליניים, אך השמדה של DUSP6 עולה כמח_strategy מהתקנה מהנדסת מבטיחה להפוך את "תרופות החיות" נגד סרטן לעוצמתיות יותר, ארוכות טווח ובעלות פוטנציאל להועיל לטווח רחב יותר של חולים.
ציטוט: Ma, X., Zhang, Y., Wang, Y. et al. DUSP6 ablation restores CAR T-cell fitness impaired by tumor CD58 loss through invigoration of AP-1 signaling. Sig Transduct Target Ther 11, 100 (2026). https://doi.org/10.1038/s41392-026-02597-5
מילות מפתח: תאי CAR T, CD58, DUSP6, אימונותרפיה של סרטן, מטבוליזם של תאי T