Clear Sky Science · he
שחרור הפוטנציאל של מסלול STING המוּתוּך במטעני ננובום בימטליים כדי לשפר משתפי‑פעולה דו‑ספציפיים של תאי T לטיפול פוטו‑אימונותרפי בסרטן המעי הגס
לחזור ולהפנות את המערכת החיסונית נגד סרטן המעי
סרטן המעי והחלחולת נפוצים ולעתים קטלניים, חלקית כי הגידולים לומדים להתחבא ממערכת החיסון. מחקר זה בוחן אסטרטגיה חדשה שאוחזת כמה מנגנוני לחימה בסרטן בתוך "ננובום" זעיר אחד, כדי להעיר את ההגנות של הגוף, לסייע לתאי החיסון לאתר את הגידול, ולמנוע מהסרטן לחזור או להתפשט.
מדוע תרופות חיסוניות של היום זקוקות לשדרוג
סוג מבטיח של תרופות בסרטן, שנקראות משתפי‑פעולה דו‑ספציפיים לתאי T, פועלות כמו מכנים ביולוגיים: קצה אחד תופס תא T (לוחם חיסוני מרכזי) והקצה השני מתחבר לסמן על תא הגידול, וכופה על השניים להיפגש כדי שהתא ה‑T יהרוג. בעוד שהן עוצמתיות בסרטנים של דם, תרופות אלה מתקשות בפצעים מוצקים כמו סרטן המעי הגס. הן מופרשות במהירות מהגוף, עלולות לתקוף רקמות בריאות שמשתפות את אותו הסמן, ולעיתים נתקלות בגידולים "קרים" שחסרים בהם תאי חיסון מספיקים כדי שהטיפול יעבוד. לכן רופאים ומדענים מחפשים דרכים להעביר את התרופות האלה בבטחה יותר ולהפוך גידולים קרים ל"חמים" המלאים בתאי חיסון מוקטבים.
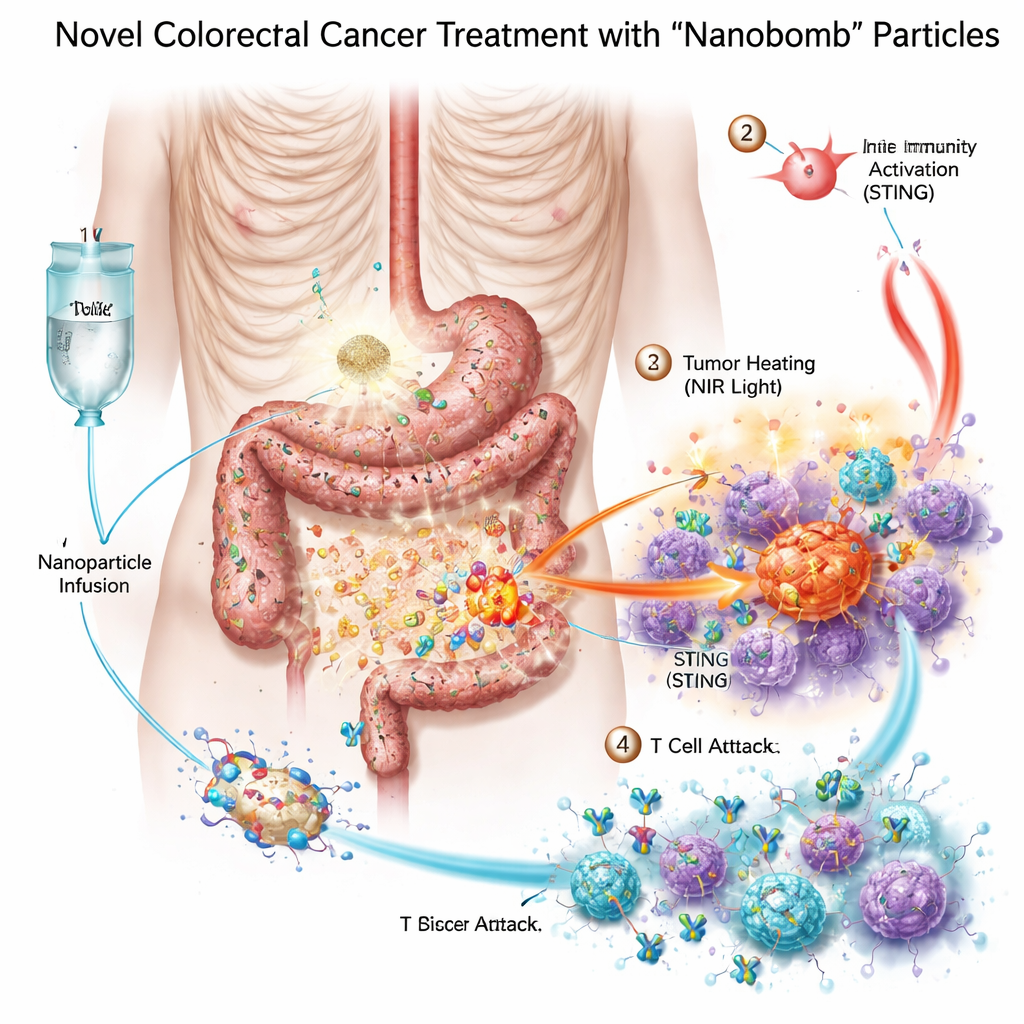
אריזה של שלוש נשקים בתוך "ננובום" זעיר אחד
החוקרים תכננו ננובום בימטלי — בשמו המדעי MnO2/Co‑DA@BiTE/HPT — שמשלב שלוש מצבי טיפול בחלקיק אחד. תחילה, הליבה מכילה מנגן וקובלט, מתכות שיכולות להפעיל מערכת אזעקה תאית הנקראת מסלול STING, שמסייעת לגוף לחוש סכנה ולגייס תאי חיסון. שנית, פני השטח של החלקיק מצופים במשתף‑פעולה דו‑ספציפי לתאי T שמקשר בין תאי T ותאי סרטן. שלישית, החומר סופג אור בקרינת תת‑אדום קרוב, מה שמאפשר לחמם את הגידול מבחוץ בתוך טיפול פוטותרמלי. כדי לוודא שהננובומים יתמקדו בתאי סרטן של המעי הגס, הצוות הוסיף קטע DNA קצר, אפטמר, שמזהה את PD‑L1, מולקולה שלעתים קרובות שפעילה על גידולים אלה. כאשר חלקיקים אלה מגיעים לגידול, אנזימים טבעיים ברקמת הגידול מסייעים לפרק אותם ולשחרר את המטען בדיוק במקום שבו הוא נדרש.
חימום, איתות וגיוס צבא החיסון
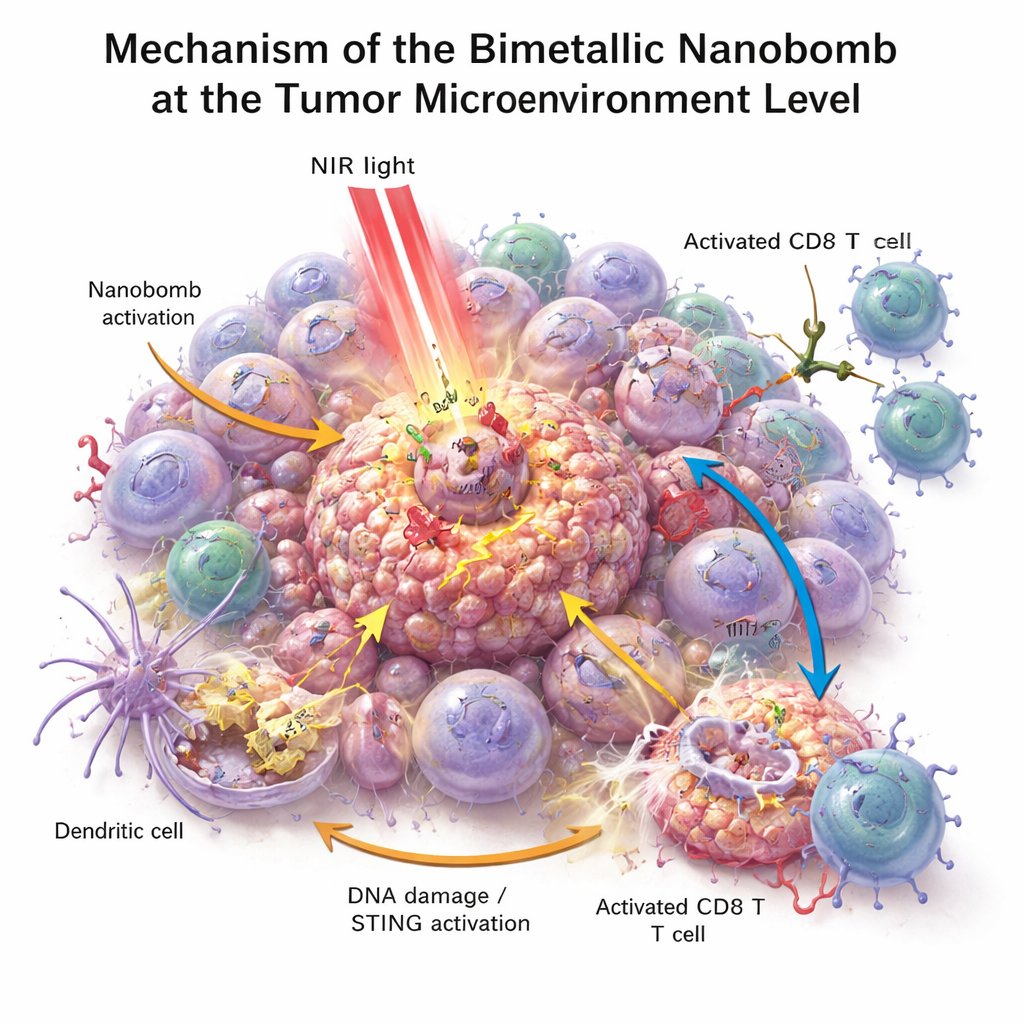
בצלוחיות מעבדה, הננובומים השמידו תאי סרטן של המעי הגס ביעילות רבה יותר מכל רכיב בודד לבדו. כאשר הוארו בקרינת תת‑אדום קרוב, החלקיקים התחממו, יצרו לחץ ונזק בתאי הסרטן, וסייעו לייצר סוגי חמצן תגובתיים — מולקולות פעילות מאוד שפוגעות עוד בתאי הגידול. הלחץ הזה שבר את ה‑DNA של התאים ודחף אותם לצורת מוות בולטת במיוחד ששולחת אותות "סכנה". תאי חיסון קרובים, ובעיקר תאי דנדריט, בלעו את חומרי התאים המתים והפעילו את מסלול STING בעזרת המנגן והקובלט המשוחררים. הם אז ייצרו אינטרפרונים ומתווכים דלקתיים אחרים שמבשלים ומגייסים תאי T. במקביל, המשך‑הפעולה הדו‑ספציפי על הננובום קישר פיזית בין תאי T לתאי גידול החיוביים ל‑PD‑L1, ושיפר את הפעלת תאי ה‑T וההריגת גידול גם בגידולים שהיו קודם כבדים ו"קרים".
מתכווץ הגידול לזיכרון חיסוני מתמשך
במספר דגמי עכברים — כולל גידולי מעי תת‑עוריים, גידולים בשני צידי הגוף, גרורות ריאה ומודל החמרה לאחר ניתוח — הננובומים יחד עם אור האטו בעוצמה או כמעט עצרו את גדילת הגידול. בגידולים שטופלו היו הרבה יותר תאי CD8 הורגים ופחות תאי רגולציה‑T שלרוב מדכאים תגובות חיסוניות. תאי דנדריט בתוך הגידולים ובבלוטות הלימפה הראו סימנים של התמחות, ובדיקות דם חשפו רמות מוגברות של ציטוקינים מגרי חיסון. חשוב מכך, עכברים שניקו את הגידולים לאחר טיפול בננובום היו מוגנים טוב יותר כאשר הוחזרו אליהם תאי הסרטן, ונוצרו אצלם פחות גרורות ריאה — מה שמעיד שהטיפול סייע לבנות זיכרון חיסוני ארוך‑טווח ולא רק לכווץ את הגידול פעם אחת.
מה זה עשוי להצביע לגבי טיפול בסרטן בעתיד
עבודה זו מציגה תרופות ננו‑מנטריות "מתקפת‑שלוש" שמחממות גידולים, מפעילות אזעקת סכנה פנימית ומכוונות תאי T ישירות לתאי הסרטן — כל זאת בתוך חלקיק ממוקד יחיד. בעכברים, הגישה הזו לא רק הפכה גידולים קרים של המעי הגס לחמים ודלקתיים, אלא גם סייעה למנוע חזרה והתפשטות. למרות שהטכנולוגיה עדיין רחוקה משימוש קליני — הגדלה להיקף, בטיחות לטווח ארוך ובדיקות בבני אדם נותרות אתגרים מרכזיים — היא מציעה מתווה לטיפולים עתידיים המשלבים חומרים חכמים עם תרופות חיסוניות כדי להעניק למטופלים תגובה אנטי‑סרטן חזקה ועמידה יותר.
ציטוט: Mu, M., Li, H., Chen, B. et al. Unleashing the potential of bimetallic nanobomb-mediated STING pathway to enhance bispecific T-cell engager against colorectal cancer photo-immunotherapy. Sig Transduct Target Ther 11, 80 (2026). https://doi.org/10.1038/s41392-026-02596-6
מילות מפתח: סרטן המעי הגס, אימונותרפיה, ננו‑חלקיקים, מסלול STING, משתף‑פעולה דו‑ספציפי לתאי T