Clear Sky Science · he
טיפול מונחה פרמקוקינטיקה–פרמקודינמיקה מותאם אישית באמצעות פלטפורמת רב‑אורגנואיד נגזרת מתאי גזע פלוריפוטנטיים מושרים בסרטן השד עם מוטציית NF1
למה מחקר זה חשוב עבור מטופלים
רבים מהמטופלים בסרטן מקבלים תרופות שעובדות היטב אצל חלק מהחולים אך לא אצל אחרים, ולעתים גורמות לתופעות לוואי קשות. מחקר זה מתאר דרך חדשה לבדוק טיפולים נגד סרטן מחוץ לגוף באמצעות מיני‑איברים שגודלו במעבדה מתאים של המטופל עצמו. העבודה מתמקדת בצורת סרטן שד שקשה לטפל בה ומונעת על‑ידי שינויים בגֵן הקרוי NF1, ומדגימה כיצד שילוב של אסטרטגיית תיקון גן עם תרופה ממוקדת יכול להוביל לטיפול בטוח, יעיל ומותאם אישית באמת.
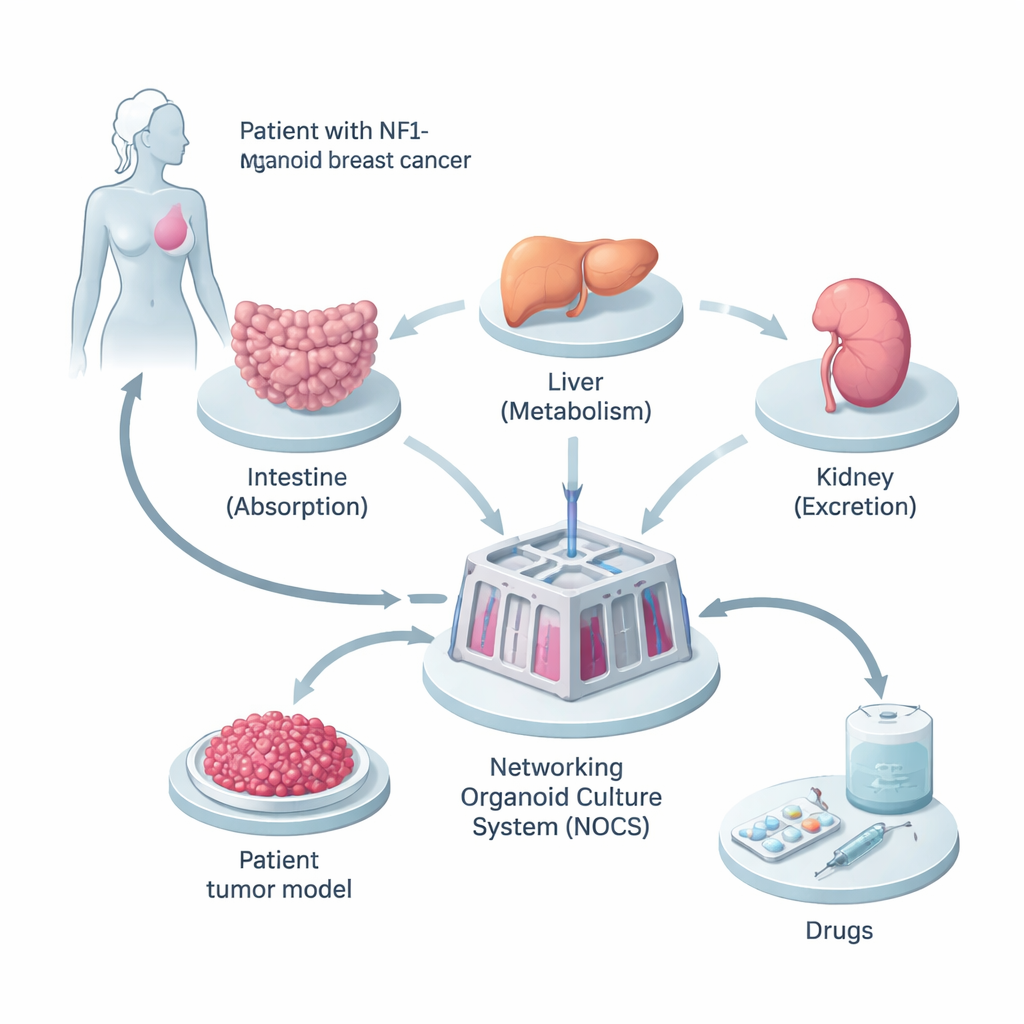
בניית גרסה מיניאטורית של גוף המטופל
החוקרים התחילו מרקמה של אישה שסרטן השד שלה נשא מוטציה תורשתית בגן NF1. הם תכנתו מחדש את התאים הדמויי עור התקינים שלה לתאי גזע פלוריפוטנטיים מושרים, היכולים להפוך כמעט לכל סוג תא בגוף. מהם גידלו שלושה סוגי מיני‑איברים—מעי דק, כבד וכליה—מפני שאלו הם האתרים המרכזיים שבהם תרופות נספגות, מעובדות ומוסרות. במקביל יצרו ספירואידים תלת‑ממדיים של הגידול מתאים סרטניים שלה, ושמרו על תערובת סוגי התאים והשינויים הגנטיים שהיו בגידול המקורי.
מעגל בדיקה חי של תרופות
כדי לגרום לאותם מיני‑איברים להתנהג יותר כמו גוף אמיתי, הקבוצה קישרה ביניהם במכשיר ממולא נוזל שנקרא מערכת תרבית אורגנואידים מקושרת, או NOCS. בסידור זה המדיום זורם בין מדורי המעי, הכבד, הכליה והגידול, ומחקה את מחזור הדם. ניתן להוסיף תרופות באופן המדמה בליעה או קבלת זריקה, וחיישנים ומשאבות שולטות בקצב תנועת ה"דם" ובתדירות הריענון שלו. זה איפשר למדענים לעקוב כמה תרופה נספגת, כמה מהר היא מתפרקת וכמה חזק היא פועלת על הגידול—ולכל זה במודל אנושי מותאם‑מטופל.
תיקון גֵן שבור באמצעות דילוג על אקזון
הגידול של המטופלת נשא מוטציה מזיקה ב‑NF1 שממשיכה להפעיל מסלולי גדילה ומגבילה את יעילותן של תרופות תקניות רבות. הצוות תכנן מקטעים קצרים של חומר גנטי, שנקראים אוליגונוקלאוטידים אנטיסנס, כדי לגרום למכונת עיבוד ה‑RNA של התא לדלג מעל החלק הפגום (אקסון 2) של גן NF1. באמצעות מערכת ידבוקת ויראלית שמשמרת פעולה למשך ימים, הם יצרו דילוג יציב על האקסון בתאי הסרטניים של המטופלת. כך נוצר חלבון NF1 מקוצר אך פונקציונלי, אותות הגדילה המופרזים נחלשו, ותאי הגידול הפכו רגישים יותר לטיפול.
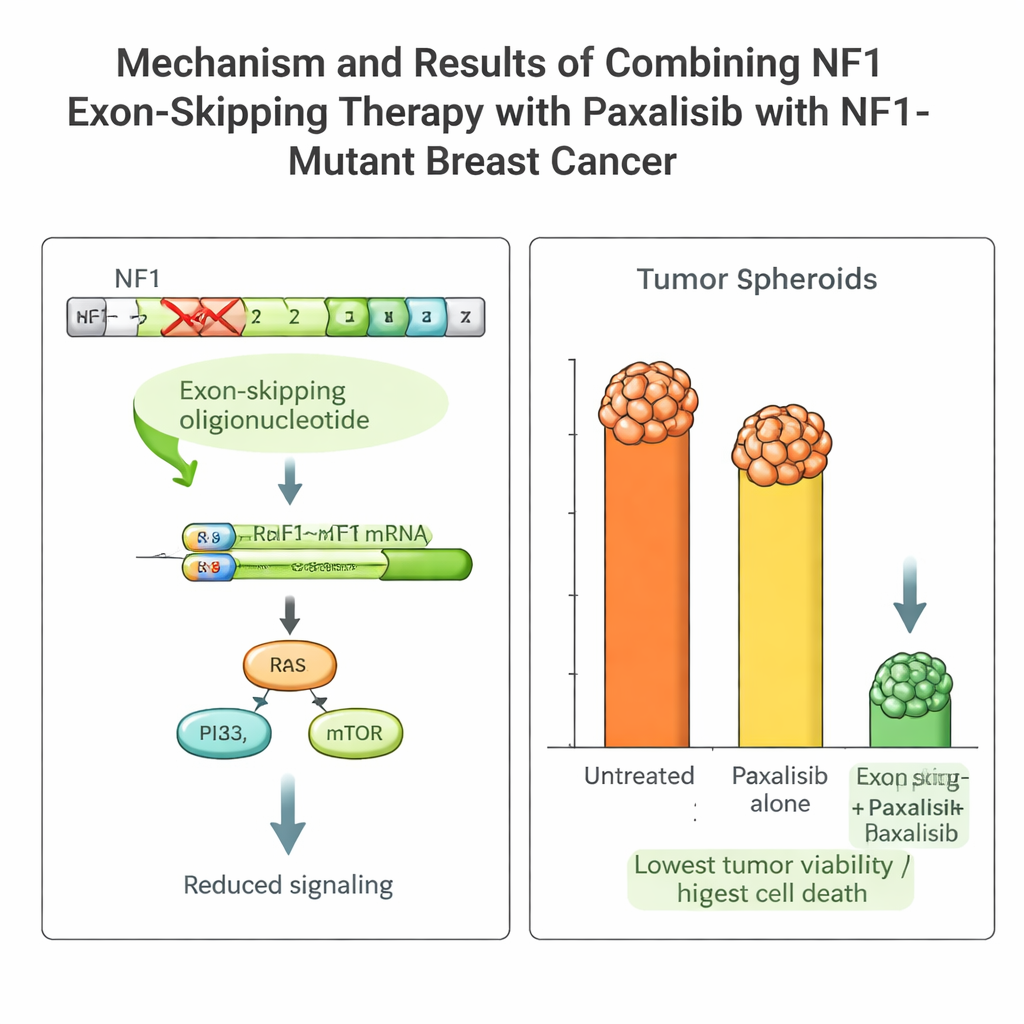
בחירת התרופה הממוקדת הנכונה עם הדרכת PK/PD
בזכות פלטפורמה זו השוו החוקרים מספר תרופות מתקדמות שחוסמות את ציר PI3K–mTOR, שממוקם אחרי NF1 במורד הזרם. הם מדדו פרמקוקינטיקה (איך הגוף מנהל את התרופה) ופרמקודינמיקה (איך התרופה פועלת על הגידול) הן בעכברים והן ב‑NOCS. תרופה אחת, פאקסליסיב (Paxalisib), בלטה: היא נספגה היטב במעי, נשמרה ברמות שימושיות במערכת והציגה התנהגות דומה בבעלי‑חיים ובמכשיר האורגנואידים. כשהיא שולבה עם דילוג האקסון ב‑NF1, הכוח ההורס של פאקסליסיב נגד תאי הגידול של המטופלת גדל באופן דרמטי, עם ירידות חזקות בצמיחה וסימני מוות תאי מתוכנת ברורים, הן ב‑NOCS והן בעכברים נשאי גידול המטופלת.
איזון תועלת וסיכון בין האיברים
מכיוון שמודלי המעי, הכבד והכליה היו חלק מאותו מעגל, החוקרים יכלו גם לצפות סימני נזק מוקדמים לאיברים. פאקסליסיב גרמה לתגובות סטרס ולחלישות עדינה במחסום במודלי המעי והכליה וסימני מאמץ בכבד, אך ללא אובדן משמעותי של חיוניות התאים במינון שנבדק. סוג זה של מבט על כל הגוף, באמצעות רקמה אנושית, מציע דרך להשוות אפשרויות טיפול לא רק לפי עד כמה הן מצמצמות גידולים, אלא גם לפי השפעתן על איברים בריאים — לפני שהתרופה אף מגיעה לחולה.
מה משמעות הדבר עבור טיפול בסרטן בעתיד
במלים פשוטות, המחקר מראה שכעת אפשר לגדל "גוף מיניאטורי על שבב" מפושט ומותאם‑לחולה שיכול לבדוק כיצד תרופות שונות — ואפילו גישות לתיקון גנים — יתנהגו וישתלבו. עבור מטופלת זו עם סרטן שד נשא NF1, האסטרטגיה האופטימלית הייתה שילוב של טיפול בדילוג אקסון על NF1 והתרופה הפומית פאקסליסיב, שהאטו יחד את צמיחת הגידול הרבה יותר מכל אחת בנפרד. אם יפותח הדבר weiter ונבדק בעוד מטופלים, פלטפורמות כאלה יכולות לכוון רופאים לתוכניות טיפול המותאמות לגנים ולביולוגיה של כל אדם, לשפר את סיכויי ההצלחה ולהפחית רעילות לא נחוצה.
ציטוט: Lim, J.H., Mun, S.J., Kang, H.M. et al. Personalized pharmacokinetic–pharmacodynamic guided therapy via an induced pluripotent stem cell–derived multi-organoid platform in NF1-mutant breast cancer. Sig Transduct Target Ther 11, 79 (2026). https://doi.org/10.1038/s41392-026-02595-7
מילות מפתח: אונקולוגיה מותאמת אישית, סרטן השד, אורגנואידים, מוטציית NF1, טיפול ממוקד