Clear Sky Science · he
הגברת פעילות KLF15 בקרדיומיוציטים: גישה חדשה למניעת תכנות פתולוגי ופיברוזה באמצעות dCas9VPR חסר נוקלאז
תכנות מחדש של הלב הכושל
אי ספיקת לב פוגעת במיליונים, ולעתים מתפתחת בהדרגה לאחר שנות יתר לחץ דם או מחלת מסתם. במצבים אלה תאי שריר הלב לא רק מתרחבים, אלא גם מפעילים תוכנית גנטית "עוברית" והלב מתמלא ברקמת צלקת. מחקר זה בוחן שיטה חדשה לדחוף את מנגנון בקרה הגנטי של הלב חזרה לכיוון בריאות — ללא חיתוך DNA — על ידי הגברה עדינה של רגולטור מגן הנקרא KLF15 בקרדיומיוציטים.
כשתאי הלב מאבדים את זהותם
בלב בוגר ובריא, קרדיומיוציטים — תאי שריר הלב — צורבים שומנים בצורה יעילה לתפוקת אנרגיה ומתחזקים דפוס יציב של פעילות גנים. באמצעות רצף RNA ברמת התא הבודד בעכברים שנחשפו לעומס לחץ כרוני, החוקרים מיפו כיצד קרדיומיוציטים בודדים משתנים כשהלב עובר מתפקוד נורמלי להתרחבות ולבסוף לכישלון. הם מצאו כי גורם שעתוק בשם KLF15, שאמור לשמור על שיווי משקל בין מטבוליזם וצמיחה, הראה את השינוי החזק ביותר בפעילות בתאים החולים. ככל שהעומס גדל, רמות KLF15 ירדו ויכולתו לדכא גנים עובריים וקשורים למתח נחלשה. דפוסים דומים של ירידה ב‑KLF15 נצפו גם בלבבות אנושיים של חולים עם קרדיומיופתיה דילטטיבית והיפרטופית, מה שמצביע על כך שההפרעה הזאת שמורה במינים שונים.
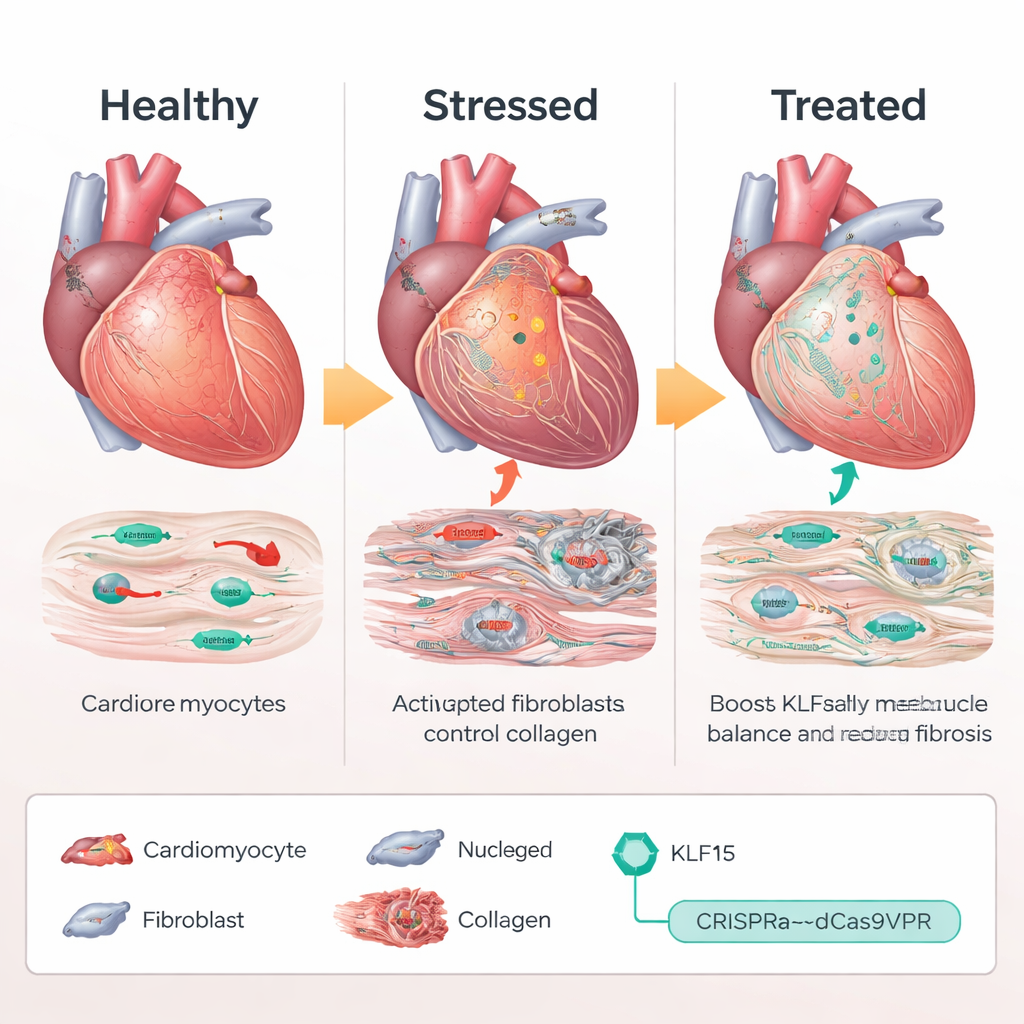
שימוש ב‑CRISPR כסיבוב עוצמה, לא כסכין
במקום להוסיף עותק נוסף של גן KLF15 או לחתוך DNA, הצוות השתמש במערכת "הפעלה" מבוססת CRISPR, הנקראת dCas9VPR, שנקשרת בקרבת הגן הטבעי Klf15 ומגבירה את הבטא האנדוגנית שלו. בעכברים מהונדסים המביעים את מפעיל ה‑CRISPR הזה אך ורק בקרדיומיוציטים, המדענים מסרו RNA מנחים באמצעות נגיף אדנו‑קשור (AAV9) כדי לכוון את הפרומוטר של Klf15. תחת עומס לחץ כרוני, עכברים שקיבלו מנחים המפעילים את Klf15 שמרו על רמות Klf15 קרובות לנורמליות. תאי שריר הלב שלהם נשארו קטנים יותר, תפקוד השאיבה הידרדר פחות, וההישרדות השתפרה בהשוואה לבעלי חיים בבקרת. ברמה המולקולרית, גנים של לחץ ועובריות שתקו, בעוד שגנים מטאבוליים ומטפלים בסידן חזרו לתפקוד, מה שמצביע על כך שהתוכנית השעתוקית הפגומה הותקנה מחדש ברוב המקרים.
השקטת יצירת הצלקת באמצעות תקשורת בין‑תאית
אי ספיקת לב מונעת לא רק מתאי שריר חולים אלא גם מפיברובלסטים, תאי תמיכה שמייצרים קולגן ויוצרים רקמת צלקת נוקשה. ניתוחים ברמת תא בודד وتصوير רקמות הראו שהשבת Klf15 בקרדיומיוציטים הפחיתה את הפעלת הפיברובלסטים ואת הפיברוזה הכוללת, אף על פי שהטיפול הגנטי לא כוון ישירות לפיברובלסטים. הצוות עקב אחרי השפעה זו והצביע על חלבון מופרש בשם AZGP1. כאשר Klf15 הוגבר בקרדיומיוציטים, היו עלייה בייצור ובשחרור של AZGP1. הן בלבבות עכברים והן ברקמות לב אנושיות נגזרות מתאי גזע, AZGP1 גבוה דיכא את מסלול TGF‑β / SMAD בפיברובלסטים — נהג מרכזי ביצירת צלקת — והוריד רמות של סמנים כגון α‑SMA ו‑POSTN. חשוב לציין כי מעבר לביטוי מוגבר של AZGP1 בקרדיומיוציטים לבדם לא תכנת מחדש את תאי השריר, מה שמראה כי KLF15 מגן בעיקר על קרדיומיוציטים ישירות ומשתמש ב‑AZGP1 כשליח להגבלת הפיברובלסטים.
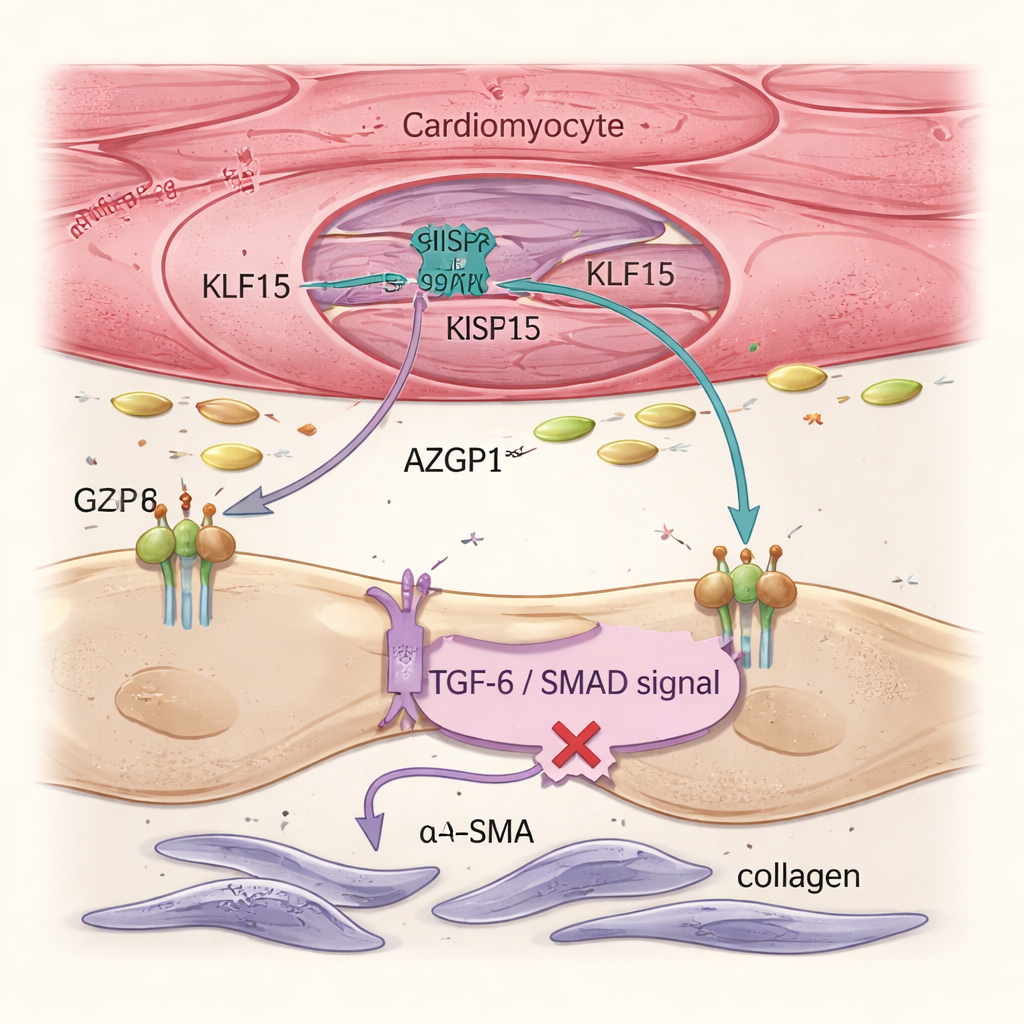
מודלים של רקמות אנושיות מאשרים את המעגל המגן
כדי לבדוק האם מנגנונים אלה מתקיימים בתאים אנושיים, החוקרים השתמשו בקרדיומיוציטים נגזרים מתאים פלוריפוטנטיים מושרים (iPSC) שגודלו ברקמות לב מהונדסות תלת‑ממדיות. כאשר נחשפו לעומס מכני המדמה יתר לחץ דם, רקמות אלה איבדו KLF15, הפעילו גנים של מתח ועובריות, התקשו, וכוח הכיווץ שלהן נחלש — חזרה על תכונות המחלה. שחזור KLF15 באמצעות CRISPRa מנע את הירידה הזו, שמר על יצור כוח ושיפר את ההבעה הגנית בחזרה לכיוון מטבוליזם ומבנה בוגרים. ניסויים מפורטים הראו כי TGF‑β1, אות פרו‑פיברוטי ידוע, מוריד את KLF15 בקרדיומיוציטים אנושיים דרך מסלול SMAD2/3, מה שמסייע להסביר כיצד מתח כרוני מוביל לעיבוד מזיק. לבסוף, הצוות הנדס מערכת CRISPRa קומפקטית, "מיני", המבוססת על וריאנט Cas9 קטן שמתאימה לוקטור AAV9 יחיד ומונעת על‑ידי פרומוטר ספציפי לקרדיומיוציטים. בפרוסות חדות בדיוק מרקמת לב אנושית כושלת, הוקטור הזה הגדיל בהצלחה את רמות KLF15 ושיפר את הביצועים הכיווציים במשך ימים בתרבית.
מתווה לגנטיפיה עדינה יותר
ללא מומחיות מיוחדת, המסר המרכזי הוא שעבודה זו ממחישה כיצד הגברה זהירה של רגולטור מגן בודד בתוך תאי שריר הלב יכולה גם לייצב את זהותם וגם לשלוח אותות שמגבילים את היווצרות הצלקת. באמצעות מפעיל מבוסס CRISPR שאינו חותך DNA, הגישה מתאמת את הגן הקיים של הלב במקום להכניס גן מלאכותי. המחקר מגדיר מסלול TGF‑β → KLF15 → AZGP1 שמקשר מתח מכני לעיבוד מזיק ומדגים, בעכברים, במודלי תאים אנושיים ובפרוסות רקמת לב אנושיות, כי השבתת KLF15 יכולה לקטוע את תגובת השרשרת הזו. אף שעדיין בשלב פרה‑קליני, מערכת CRISPRa הקומפקטית המכוונת לקרדיומיוציטים שמוצגת כאן מציעה מפת דרכים אפשרית לטיפול בצורות נפוצות של אי ספיקת לב שאינן גנטיות, באמצעות תכנות פעילות גנים במקום כתיבת הגנום מחדש.
ציטוט: Schoger, E., Kim, R., Bleckwedel, F. et al. Enhancing KLF15 activity in cardiomyocytes: a novel approach to prevent pathological reprogramming and fibrosis via nuclease-deficient dCas9VPR. Sig Transduct Target Ther 11, 76 (2026). https://doi.org/10.1038/s41392-026-02593-9
מילות מפתח: אי ספיקת לב, KLF15, הפעלה מבוססת CRISPR, פיברוזיס לבבי, AZGP1