Clear Sky Science · he
מולקולות חמצון תגובתיות (ROS) בסרטן: מהמנגנון להשלכות טיפוליות
כשמולקולות מועילות הופכות למסוכנות
בתוך כל תא, ניצוצות כימיים זעירים הנקראים מולקולות חמצון תגובתיות, או ROS, נוצרים כל הזמן כחלק מחיי התא השגרתי. ברמות המתאימות הן מסייעות לתאים לגדול, לתקשר ולהגן מפני מזיקים. אך מאמר זה מסביר כיצד אותן מולקולות יכולות גם לפגוע ב-DNA, לעוות את חיבורי התא ולהניע את הסרטן לצמוח, להתפשט ולהיות עמיד לטיפול. הבנת ה"חיים הכפולים" של ה-ROS מסייעת לחוקרים לעצב טיפולים חדשים בסרטן שמטרתם או להרגיע את המתח החמצוני המזיק או לדחוף אותו מעבר לקצה כדי להמית תאי גידול.
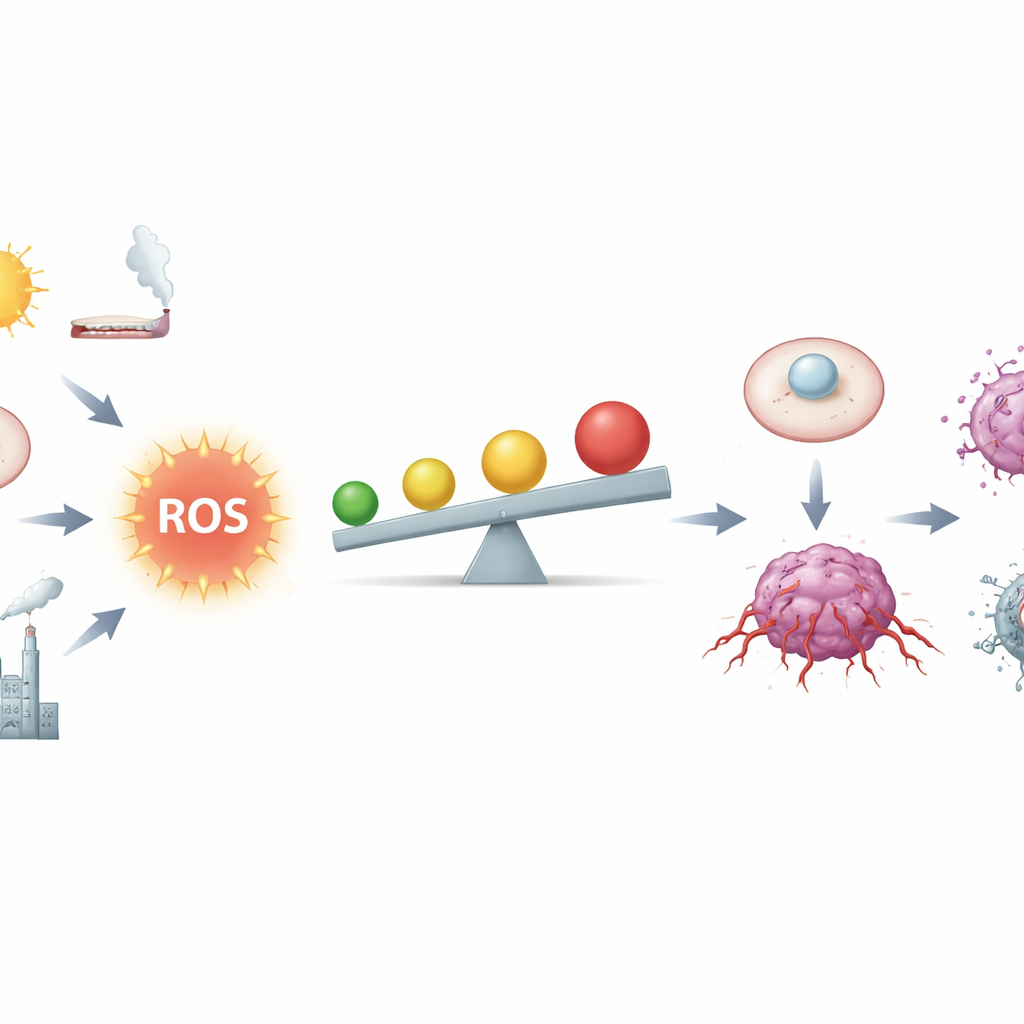
הקו הדק בין דלק לאש
המחברים מתארים את ה-ROS כתוצרי לוואי כימיים של הנשימה והמטבוליזם, אך גם כשליחים חזקים. ברקמות בריאות, רמות נמוכות של ROS עוזרות לשלוט במחזור התא, לתקן נזקים ולכוונן את המערכת החיסונית. תאים שומרים על אותות אלה תחת שליטה באמצעות רשת אנטי-אוקסידנטית מורכבת, כולל מולקולות כמו גלוטתיון ואנזימים שבניהולם עומד מתג מאסטר שנקרא Nrf2. תאי סרטן, לעומת זאת, פועלים קרוב יותר לאזור הסכנה: גנים פגומים, מיטוכונדריות מעומס יתר, דלקת כרונית, עישון, קרינה ומתכות מסוימות מגדילים את רמות ה-ROS. ברמות מתונות גבוהות ה-ROS יכולים לגרום לקרעים ב-DNA, ליציבות כרומוזומלית לקויה ולהפעלה כרונית של מסלולי גדילה והישרדות, מה שמקל על התא התקין להפוך לתא סרטני.
כיצד מתח חמצוני מעצב את התנהגות הגידול
לאחר שהגידול ביסס את עצמו, ה-ROS ממשיכים לעצב את הביולוגיה שלו. מתח חמצוני מתון מפעיל מסלולי גדילה רבים שמעודדים חלוקה תאית, יצירת כלי דם, חדירה לרקמות סמוכות ועמידות לכימותרפיה. ה-ROS יכולים לתכנת מחדש את האופן שבו תאי הסרטן משתמשים בסוכרים, בשומנים ובחומצות האמינו, ולהכווין דלק למסלולים שמייצרים כוח אנטי-אוקסידנטי נוסף וחומרי בניין לתאים חדשים. הם גם משפיעים על החלטות גורל התא: בהתאם לעוצמה ולהקשר, ה-ROS יכולים להזיז את המאזן לעבר אותות הישרדות או לעבר צורות שונות של מוות מתוכנת, כולל אפופטוזיס קלאסי וצורות חדשות כמו ferroptosis, necroptosis ו-cuproptosis. כך ה-ROS הם גם שותפים בהתקדמות הגידול וגם טריגרים פוטנציאליים להשמדת הגידול.
שכתוב המערכת החיסונית ותגובת התרופות
הסקירה מדגישה שה-ROS אינם פועלים רק בתוך תאי הסרטן — הם משנים גם את השכונה של הגידול. מתח חמצוני גבוה יכול לשחוק או להרוג תאי T ותאי NK לוחמי סרטן, תוך שזוית יתר לטובת תאים מדכאים שמגנים על הגידול מפני התקפה. ה-ROS מסייעים גם לגידולים להעלות ביטוי של אותות ״אל תהרוג אותי״ כמו חלבוני checkpoint, ומחלישים את ההשפעה של אימונותרפיה. במקביל, רמות מתונות של ROS יכולות להניע עמידות לתרופות על ידי חיזוק משאבות פליטת התרופות ומערכות התגובה ללחץ, מה שמאפשר לתאי סרטן להוציא החוצה כימותרפיה או לתקן את הנזקים שהיא גורמת. יחד עם זאת, בתנאים אחרים, דחיפת ה-ROS מעבר לסף קריטי יכולה לפרק את ההגנות הללו ולשחזר את הרגישות לטיפול.
להפוך חולשה רדוקסית לאסטרטגיית טיפול
מכיוון שתאי סרטן מתהלכים על חבל דק בין שימוש ב-ROS להרעלה מהם, המחברים רואים באיזון ה-ROS מנוף טיפולי. אסטרטגיה רחבה אחת היא להוריד ROS מזיקים או לחזק אנטי-אוקסידנטים, בעיקר למניעה או להגנה על רקמות בריאות בזמן טיפול. אסטרטגיה אחרת היא לעשות ההפך בגידולים: לעכב מערכות אנטי-אוקסידנטיות או להגביר ייצור ROS עד שתאי הסרטן יעברו את סף המוות, במיוחד בשילוב עם קרינה, תרופות ממוקדות או אימונותרפיה. גישה שלישית היא להשאיר את רמות ה-ROS כפי שהן אך לחסום את המתגים הרגישים ל-ROS — חלבוני איתות, אנזימי מטבוליזם או מסלולי מוות — שעליהם הגידול מסתמך. בכל הרעיונות הללו רצה הנושא של התאמה אישית: סוגי סרטן שונים נושאים "חתימות רדוקס" שונות, ולכן טיפולים עתידיים עשויים להזדקק לבדיקות דם או רקמה של נזק חמצוני, יכולת אנטי-אוקסידנטית וגנים הקשורים ל-ROS כדי לבחור את הטיפול המתאים לכל חולה.
מה המשמעות לחולים
במילים פשוטות, המאמר טוען ש-ROS אינם רעים לחלוטין ולא טובים לחלוטין; הם כלים רבי עוצמה שבהם משתמשים תאים — ובעלי חיים — כולל תאי סרטן. תאי סרטן נוטים לפעול קרוב יותר לנקודת ההיפוך של המתח החמצוני מאשר תאים בריאים, מה שעשוי ליצור חלון טיפולי. עם זאת, מאחר שאנטי-אוקסידנטים ופרו-אוקסידנטים יכולים להועיל או להזיק בהתאם למינון, לזמן ולסוג הגידול, שימוש גורף בתוספי תזונה או בתרופות שמגבירות ROS הוא מסוכן. המחברים מסכמים שהעתיד שייך לטיפולים ומבחנים מהונדסים בקפידה שקוראים את מצב הרדוקס של כל גידול ואז מניחים את ה-ROS ומערכות האנטי-אוקסידנטיות בדיוק הנדרש — או כלפי מטה כדי להגן על רקמות תקינות, או כלפי מעלה כדי לדחוף את תאי הסרטן מעבר לנקודת השבירה שלהם.
ציטוט: Akter, S., Madhuvilakku, R., Kar, A.K. et al. Reactive oxygen species (ROS) in cancer: from mechanism to therapeutic implications. Sig Transduct Target Ther 11, 111 (2026). https://doi.org/10.1038/s41392-026-02583-x
מילות מפתח: מולקולות חמצון תגובתיות, מתח חמצוני, מטבוליזם של סרטן, טיפול ברדוקס, מיקרוסביבה גידולית