Clear Sky Science · he
אנטיגן גרעיני חיצוני של נגיף אפשטיין–באר מעורר עמידות לגידול מונעת על ידי ADAR1 נגד אימונותרפיה
מדוע נגיף שכיח לרוב חשוב לטיפול בסרטן
רבים מסוגי הסרטן מטופלים כיום בתרופות אימונותרפיות המשחררות את מערכת החיסון של הגוף. עם זאת, רוב המטופלים עדיין אינם נהנים מהטיפול, כי הגידולים שלהם לומדים להסתיר עצמם מפני התקפה חיסונית. המחקר הזה חושף כיצד נגיף נפוץ מאוד, נגיף אפשטיין–באר (EBV), מסייע לגידולים לכבות את המערכות ההגנתיות החיסוניות ולהתנגד לתרופות החזקות הללו — וכיצד סוג חדש של מולקולה מתוכננת עשוי להדליק מחדש את אותן הגנות.
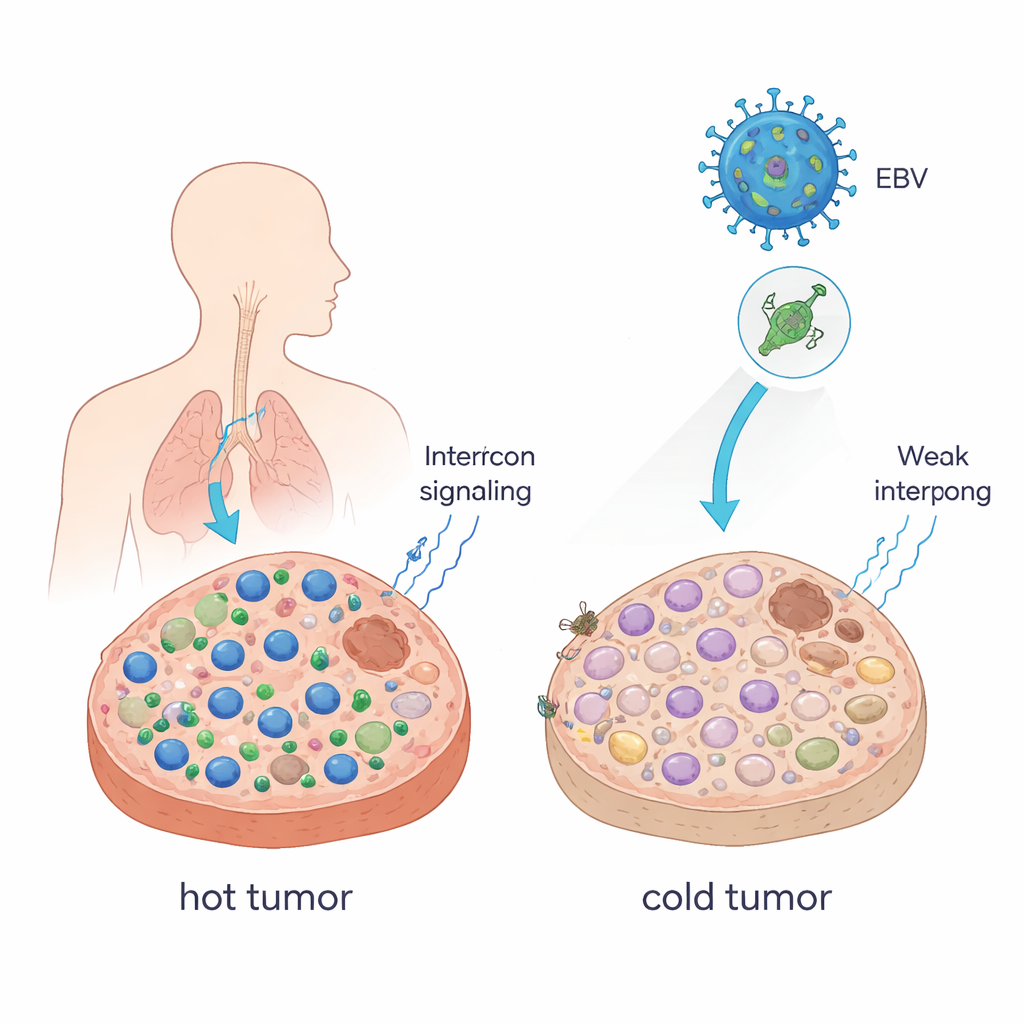
הפיכת גידולים חמים לקרים
רופאים מתארים לעתים גידולים כ"חמים" כאשר הם מלאים בתאי T ההורגים סרטן, וכ"קרים" כאשר תאים אלו נדירים. גידולים חמים בדרך כלל מגיבים היטב לחסימת נקודות ביקורת חיסוניות (ICB) כגון נוגדני אנטי–PD-1; גידולים קרים לעתים קרובות לא. הכותבים הראו שחלבון יחיד של EBV, הנקרא EBNA1, יכול לדחוף גידולים למצב קר יותר ומתחמק יותר. כאשר אילצו תאי גידול של עכבר להפיק EBNA1 וגדלו אותם בעכברים עם מערכת חיסון שלמה, הגידולים גדלו יותר, הכילו פחות תאי CD8+ ותאי הרג טבעי, והיו בהם יותר מאקרופאגים מדכאי חיסון. אותות הקרויים אינטרפרונים — שליחים מרכזיים שמגויסים לסייע לתאי החיסון — הופחתו באופן חזק. במדגמי חולים של קרצינומה של האף והלוע, סוג סרטן המקושר חזק ל-EBV, גידולים שהביעו EBNA1 הציגו בדומה פחות תאי CD8+ מאשר רקמה נורמלית.
קיצור דרך נגיפי למכונת הבקרה של RNA בתא
כדי להבין כיצד EBNA1 מעצב מחדש את מיקרו-הסביבה של הגידול, החוקרים חיפשו חלבונים אנושיים המתקשרים פיזית איתו. הם התרכזו בחלבון הנקרא IGF2BP3, הקורא סימנים כימיים קטנים (m6A) על מולקולות mRNA ויכול להגביר את יציבותן או את תרגומן לחלבון. EBNA1 התקשר בחוזקה ל-IGF2BP3 בכמה סוגי תאים, כולל תאי סרטן החיוביים ל-EBV. נתונים מתאי חולים הראו שרמות גבוהות של IGF2BP3 לוּו יחד עם פעילות גנים הקשורים לאינטרפרון מוחלשת וחדירת תאי CD8+ נמוכה יותר, מעלים חשד כי הברית בין הווירוס והמאחסן יכולה להחליש את החיסון נגד הגידול.
הגברה של עורך RNA שמשתיק אותות סכנה
ניתוח מעמיק הדגיש מטרה מרכזית של אינטראקציה זו: ADAR1, אנזים שמערך RNA דו-גדילי על ידי שינוי אותיות "A" מסוימות ל"I". עריכות אלו יכולות לגרום ל-RNA הדמוי-וירוס בתוך התאים להיראות פחות מסוכן לחיישנים פנימיים, ובכך להפחית תגובות אינטרפרון. המחברים מצאו כי EBNA1, IGF2BP3 ופקטור התרגום EIF4G1 יוצרים קומפלקס תלת-חלקי על mRNA של ADAR1. קומפלקס זה מגדיל סימון m6A, מגייס את מכונת התרגום ומגביה באופן סלקטיבי את ייצור חלבון ADAR1 בלי להעלות את רמות ה-RNA שלו. כתוצאה מכך, תאי הגידול מבצעים יותר עריכות RNA באלמנטים גנטיים חוזרים הנמצאים בסמוך לגנים הקשורים לאינטרפרון. עריכות אלו מצמצמות את מאגר ה-RNA הדו-גדילי הלא-ממותג שהיה מידי נוטה להתריע לחיישנים כגון MDA5 ו-PKR, ומחלישות את יצור האינטרפרון ועוזרות לגידולים להסתתר מפני התקפה חיסונית.
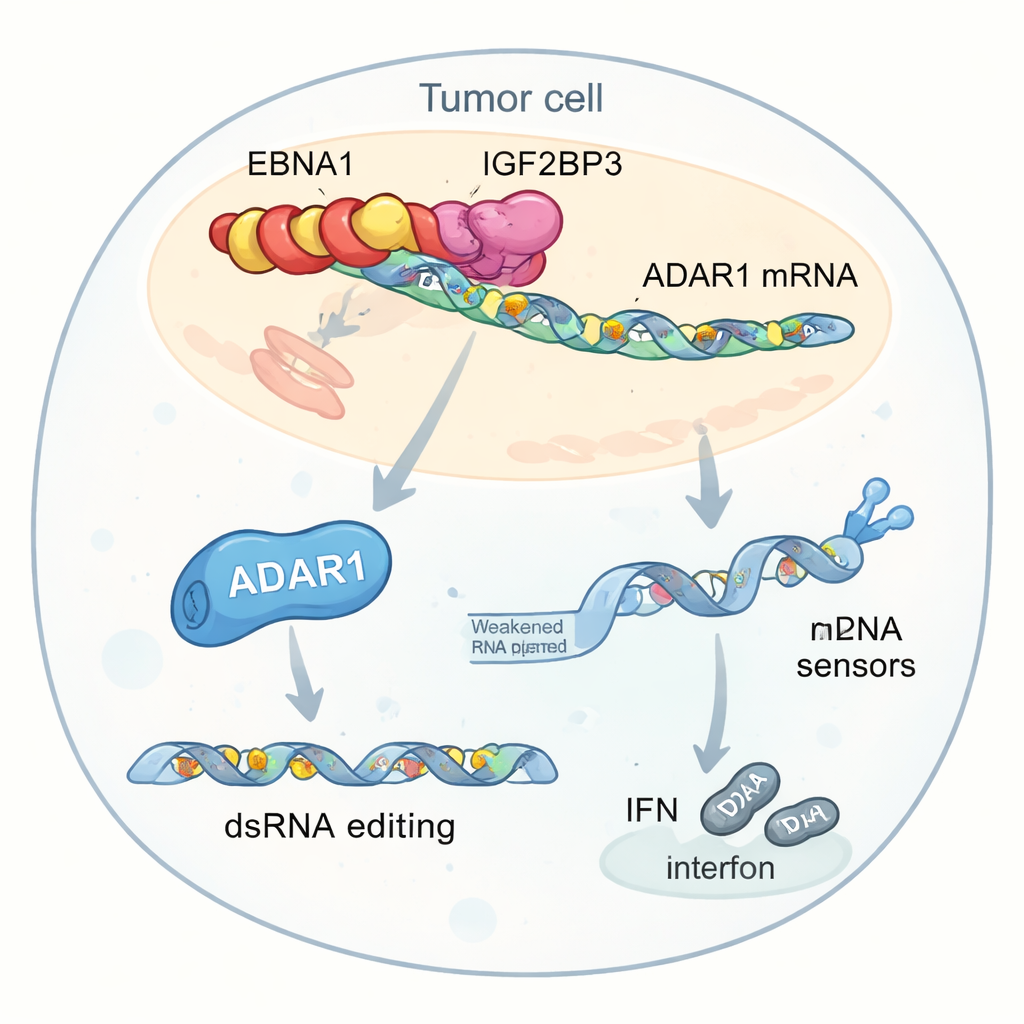
פחות אינטרפרון, אימונותרפיה חלשה יותר
כאשר תאי גידול שמביעים EBNA1 נחשפו לתאי T ולנוגדני אנטי–PD-1 במבחנה, הם היו קשים יותר להריגה ביחס לתאים ביקורת ושיחררו פחות אינטרפרון. גם כשהטיפו אותם ישירות באינטרפרון, התאים נושאי EBNA1 היו פחות רגישים וחיישני ה-RNA הפנימיים שלהם הופעלו פחות חזק. הורדת רמות ADAR1 ביטלה חלקית את ההשפעות הללו, שחזרה פעילות חיישנים ואיתות אינטרפרון. ניסויים גנטיים וריצוף אישרו כי תאים המביעים EBNA1 הראו יותר אירועי עריכת A-to-I באזורי RNA מסוימים, במיוחד לאחר גירוי באינטרפרון, וחיזק את הרעיון שהגברה ויראלית של ADAR1 מסייעת לנטרל אותות סכנה שהיו מעוררים תגובות חיסוניות חזקות.
מפחית מתוכנן שמעורר מחדש התקפה חיסונית
הצוות שאל האם הסרת EBNA1 מהגידולים תוכל להשיב את רגישותם לאימונותרפיה. הם תכננו מולקולת PROTAC, EP-1215, שמסמנת את EBNA1 להרס על ידי מערכת המיחזור של התא עצמו. במינונים נמוכים, EP-1215 פירק ביעילות את EBNA1 והפחית רמות חלבון ADAR1. בניסויי עכברים, טיפול ב-EP-1215 לבד השפיע במידה מוגבלת על גידולים חיוביים ל-EBNA1, וגם אנטי–PD-1 לבד היה חלש. אך בשילוב, שני הטיפולים הקטינו באופן חד את הגידולים, הגבירו חדירת תאי CD8+ והגבירו תאי T המייצרים אינטרפרון. במודלים של עכברים ממושרים שנשאו תאי חיסון אנושיים וגידולים קשורים ל-EBV, השילוב שוב עלה על הטיפולים הבודדים, ללא רעילות כבד או כליות בולטת.
מה משמעות הדבר עבור הטיפול בסרטן בעתיד
ללא מומחיות מיוחדת, המסר הוא שנגיף שכיח יכול בשקט לשכתב תאי סרטן כדי להחליש מערכות אזעקה פנימיות, ולכבות אותות כימיים שהיו מושכים ומפעילים תאי חיסון. EBNA1 עושה זאת על ידי חטיפת קורא RNA של המאחסן (IGF2BP3) ופקטור תרגום (EIF4G1) כדי לייצר עודף של עורך ה-RNA ADAR1, שמעריך את מבני ה-RNA שהחיישנים החיסוניים נועדו לזהות. על ידי פירוק EBNA1 עם PROTAC מתואם כמו EP-1215, המחברים הצליחו להשיב את אותות הסכנה הללו ולהפוך גידולים עמידים לרגישים שוב לתרופות נקודת הביקורת הקיימות. אם אסטרטגיות דומות יימצאו בטוחות ויעילות בבני אדם, תקיפת עוזרים ויראליים כגון EBNA1 עשויה להציע דרך חדשה להמיר גידולים קרים הקשורים ל-EBV ליעדים חמים שאימונותרפיות מודרניות יכולות סוף‑סוף לפגוע בהם.
ציטוט: Liu, C., Sun, Z., Li, C. et al. Exogenous Epstein–Barr virus nuclear antigen 1 induces ADAR1-driven tumor resistance against immunotherapy. Sig Transduct Target Ther 11, 63 (2026). https://doi.org/10.1038/s41392-026-02574-y
מילות מפתח: נגיף אפשטיין–באר, עמידות לאימונותרפיה, ADAR1, עריכת RNA, קרצינומה של האף והלוע