Clear Sky Science · he
PKC-אתה מקדם גרורות בסרטן השד על ידי ויסות מסלול האותות Hippo–YAP
מדוע מחקר זה חשוב
סרטן שד שלילי לשלושה סמנים (TNBC) הוא אחד הסוגים המסוכנים ביותר של סרטן השד, כי הוא מפיץ מוקדם וללא טיפולים ממוקדים. במחקר זה מתגלות הדרכים שבהן אנזים ספציפי בתוך תאי הסרטן, הנקרא PKC‑אתה (PKCη), פועל כמפסק ראשי שמסייע לגידולים להשתחרר, לנוע בגוף ולזרוע גידולים חדשים. באמצעות הבנת המפסק הזה, החוקרים גם מבודדים פפטיד טבעי קטן שיכול לכבות אותו — ואפשר שזה יוביל לגישה טיפולית חדשה למחלה אגרסיבית זו. 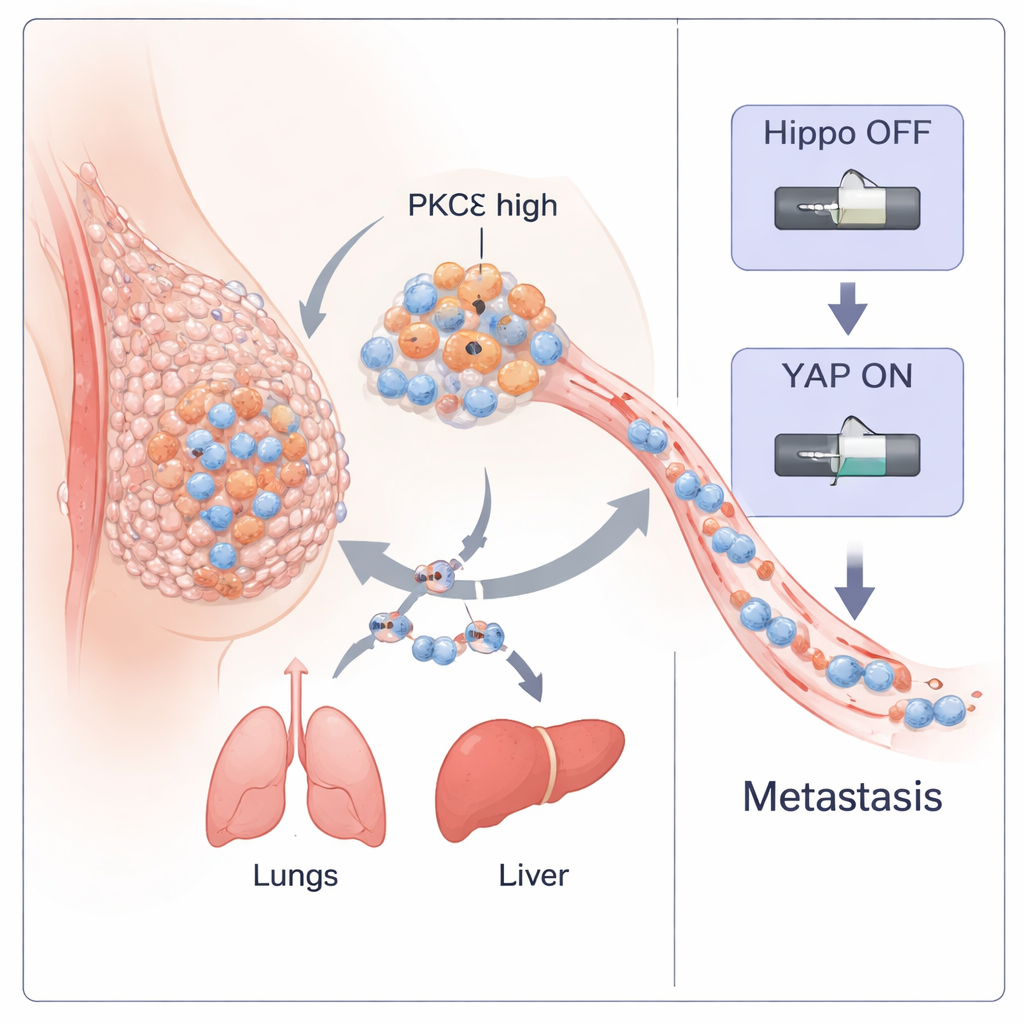
מניע סמוי בגידולים תוקפניים של השד
הצוות התחיל בחיפוש בבסדי נתונים גדולים של מטופלי סרטן שד. הם מצאו שהגן המקודד ל‑PKCη (PRKCH) גבוה במיוחד בסוג תאים הנקראים "claudin‑low", שמצטלב במידה רבה עם TNBC ושופע תאים דמויי־גזע בעלי תנועתיות גבוהה. ברשומות ממטופלי קבוצות שונות, גידולים עם ביטוי גבוה של PRKCH הציגו חתימות חזקות של המעבר האפיתלי‑מזנכימלי (EMT) — תהליך שבו תאים שסודרו בעבר משחררים את הקשרים שלהם, משנים צורה והופכים ליותר פולשניים. רמות PRKCH היו גם גבוהות יותר במדגמי גרורות מאשר בגידולים הראשוניים המקוריים, וצביעת חלבון ברקמות TNBC אנושיות הראתה PKCη פעיל, סביב גרעיני, בגידולים בדרגות גבוהות ומתקדמות. יחד, ממצאים אלה הציעו כי PKCη קשור קשר הדוק לאגרסיביות ולפיזור הגידול.
מצלחת המעבדה לעכבר: הוכחה ש‑PKCη מזין פיזור
כדי לבדוק סיבתיות, החוקרים השתמשו בעריכת גנים CRISPR להסרת PKCη משתי שורות תאים TNBC בעלות תאוצת גרורתיות גבוהה, אחת של עכבר (4T1) ואחת אנושית (MDA‑MB‑231). בלעדיו התאים נטו למצב "אפיתלי" יותר: חלה עלייה בחלבוני הדבק כגון E‑cadherin ו‑EpCAM, וירידה בסמנים המזנכימליים הקלאסיים כמו וימנטין ו‑N‑cadherin. תאים חסרי PKCη יצרו פחות מושבות וקטנות יותר, נדדו ופולשו פחות ביעילות, היו רגישים יותר למוות תאי כשהם מנותקים והראו ירידה חדה בתכונות תאי גזע סרטניים, כולל פחות תאים CD44high/CD24low ו‑ALDH‑חיוביים וקיבולת יצירת כדורים מופחתת. בעת הזרקה לעכברים, תאים חסרי PKCη יצרו גידולים ראשוניים קטנים בהרבה ומעט מאוד גרורות לריאות, כבד, מוח ואיברים אחרים; העכברים גם שרדו זמן ארוך יותר. השבת PKCη הפכה את השינויים האלה, ואישרה כי האנזים מקדם באופן פעיל את ההתקדמות והפיזור של TNBC.
כיצד PKCη חוטף מסלול בקרה על גדילה
המחקר התמקד לאחר מכן באופן שבו PKCη מפעיל את כוחו המקדם‑גרורתיות. נתוני מטופלים הראו שרמות PKCη עלו וירדו יחד עם YAP, חלבון מתג חזק הנשלט על ידי מסלול Hippo — "בלם הבטיחות" התאי שמאופיין בעיכוב גדילה. רמות גבוהות של PRKCH או של YAP1 חזו תוצאות גרועות יותר למטופלים, ורמות גבוהות של שניהם יחד נקשרו להישרדות חופשית מגרורות מרוחקות נמוכה במיוחד. בתאי TNBC, הסרת PKCη הורידה את רמות YAP הכוללות והעבירה אותו מהגרעין לציטופלזמה, שם הוא אינו פעיל. ניסויים ביוכימיים הראו ש‑PKCη נקשר פיזית ל‑YAP ומוסיף ספציפית תג פוספט באתר Ser128. שינוי זה מייצב את YAP ועוזר לו להיכנס לגרעין ולהדליק גנים שמקדמים EMT, תכונות גזע וגרורתיות. בהיעדר PKCη, YAP מסומן במקום זאת באתרים אחרים (Ser127 ו‑Ser397) שגורמים לו להיקשר לחלבוני 14‑3‑3, להיתפס בציטופלזמה ולפגוע בו עד לפירוק. בנוסף, PKCη משנה את PTEN — מעצור טבעי על האנזים AKT — ובכך שומרת על פעילות AKT נמוכה ודוחקת מטה את קינאזות ה‑Hippo שמנעות בדרך כלל מפעילות YAP. כך PKCη מפעילה ישירות את YAP ובמקביל מונעת בעקיפין את פעולת הבלם של Hippo. 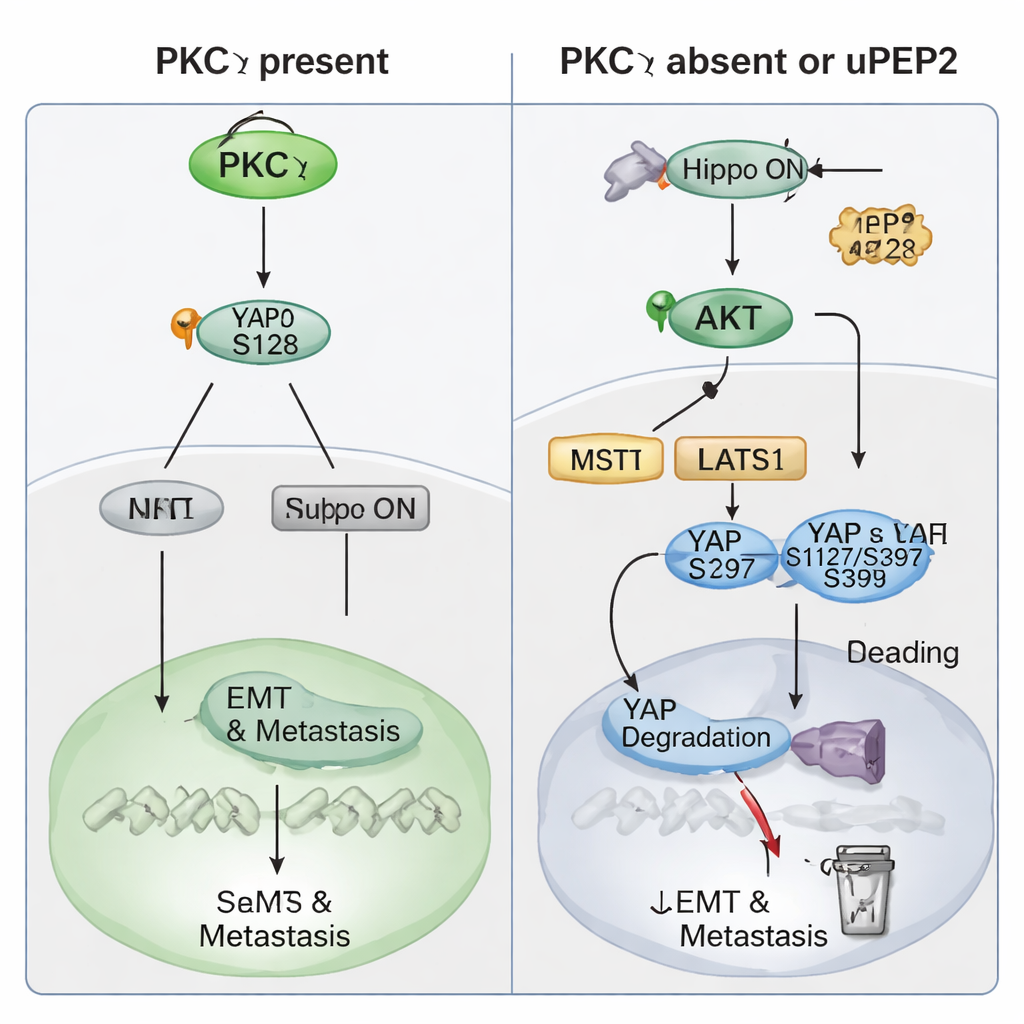
פפטיד זעיר שמנטרל את מפסק הסרטן
באופן מעניין, לגן PKCη יש קוד פתוח קצר מקדמי (uORF) המקודד למיקרופפטיד הנקרא uPEP2. עבודה קודמת הראתה ש‑uPEP2 יכול להיקשר ולחסום את PKCη ואת אנזימים קשורים. כאן, טיפול של תאי TNBC ב‑uPEP2 סינתטי חיקה את השפעות כריתת PKCη: נצפו ירידות בנדידה, בפלישה ובהתנהגות דמויית‑גזע, סמני EMT הוסטו לפרופיל פחות אגרסיבי, ורמות YAP ירדו בעוד שסימני הפוספורילציה שמכבים אותו עלו. בגידולים בעכברים, uPEP2 הפחית PKCη ו‑YAP בגידולים הראשוניים, הגדיל את כיבוי YAP ונקשר עם פחות מיקרו‑גרורות בכבד ובריאות. מבחינה מנגנונית, uPEP2 מקדם פירוק של PKCη, משיב את מסלול Hippo לפעולה ודוחף את YAP להישאר בציטופלזמה ולהתפרק.
מה משמעות הדבר עבור טיפולים עתידיים
לקריאה לא מקצועית, המסר המרכזי הוא שהחוקרים זיהו את PKCη כציר המאפשר לסוגי סרטן השד האגרסיביים ביותר להשתחרר, לנוע ולתפוס איברים מרוחקים על‑ידי השתקת מערכת בקרה טבעית על הגדילה והפעלה של "דוושת הגז" YAP. על‑ידי השמדת PKCη או שימוש בפפטיד טבעי קטן uPEP2 כדי לפרקו, הם הצליחו לשחזר את בלם הבטיחות של Hippo, לשתק את YAP ולהפחית במידה ניכרת גרורתיות במודלים פרה־קליניים. למרות שעבודה זו עדיין בשלבי ניסוי ונערכה בשורות תאים ובעכברים חסרי מערכת חיסון, היא מציינת את PKCη ואת האינטראקציה שלו עם YAP כמטרות מבטיחות לטיפולים חדשים ב‑TNBC, ומציעה שתרופות בסגנון uPEP2 עשויות יום אחד לסייע למנוע או להגביל את התפשטות הסרטן הקשה לטיפול הזה.
ציטוט: Liju, V.B., Waidha, K., Muraleedharan, A. et al. PKC-eta promotes breast cancer metastasis by regulating the Hippo–YAP signaling pathway. Sig Transduct Target Ther 11, 58 (2026). https://doi.org/10.1038/s41392-026-02572-0
מילות מפתח: סרטן שד שלילי לשלושה סמנים, PKC-אתה, מסלול Hippo-YAP, המעבר האפיתלי‑מזנכימלי, גרורתיות סרטנית