Clear Sky Science · he
Serpina3c מגן מפני מחלת כבד שומנית הקשורה להפרעה מטבולית בעובר שנגרמה מחשיפה פרה‑ניטלית לפרדניזון
מדוע המחקר הזה חשוב לילדים בעתיד
נשים רבות זקוקות לפרדניזון במהלך ההיריון כדי לשלוט במחלות אוטואימוניות ודלקתיות חמורות. רופאים יודעים שהוא יכול להציל חיים של אימהות, אך ידוע הרבה פחות כיצד הוא מעצב את הבריאות לטווח הארוך של ילדיהן. המחקר הזה בוחן שאלה דחופה: האם נטילת פרדניזון במהלך ההיריון עלולה לשנות באופן שקט את הכבד של הילד, כך שהילד יפתח מחלת כבד שומנית בהמשך החיים, במיוחד בשילוב עם תזונה בלתי‑בריאה? ואם כן, האם אפשר להפחית או להפוך את הסיכון הזה?
בעיה כבדית הולכת וגדלה בעולם
מחלת כבד שומנית הקשורה להפרעה מטבולית (MASLD) היא כיום אחת מהמחלות הכרוניות של הכבד השכיחות ביותר, משפיעה על בערך שליש מהאוכלוסייה העולמית וצפויה לגדול עוד. היא כוללת הצטברות שומן פשוטה בכבד, ‘‘הפטיטיס שומנית’’ מדלקתית, צלקות, שחמת ואף סרטן הכבד. MASLD קשורה באופן חזק להשמנת יתר, לחץ דם גבוה וסוכרת סוג 2. מדענים מבינים יותר ויותר שהזרעים למחלה זו עשויים להימזר עוד לפני הלידה, כאשר העובר המתפתח נחשף ללחצים כמו תזונה לקויה, זיהום סביבתי או תרופות. הרעיון הזה — שהסביבה המוקדמת בחיים מעצבת את סיכון המחלה לכל החיים — מוכר כ׳מקורות ההתפתחות של הבריאות והמחלה׳.
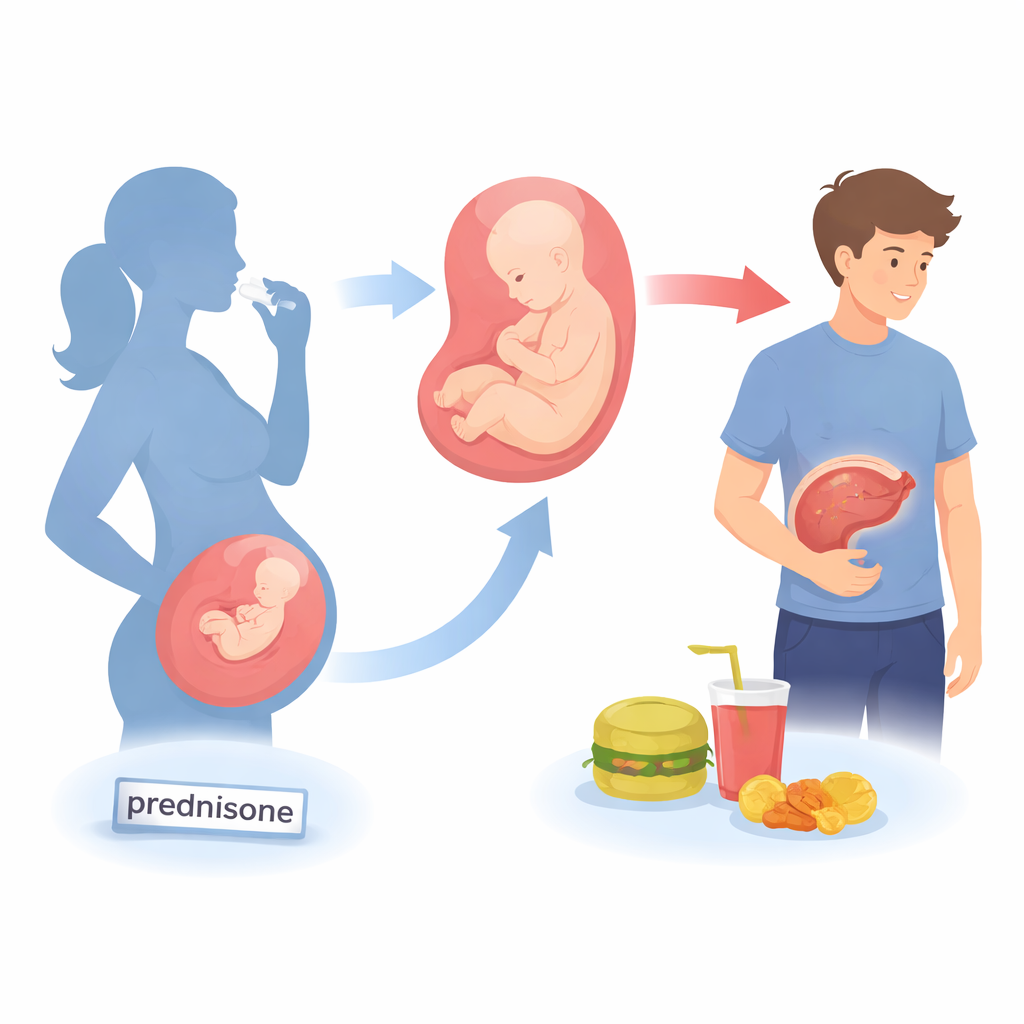
פרדניזון לפני הלידה כ״מכה ראשונה״
כדי לבדוק כיצד פרדניזון פרה‑ניטלי משפיע על הכבד, החוקרים טיפלו בעכברים וחולדות בהריון במינונים שנבחרו כדי לדמות מינונים קליניים נמוכים בבני אדם. לאחר מכן הם עקבו אחרי הצאצאים עוד מטרום הלידה ועד לבגרות צעירה. בעצמם, בעלי החיים הצעירים שנחשפו לפרדניזון ברחם היו קטנים יותר וכבר הראו סימנים של טיפול שומנים לא תקין בכבד: טיפות שומן רבות יותר, רמות טריגליצרידים גבוהות יותר בכבד ושימוש חלש יותר בשומנים לאנרגיה. כאשר הצאצאים גדלו, כבדיהם המשיכו לאגור שומן באופן מוגבר גם בתזונה רגילה. כאשר בעלי החיים הוצבו מאוחר יותר לתזונה עתירת שומן — המקבילה לדפוס המזון המערבי מהיר־הסעד — ההבדלים הפכו לדרמטיים. הצאצאים שנחשפו לפרדניזון פיתחו כבד שומני חמור יותר, דלקת ובמינים זכריים אף סימני צלקת ברורים. גם בקרה על רמות הסוכר בדם שלהם נפגעה, מה שמעיד על בעיה מטבולית רחבה יותר.
חלבון מגן של הכבד נעלם
בהסתכלות מעמיקה יותר, הצוות השתמש בפרופיל גנים רחב היקף כדי לחפש שינויים מולקולריים משותפים בכבד של צאצאים זכרים ונקבות. גן אחד בלט: Serpina3c, שמקודד לחלבון מופרש המשויך למשפחת מעכבי אנזימים טבעיים. בשני המינים, חשיפה פרה‑ניטלית לפרדניזון הפחיתה בחדות ובאופן מתמשך את Serpina3c בכבד ובזרם הדם, מאחריות עוברית מאוחרת ועד לבגרות. כאשר החוקרים הורידו במכוון את רמת Serpina3c רק בכבד של עכברים בריאים, גם הם הפכו לרגישים לכבד שומני ולחוסר איזון בסוכר, במיוחד בתזונה עתירת שומן. לעומת זאת, חיזוק רמות Serpina3c בכבדם של צאצאים שנחשפו לפרדניזון אחרי הלידה הציל ברובו את המצב: כבדיהם אגרו פחות שומן, טיפלו טוב יותר בגלוקוז והראו פחות דלקת וצלקת.
כיצד פרדניזון מתכנת מחדש את מתגי הבקרה של הכבד
השאלה הבאה של החוקרים הייתה כיצד פרדניזון פרה‑ניטלי מדכא את Serpina3c. הם מצאו שהצורה הפעילה של פרדניזון, פרדניזולון, מגרה יתר על המידה את קולטן הגלוקוקורטיקואידים — חלבון חיישן‑תרופות המצוי בתאי הכבד. קולטן זה שותף אז לחלבון נוסף, HDAC3, שמקשיח את אריזת ה‑DNA על ידי הסרת תגיות אצטיל קטנות מהיסטונים. הן בכבד של בעלי החיים והן בתאי כבד בתרבית, פרדניזולון הגביר פעילות של קולטן הגלוקוקורטיקואידים ושל HDAC3 דווקא באזור גן Serpina3c, והסיר תגי אצטיל באתר מפתח הנקרא H3K27. עם הסרת תגיות אלה ירדה פעילות הגן ורמות חלבון Serpina3c פחתו. חסימת הקולטן או HDAC3, או עיכוב הדה‑אצטילציה, שיקמה את תגי האצטיל, העלתה את Serpina3c ושיפרה טיפול בשומנים וסוכרים בתאי הכבד.
שרשרת תגובה מזיקה בתוך הכבד
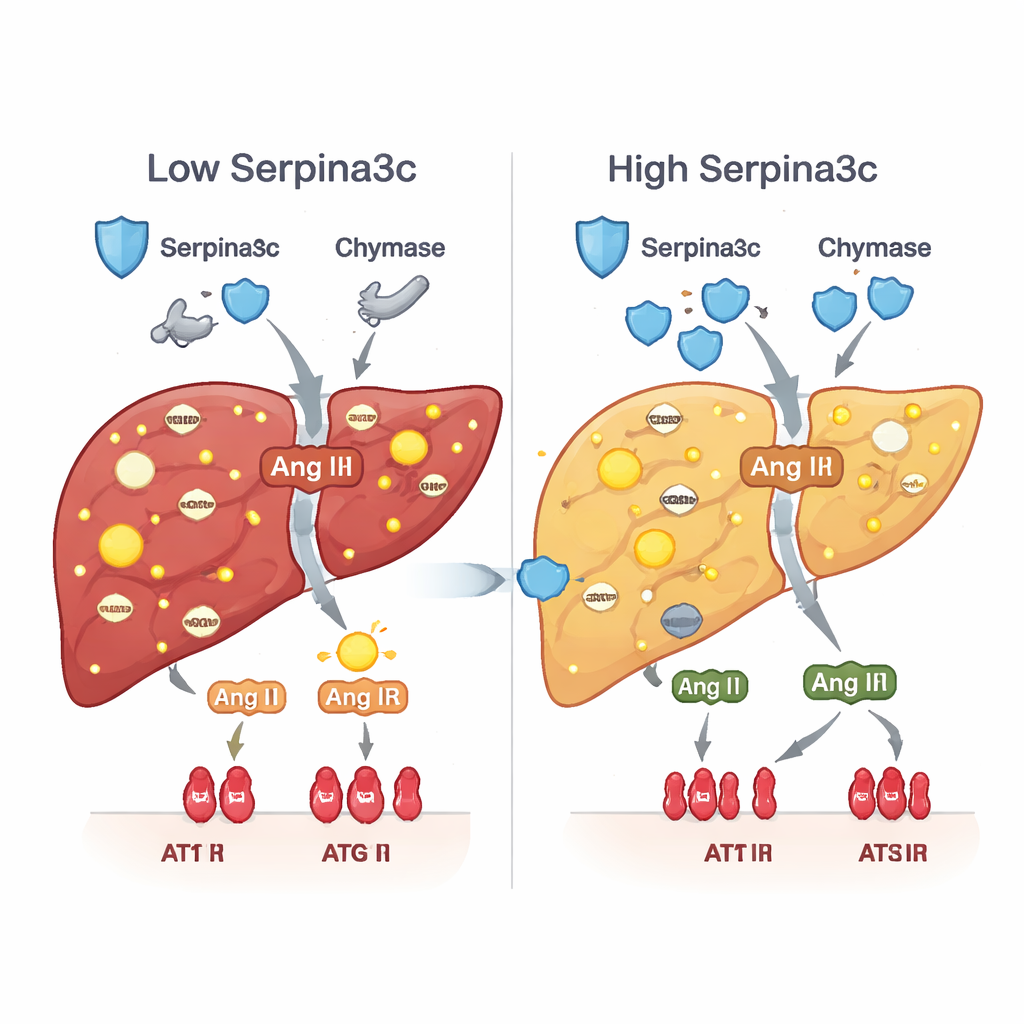
רמות Serpina3c הנמוכות הציתו מפל מים של נזקים נוספים. בתנאים נורמליים Serpina3c מסייעת לרסן אנזימים כמו כימאז שמייצרים את ההורמון אנגיוטנסין II ישירות ברקמות. כאשר Serpina3c הייתה בקופסה, רמות וכושר הפעולה של כימאז עלו, מה שהוליד עוד אנגיוטנסין II בכבד והפעיל יתר על המידה את הקולטן שלו, AT1R, בתאי הכבד. גל הורמונים מקומי זה ידוע כמניע מתח חמצוני, עמידות לאינסולין, הצטברות שומן, דלקת וצלקת. הן בבעלי החיים החשופים לפרדניזון והן בעכברים עם הדחקה ספציפית של Serpina3c בכבד, מסלול הכימאז–אנגיוטנסין II–AT1R הופעל, וגנים מרכזיים שתומכים בשריפת שומן ובקליטת גלוקוז דוכאו. שיקום Serpina3c אחרי הלידה השקט את המסלול הזה ושיקם מטבוליזם בריא יותר.
מה זה אומר עבור מטופלים ומשפחות
ללא מומחיות מיוחדת, המסר המרכזי הוא שתרופות הנצרכות במהלך ההיריון יכולות להותיר טביעת אצבע מולקולרית על כבד העובר שנמשכת עד הבגרות. במחקר זה, פרדניזון פעל כ״מכה ראשונה״, הוריד חלבון מגן (Serpina3c) באמצעות שינויים אפיגנטיים — סימנים כימיים על חלבוני אריזת ה‑DNA — כך ש״מכה שנייה״ מאוחרת יותר, כמו תזונה עתירת שומן, עוד יותר הקלה על הופעת מחלת הכבד השומנית. הצד המעודד הוא שהסיכון הזה לא היה קבוע: החזרת Serpina3c בכבד אחרי הלידה הקטינה באופן משמעותי את נזקי הכבד. למרות שהתוצאות הן ממודלים של מכרסמים, הן מעלות שאלות חשובות לגבי האופן שבו נעקוב ותומכים בילדים שאמם נזקקה לפרדניזון בהיריון, ומצביעות על Serpina3c ומערכת הכימאז–אנגיוטנסין II כיעדים מבטיחים למניעה או טיפול במחלת כבד שומנית שמקורה לפני הלידה.
ציטוט: Dai, Y., Lu, Z., Peng, Y. et al. Serpina3c protects against metabolic dysfunction-associated steatotic liver disease in offspring induced by prenatal prednisone exposure. Sig Transduct Target Ther 11, 71 (2026). https://doi.org/10.1038/s41392-025-02569-1
מילות מפתח: פרדניזון פרה‑ניטלי, מחלת כבד שומנית, אפיגנטיקה, Serpina3c, מקורות התפתחותיים