Clear Sky Science · he
גילוי ופיתוח תרופות אנטי‑ויראליות: אתגרים וכיווני עתיד
מדוע אנחנו עדיין זקוקים לתרופות טובות יותר נגד וירוסים
מגפת COVID‑19 הראתה כמה מהר וירוס חדש יכול להפוך את חיי היומיום — וכמה אנו עדיין תלויים בתרופות טובות כאשר חיסונים אינם מספיקים. מאמר הביקורת הזה מסתכל לאחור על יותר מ‑60 שנות פיתוח תרופות אנטי‑ויראליות ושואל: איך נוכל לבנות הגנות מהירות, חכמות ורחבות יותר נגד איומי וירוסים עתידיים? הוא מסביר, במונחים ברורים ונגישים, איך חוקרים מגלים, מעצבים ומנגישים תרופות אנטי‑ויראליות, מה למדו מ‑COVID‑19 ואיך כלים כמו בינה מלאכותית וננו‑טכנולוגיה עשויים לשנות את המשחק.
מהאנטי‑ויראליים הראשונים ועד ארסנל של ימינו
תרופות אנטי‑ויראליות הן תחום יחסית צעיר. התרופה הראשונה שאושרה, אידוקסירידין בשנות ה‑60, הראתה שהשינוי בבלוקים הבניין של ה‑DNA יכול להאט שכפול ויראלי, אך גם פגע בתאים בריאים ולכן נאלצה לשמש רק לעיניים. לאחר מכן הגיע אציקלוויר, תרופה פורצת דרך נגד הרפס שמופעלת בעיקר בתוך תאים נגועים, מה שהפך אותה גם לעוצמתית וגם לבטוחה. בשנות ה‑80, זידובודין הפכה לטיפול הראשון ב‑HIV, ופתחה את הדלת לתרופות משולבות מודרניות שהפכו את ה‑HIV למצב כרוני ניתן לניהול. במשך עשורים, כימיה משופרת ועיצוב בעזרת מחשב סייעו להביא תרופות מדויקות יותר נגד שפעת, הפטיטיס B ו‑C, HIV, ולבסוף SARS‑CoV‑2. הסקירה עוקבת אחרי קו הזמן הזה ומציגה כיצד כל פריצת דרך הציגה דרך חדשה להקדים את הוירוסים.
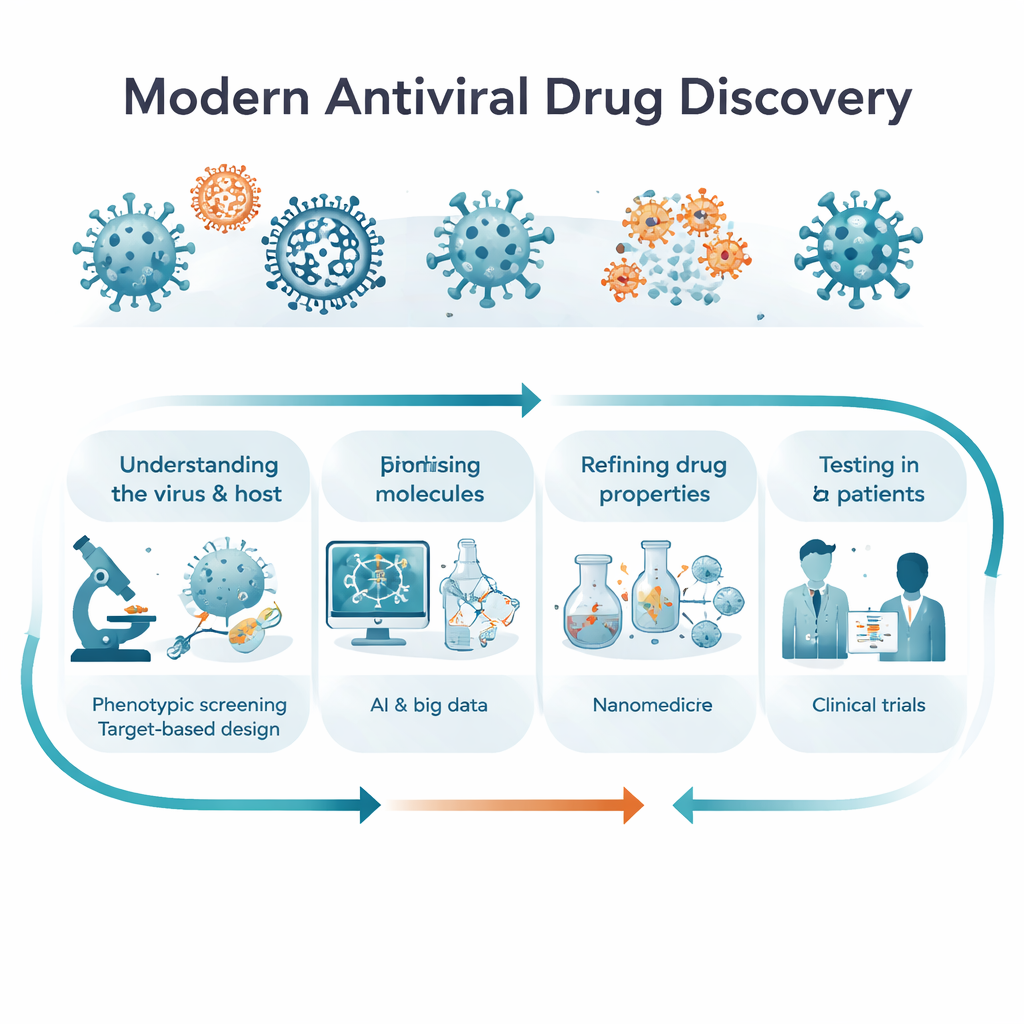
שתי דרכים למצוא תרופה טובה: לצפות בתאים מול לכוון מטרות
חוקרים בדרך כלל הולכים בשני מסלולים משלימים לגילוי אנטי‑ויראליים חדשים. בגילוי "פנוטיפי" הם לא מתחילים עם חלבון ספציפי; במקום זאת הם חושפים תאים נגועים או אורגניזמים דוגמיים לאלפים של מולקולות ושואלים פשוט: אילו מהן שומרות על הוירוס תחת שליטה ועל התא חי? גישה זו יכולה לחשוף תרופות מפתיעות, חד‑פעמיות, כולל כאלה הפועלות על יותר ממסלול אחד. בגילוי "ממוקד‑מטרה", המדענים מזהים תחילה חלבון ויראלי או חלבון מארח החיוני לזיהום — כגון פולימראז, פרוטאז או אות חיסוני — ואז מעצבים מולקולות החוסמות או מכוונות מטרה זו. המאמר מסביר כיצד אסטרטגיות אלה שונות, מדוע כל אחת חשובה בשלבים שונים של המחקר, ואיך פרויקטים עתידיים צפויים לשלב ביניהן, לעבור בקלות מתצפית רחבה להבנה מולקולרית מדויקת.
להכות בוירוס — ובמערכת התומכת שלו — במקום שגורם לו נזק
אנטי‑ויראליים מודרניים עושים הרבה מעבר לחסימת אנזים ויראלי יחיד. הסקירה מסבירה את מעגל החיים הויראלי, מחדירתו לתא ועד שכפול הגנום ושחרור, ומציינת סוגי תרופות המתערבות בכל שלב. חלק מהתרכובות נקשרות ישירות לאנזימים ויראליים או לחלבונים מבניים. אחרות פועלות על ידי כיוונון גורמים של המארח שהוירוסים תלויים בהם — כמו קולטני פני התא, אנזימי מטבוליזם מרכזיים או מסלולים של החסינות המולדת כגון אינטרפרונים וקולטני toll‑like. על‑ידי פעולה על חלבוני עזר של המארח, תרופות אלה יכולות להקטין את הסיכוי שוירוס המשתנה במהירות יברח מחסימה. המחברים מתארים גם רעיונות עולים כגון מולקולות קטנות המפרקות "טיפות" ללא ממברנה בתוך התאים שבהן הוירוסים מורכבים, או שמביאות לפירוק סלקטיבי של חלבונים ו‑RNA ויראליים במקום רק לחסום אותם.
עיצוב מולקולות טובות יותר: צורה, תכונות וממסר
הפיכת "היי‑ט" ראשוני לתרופה שימושית פירושה יותר מאשר מקסום העוצמה. כימאים מכוונים את הצורה והמטען של מולקולות כדי שהן יתאימו למטרותיהן כמו מפתחות במנעולים, לעתים בהנחיית מבני חלבון ברזולוציה גבוהה וסימולציות. הם גם משנים את מסיסות במים, יציבות וחילוף חומרים כדי להבטיח שהתרופה תגיע לרקמה הנכונה, תישאר פעילה מספיק זמן ותמנע רעילות מיותרת. המאמר נותן דוגמאות לאיך שינויים קטנים — כמו הוספת שרשרת צדדית או יצירת מלח — יכולים להגביר פעילות נגד זני HIV או קורונה עמידים תוך שיפור הבטיחות. הוא גם מסביר פרודרוגים, צורות לא פעילות או פחות פעילות שמתוכננות להיות מוסבות בתוך הגוף, ומערכות הובלה ממוקדות כגון תגים סוכריים הפונים לכבד וננומחיות שומניות שנושאות בבטחה mRNA או תרופות חומצות גרעין עדינות לתאים.
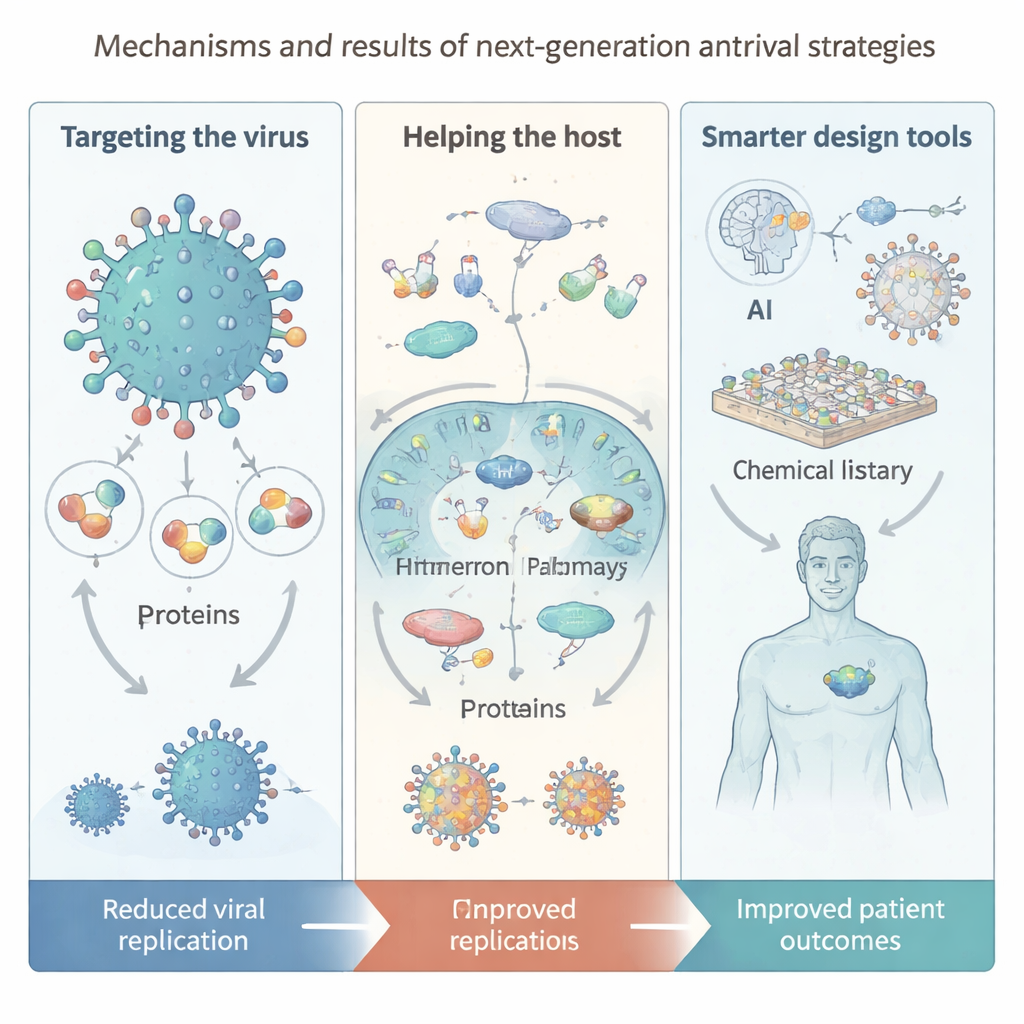
כלים חדשים: בינה מלאכותית, ספריות ענק וננו‑טכנולוגיה
נושא מרכזי בסקירה הוא איך הטכנולוגיה מעצבת מחדש את גילוי האנטי‑ויראליים. בינה מלאכותית עוזרת כיום לחזות מבני חלבון, לחפש ספריות "ווירטואליות" עצומות המכילות מיליארדי מולקולות אפשריות, ולהציע תרכובות חדשות או שילובי תרופות. ספריות מקודדות ב‑DNA ופלטפורמות פפטידיות מקרוציקליות מאפשרות סינון מהיר במיוחד של מרחבי כימיה ענקיים, בעוד מערכות סינתזה וטיהור אוטומטיות מאיצות את לולאת הבנייה‑והבדיקה. מצד ההעברה, ננו‑טכנולוגיה מספקת חלקיקים דמויי וירוס, פולימרים חכמים ו"ננו‑זימים" היכולים לפגוע ישירות בציפוי הוירוס או לחדד תגובות חיסוניות. עם זאת, המחברים מזהירים שמודלים של בינה מלאכותית עדיין תלויים בנתונים איכותיים, שרבות מהמולקולות שנוצרו קשות להכנה או לבדיקה, ושיש לטפל בנושאי בטיחות, הוגנות ופרטיות ככלים אלה הופכים מרכזיים יותר.
לאן הולך גילוי תרופות אנטי‑ויראליות
לקורא שאינו מומחה, המסר המרכזי של המאמר הוא גם מצנן וגם מעודד. וירוסים משתנים במהירות, ואף גלולה אחת לא תעבוד לנצח או נגד כל איום. אבל על‑ידי למידה מ‑COVID‑19, העמקת ההבנה של אינטראקציות וירוס–מארח ושילוב כימיה חכמה, ביולוגיה מתקדמת, בינה מלאכותית וננו‑טכנולוגיה, המדענים בונים ארגז כלים אנטי‑ויראלי גמיש יותר. טיפולים עתידיים צפויים להיות רחבי היקף יותר, סובלים טוב יותר ומתואמים לבחינת "נקודות התורפה" בתהליך ההדבקה, לא רק בוירוס עצמו. המשך שיתוף פעולה בין דיסציפלינות, תעשיות ומדינות יהיה חיוני כדי להפוך את ההתקדמויות המדעיות הללו לתרופות נגישות, מעשיות וזולות לפני שתגיע המגפה הבאה.
ציטוט: Du, S., Hu, X., Li, P. et al. Antiviral drug discovery and development: challenges and future directions. Sig Transduct Target Ther 11, 69 (2026). https://doi.org/10.1038/s41392-025-02539-7
מילות מפתח: גילוי תרופות אנטי‑ויראליות, תרופות ל‑COVID-19, תרופות אנטי‑ויראליות הממוקדות במארח, בינה מלאכותית בעיצוב תרופות, ננו‑טכנולוגיה ברפואה