Clear Sky Science · he
תאי CD4 ציטוטוקסיים: מוצא, פונקציות ביולוגיות, מחלות ומטרות טיפוליות
כשהתאים המסייעים הופכים לרוצחים
מערכת החיסון מוצגת לרוב בתפקידים פשוטים: חלק מהתאים מזהים את הבעיה, אחרים מנהלים את המאבק עצמו. המאמר מתמקד בקבוצה מפתיעה שמטשטשת את הגבול הזה — תאי CD4 ציטוטוקסיים. ידועים זמן רב בעיקר כ»תאי עזר« שמאחדים תגובות חיסוניות, אך תת-אוכלוסייה מסוימת של תאי CD4 יכולה להפוך בעצמה לתאים חמושים בעלי יכולת הרג. הבנת האופן שבו נוצרים תאים משני-צורה אלה, מה תפקידם ואיך הם תורמים למחלות כגון סרטן, זיהומים ויראליים, הפרעות אוטואימוניות ומחלות לב עשויה לפתוח דרכים חדשות הן להגברת החיסון והן להרגעת דלקת מזיקה. 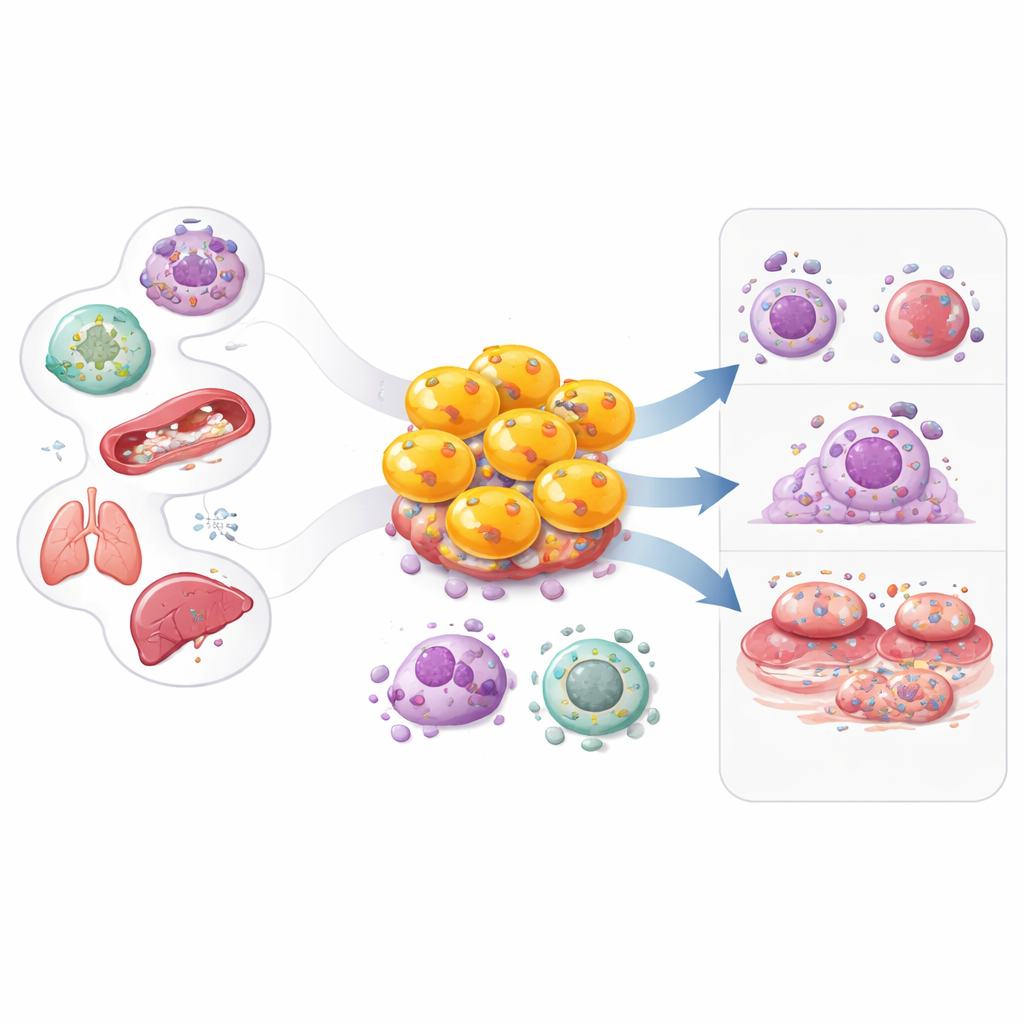
כיצד התגבש מגנן גמיש
עבודות ראשוניות בסוף שנות ה-70 וה-80 הראו כי חלק מתאי CD4 יכולים להרוג ישירות תאים המציגים סימני חיסון מתאימים, בדומה לתאי CD8 הקלאסיים. בתחילה נטו מדענים רבים לדחות ממצאים אלה כהשערות הנובעות מתנאי מעבדה. בעשורים שלאחר מכן, מודלים בעכברים של שפעת ומחקרים באנשים עם דלקת מפרקים שגרונית, מחלת לב, זיהומים ויראליים כרוניים וסרטן איששו שתאי CD4 ציטוטוקסיים קיימים ובעלי חשיבות קלינית. כלים מודרניים כמו ציטומטריה בזרם וריצוף RNA של תא יחיד מיפו מאז את המגוון שלהם, והראו שתאים אלה מתרחבים בזיהומים כרוניים, בגידולים, בהזדקנות ובכמה מחלות דלקתיות, שם הם יכולים להתמיד למשכי זמן ארוכים.
מאיפה באים אותם עזרי-רוצחים
הסקירה מסבירה שתאי CD4 ציטוטוקסיים נוטים להיווצר בשתי דרכים עיקריות. רעיון אחד טוען שהם דומים במידה מסוימת לתאי הרוצח הטבעיים (NK) שכן הם חולקים הרבה קולטנים על-גבי הממברנה ומולקולות ציטוטוקסיות, מה שמעיד על מסלול התפתחותי קשור. עם זאת, ראיות מצטברות תומכות בעמדה אחרת: רוב התאים האלה מתחילים כתאי עזר CD4 רגילים — במיוחד תתי-סוגים בדמיון ל-Th1 — ותחת חשיפה כרונית לאנטיגן ואותות דלקת חזקים הם »משחזרים עצמם« למצב ציטוטוקסי מפורט סופי. המעבר הזה נשלט על ידי רשת של גירויים חיצוניים (כגון אינטרלוקינים 2, 7 ו-15) ומתגים פנימיים (כולל Runx3, T-bet, Eomes, Blimp-1 ו-Hobit) אשר יחד מדליקים גנים בקוד לפורפורין, גרנזימים ולליגנדים המפעילים מוות.
איך הם הורגים ומעצבם דלקת
תפקודית, תאי CD4 ציטוטוקסיים פועלים בשני נתיבי תקיפה עיקריים. בנתיב הגרנולות הם יוצרים מגע הדוק עם תא המטרה ומשחררים מנות המכילות פרפורין וגרנזימים, שמחורר אותן ומפעילים מוות מוקצב מתוכו. בנתיב ליגנדי המוות הם מציגים מולקולות על פני השטח כגון Fas ligand ו-TRAIL, שמתקשרות לקולטנים תואמים על תאי המטרה ומפעילות תוכנית התאבדות פנימית. מעבר להרחה ישירה, תאים אלה מפרישים מסרים דלקתיים כמו אינטרפרון-גאמא, גורם נמק גידול וצמיחה שמגייסים ומפעילים תאים אחרים, מעצבים כלי דם ומשנים את התנהגות הרקמה המקומית. שלא כמו העזרים הקלאסיים, לעיתים קרובות הם עמידים ל»בלמים« רגולטוריים כמו תאי T רגולטוריים ופחות נוטים לאפוטוזה, מה שמאפשר הצטברות במחלות כרוניות. 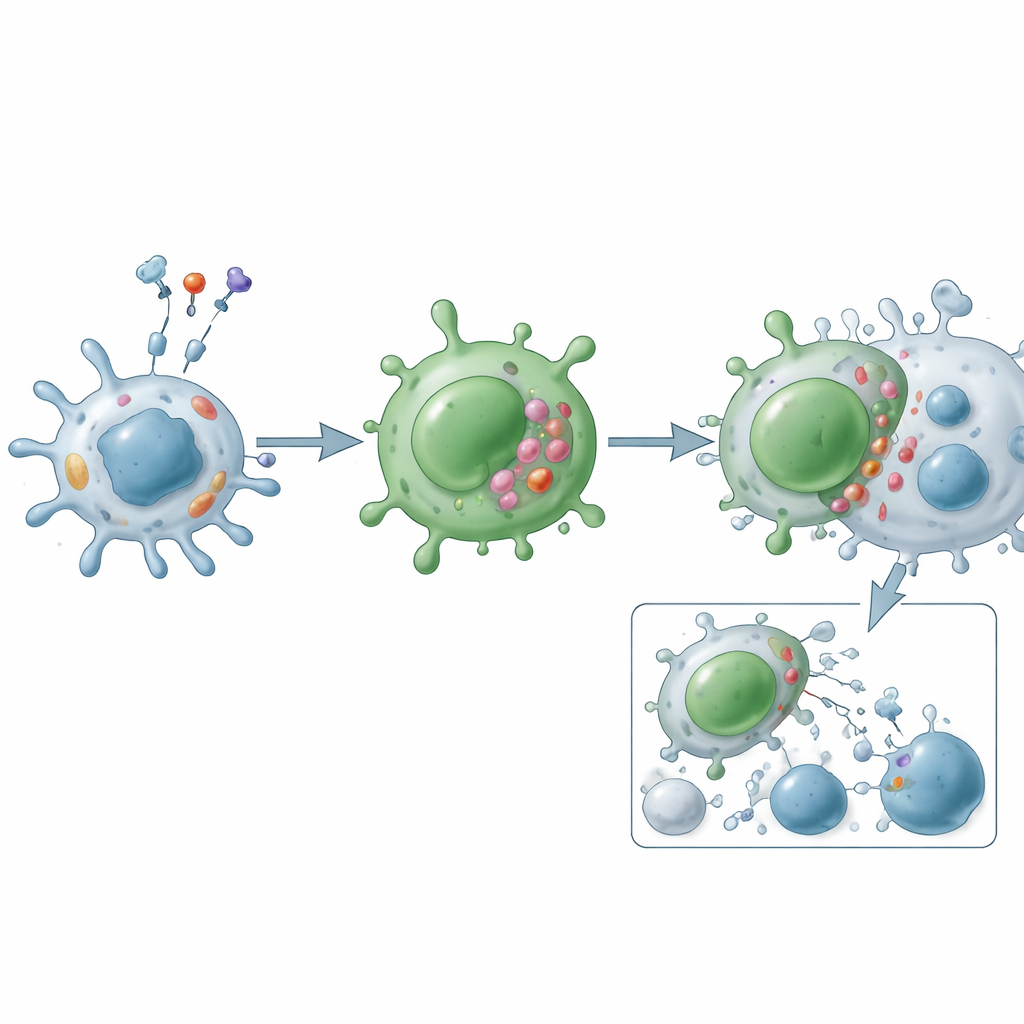
חברים בזיהום וסרטן, אויבים באוטואימוניות ומחלות לב
התנהגות זו בעלת השפעה כפולה ניכרת במצבים רבים. בהפטיטיס B כרונית, HIV ו-COVID-19, תאי CD4 ציטוטוקסיים מסייעים לשלוט בוירוסים כאשר תאי CD8 מותשים, ונוכחותם יכולה להתקשר לשליטה טובה יותר או להחלמה. בגידולים מוצקים ובממאציות דם הם יכולים לזהות ישירות תאי גידול המציגים סמנים חיסוניים או אותות סטרס מתאימים ועלולים לשפר תשומות לאימונותרפיות כמו מעכבי נקודות ביקורת וטיפולי CAR-T. באותו הזמן, אותם מנגנונים עלולים לגרום נזק: בלופוס, דלקת מפרקים שגרונית, דלקת מעי דלקתית, מחלת עורקי הכוריד, פרפור עליות, ארטריטיס של תאי ענק ודחיית שתל, תאי CD4 ציטוטוקסיים מורחבים חודרים לרקמות, פוגעים בכלי דם או איברים ומגבירים דלקת ממושכת, לעתים קרובות בהתאמה לפרוגנוזה גרועה יותר.
להפוך כלי מסוכן לטיפול
מכיוון שתאי CD4 ציטוטוקסיים יכולים להיות גם מגנים וגם הרסניים, המאמר מדגיש אסטרטגיות טיפוליות חדשות ששואפות לכוונן את האוכלוסייה הזו במקום להשמידה כולה. גישה אחת היא להחליש את הפעילות המזיקה שלהם באמצעות מעכבים סלקטיביים שממוקדים בקולטני קוסטימולציה (כמו OX40 או 4-1BB), בציטוקינים דלקתיים, בתעלות יונים או במסלולי הישרדות. גישה נוספת היא לרתום את כוח ההרג שלהם בטיפולי התא המקבל (adoptive cell therapy), כולל תאי T מהונדסים גנטית ותאי CAR-T, שבהם תאי CD4 ציטוטוקסיים לעיתים מפגינים עמידות טובה יותר מאשר מוצרים שמכילים רק CD8. אסטרטגיה שלישית מציעה להפנות תאי CD4 רוצחים ארוכי-חיים שמזהים וירוסים כלפי גידולים באמצעות חיסונים או פפטידים ממקור פתוגני שמוצגים על ידי תאי סרטן. יחד, גישות אלה מציבות את תאי CD4 הציטוטוקסיים לא רק כסקרנות ביולוגית, אלא כנקודת שליטה מרכזית לטיפולים עתידיים שיכולים לחזק באופן מדויק יותר את ההגנה מפני זיהומים וסרטן ובו־בזמן להפחית דלקת הפוגעת ברקמות.
מנוף חדש לאימונותרפיות עתידיות
לקוראים שאינם מומחים, המסר המרכזי הוא כי תאי CD4 ה»מסייעים« גמישים הרבה יותר משהאמינו בעבר: חלקם יכולים לעבור למצב רוצח חמוש המגן מפני זיהומים מתמשכים וסרטן, אך גם תורם לאוטואימוניות, לנזק כלי דם ולדחיית שתלים. הסקירה טוענת כי לימוד אופן המעקב אחר תאים אלה, חיזוי מתי הם יסייעו או יזיקו וכיצד לכוונם באמצעות תרופות או טיפולים מהונדסים עשוי לשנות את הדרך בה מטפלים במגוון רחב של מחלות כרוניות — מהפטיטיס ו-HIV ועד דלקת מפרקים, קוליטיס, מחלות לב ולוקמיה. במקום פשוט לכבות או להמריץ את מערכת החיסון, טיפולים עתידיים עשויים להתרכז בהכוונת סוגי תאים רבי-עוצמה כמו תאי CD4 ציטוטוקסיים אל מטרות מועילות והרחק מרקמות הגוף שלנו.
ציטוט: Lai, L., Ran, S., Li, Y. et al. Cytotoxic CD4+ T cells: origin, biological functions, diseases and therapeutic targets. Sig Transduct Target Ther 11, 85 (2026). https://doi.org/10.1038/s41392-025-02533-z
מילות מפתח: תאי CD4 ציטוטוקסיים, פלסטיות של תאי חיסון, דלקת כרונית, אימונותרפיה לסרטן, מחלה אוטואימונית