Clear Sky Science · he
IFFO1 מונע סרטן השד על ידי תיאום פיצול המיטוכונדריה וסינתזת חומצות השומן דרך ציר LaminA/C‑PGC1α
מדוע מחקר זה חשוב
סרטן השד נותר אחד הגורמים המובילים לתמותה ממחלת הסרטן בקרב נשים, בעיקר משום שחלק מהגידולים ממשיכים לצמוח, להתפשט ולהתחמק מטיפולים קיימים. המחקר חושף "בלם" תאי שלא קיבל התייחסות מספקת עד כה, בשם IFFO1, שמאט את סרטן השד על ידי ויסות שני מנועים מרכזיים לצמיחת הגידול: תחנות האנרגיה של התא, המיטוכונדריות, ויכולתו של התא לייצר ולאחסן שומנים. הבנת הבלם הזה מציעה גישה טיפולית חדשה שעשויה להיות יעילה על פני תת‑סוגים שונים של סרטן השד.
שומרת מוסתרת בתוך תאי השד
החוקרים התחילו בבחינת דגימות מ‑30 נשים עם סרטן שד, וכן בסיסי נתונים ציבוריים גדולים של סרטן. הם מצאו שרמות החלבון IFFO1 היו בעקביות נמוכות יותר ברקמת הגידול מאשר ברקמה השדית התקינה הסמוכה. ככל שהשלב של הסרטן היה מתקדם יותר, כך IFFO1 היה פחות נוכח, ומטופלות של גידולים עם רמות גבוהות יותר של IFFO1 נטו לחיות זמן רב יותר. בתאי סרטן שד שמוחזקו במעבדה, אילוץ להבעה מוגברת של IFFO1 הקטין באופן חמור את היכולת של התאים לגדול, להתחלק ולהיגרר — התנהגויות הנדרשות להתרחבות ולהתפשטות הגידול. IFFO1 גם דיכא תוכנית תאית הידועה כהעברה אפיתליאלית‑מזנכימלית, שמקלה על תאי סרטן להתנתק ולחדור רקמות אחרות.
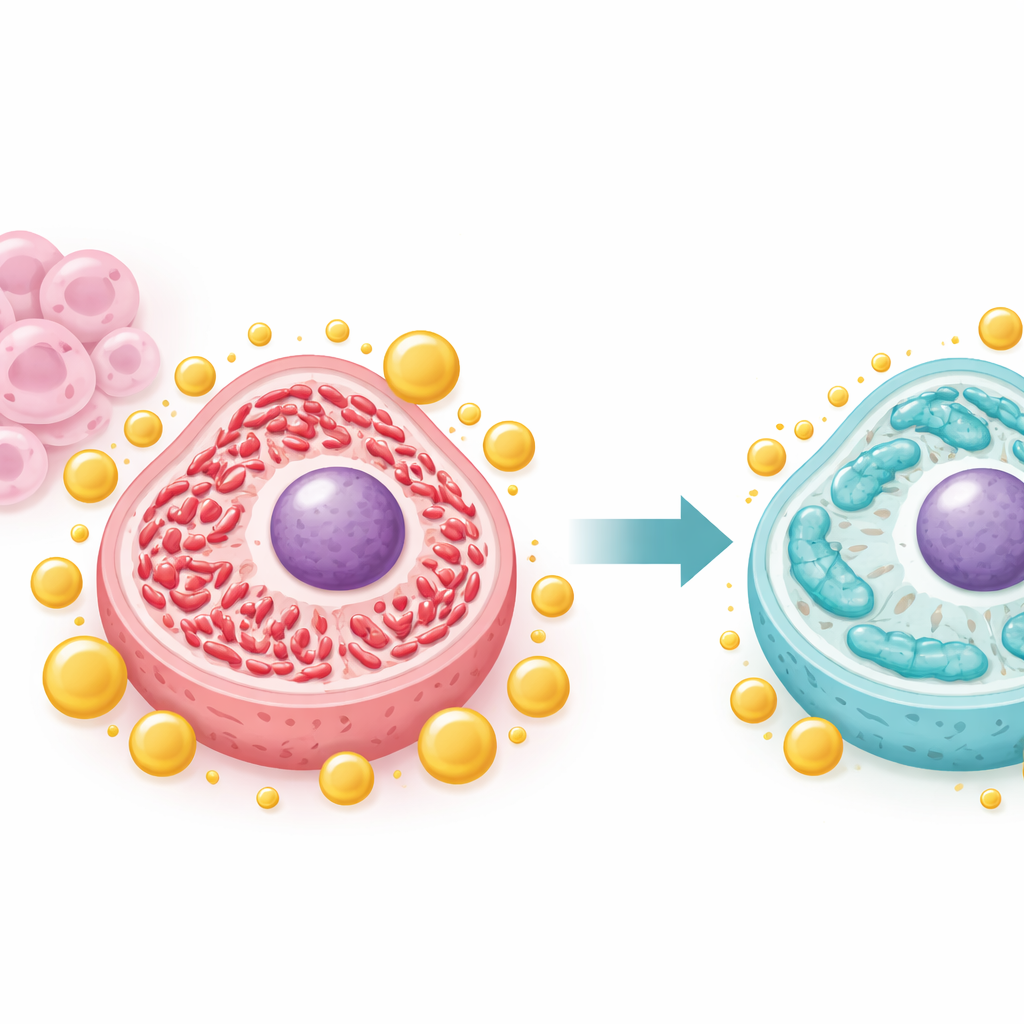
הרגעה של תחנות אנרגיה פעילות מדי
תאי סרטן לעתים קרובות משנים את צורת המיטוכונדריות, תחנות הכוח הזעירות שבתוך התא, כדי לתמוך בצמיחה מהירה. הצוות הראה כי IFFO1 מזיז את האיזון מרמת "פיצול" גבוהה ומקוטעת למצב של "מיזוג" מוארך — מצב הנחשב לרוב לבריא ויציב יותר. כאשר IFFO1 היה בשפע, חלבוני פיצול מרכזיים כגון Drp1 ו‑Fis1 ירדו, בעוד שחלבוני מיזוג עלו. במיקרוסקופ נצפו מיטוכונדריות ארוכות פחות מקוטעות, ומדדים של DNA מיטוכונדריאלי ותפוקת אנרגיה ירדו מרמות חריגות שנצפו בתאים אגרסיביים. שינויים אלה מצביעים על כך ש‑IFFO1 מונע מהמיטוכונדריות להכנס למצב היפראקטיבי שתומך בצמיחה גידולית בלתי מבוקרת.
ניתוק קו אספקת השומנים
גידולים שגדלים במהירות אינם זקוקים רק לאנרגיה; הם זקוקים גם לאספקה יציבה של שומנים לבניית ממברנות חדשות ולמולקולות איתות. המחקר מצא ש‑IFFO1 גם מדכא את האצה המטבולית הזו. בתאים עם עודף IFFO1 הופחתו חלבונים מרכזיים בבניית שומנים — כולל FASN, SREBP‑1, SCD1 ואחרים. בדיקות אנזימטיות איששו פעילות סינתאזת שומן נמוכה יותר, ובדיקות כימיות הראו ירידות בחומצות שומן חופשיות, טריגליצרידים וכולסטרול. חומרים צובעים המדגישים מאגרי שומן הראו פחות טיפות שומניות ופחות שומן נייטרלי כולל בתוך תאי הסרטן. בניגוד לכך, הגברה של חלבון הפיצול Drp1 גרמה לאפקט הפוך — הגברה של ייצור השומן, בעוד שהשתקה של Drp1 צמצמה אותו — מה שתומך בקשר ישיר בין צורת המיטוכונדריה לאספקת השומן בסרטן.
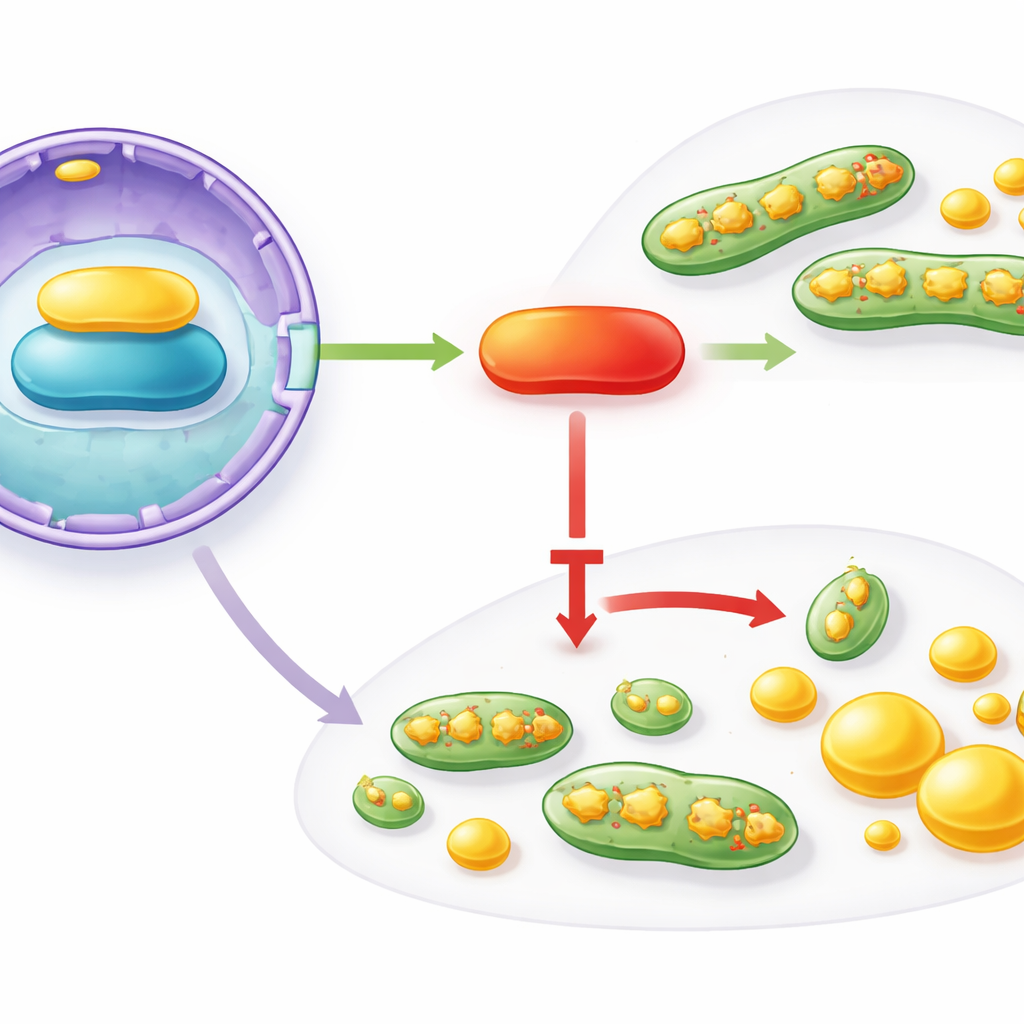
שרשרת איתות מהגרעין אל המיטוכונדריה
איך IFFO1 מארגן את השינויים הרחבים האלה? החוקרים עקבו אחרי שרשרת אינטראקציות שמתחילה בגרעין התא ומסתיימת במיטוכונדריה ובמכונת ייצור השומנים. IFFO1 נקשר באופן פיזי לחלבון מבני של מעטפת הגרעין בשם Lamin A/C, ומעלה את רמותיו. Lamin A/C, בתורו, תומך בפעילותו של PGC1α — רגולטור על שמפקח על בריאות המיטוכונדריות והמטבוליזם. ברקמות תאי סרטן השד ובתאים, גם Lamin A/C וגם PGC1α נמצאו מופחתים, מה שמדמה את אובדן ה‑IFFO1. כאשר המדענים הגבירו במכוון את IFFO1, Lamin A/C ו‑PGC1α עלו, פיצול המיטוכונדריה ירד, וסינתזת השומנים נחלשה. השתקת Lamin A/C מחקה את היתרונות האלה, אך שיקום PGC1α החזירם — ומצביע על ציר פונקציונלי IFFO1 → Lamin A/C → PGC1α שמרסן שינויים מיטוכונדריאליים ושומניים המקדמים גידול.
בדיקת ה"בלם" בעולמות חיים
כדי לבחון האם ההשפעות התאית מתרגמות לגידולים אמיתיים, הצוות השתיל תאי סרטן שד אנושיים עם או בלי עודף IFFO1 בעכברים. גידולים עם IFFO1 מוגבר גדלו לאט יותר, שקלו פחות בנקודת הסיום הניסיונית והראו סימנים פחותים של הצטברות שומן. במודל נפרד שבו הוזרקו תאי סרטן למחזור הדם כדי לייצר גרורות ריאתיות, תאים שמייצרים יותר IFFO1 יצרו מספר נודולים ריאתיים משמעותית נמוך יותר. ניתוחי רקמות מהעכברים השתקפו בממצאי תרבית התאים: יותר Lamin A/C ו‑PGC1α, פחות פיצול מיטוכונדריאלי וכמות סינתזת שומן נמוכה יותר.
מה זה אומר לטיפולים עתידיים
לסיכום, העבודה מציגה את IFFO1 כמדכא גידולים רב‑שכבתי המחבר את השלד המבני של התא, תחנות האנרגיה שלו ומכונת ייצור השומנים שלו. על‑ידי ייצוב Lamin A/C והגברת PGC1α, IFFO1 מונע מהמיטוכונדריות להישבר באופן מופרז וחוסם ייצור יתר של שומנים שתאי סרטן מסתמכים עליהם. להבהרת הקהל הרחב: החלבון הזה פועל כמו בלם פנימי גם על האנרגיה וגם על חומרי הבנייה שמזינים את צמיחת הסרטן והשגשוג שלו. תרופות אשר יעלו את רמות IFFO1 או יחקו את השפעותיו על ציר Lamin A/C–PGC1α עשויות אי‑אז להציע אפשרויות חדשות, במיוחד לצורות תוקפניות או עמידות לטיפול של סרטן השד.
ציטוט: Cai, H., He, J. IFFO1 inhibits breast cancer by coordinating mitochondrial fission and fatty acid synthesis via the LaminA/C-PGC1α axis. Oncogenesis 15, 16 (2026). https://doi.org/10.1038/s41389-026-00609-1
מילות מפתח: סרטן השד, דינמיקות מיטוכונדריאליות, סינתזת חומצות שומן, מטבוליזם גידול, ציר PGC1α