Clear Sky Science · he
הבקרת אונקוגנית של סינתזת נוקליאוטידים
מדוע תאי סרטן דואגים לבלוקים הבניין
כבר זמן רב מתארים את הסרטן כתאים שאינם מפסיקים להתחלק. כדי לשכפל את עצמם, תאים אלה זקוקים לאספקה קבועה של בלוקים קטנטנים הנקראים נוקליאוטידים, המרכיבים את ה‑DNA וה‑RNA ומשמשים גם כהנעה לתהליכים תאיים רבים. סקירה זו מסבירה כיצד גנים שמניעים סרטן משנים את כימיית התא כדי לשמר ייצור גבוה של נוקליאוטידים, כיצד גידולים עוברים בין אסטרטגיות שונות להשגת המולקולות האלה, וכיצד רופאים יכולים לנצל את הטריקים האלה בעזרת תרופות ישנות וחדשות.
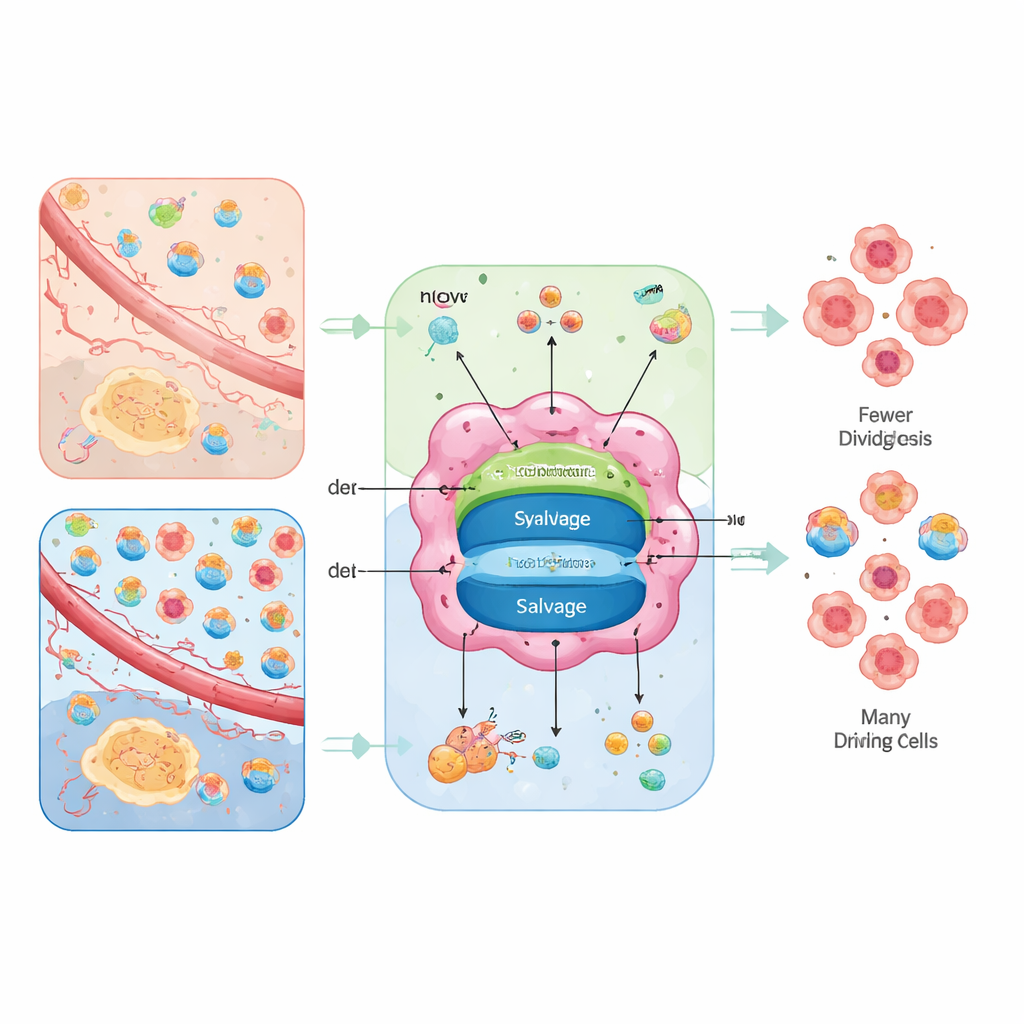
שתי דרכים לאותם בלוקים בנייה
תאים יכולים לייצר נוקליאוטידים מאפס או למחזר אותם. הדרך «מאפס», הנקראת סינתזה דה־נובו, מרכיבה טבעות ממזונות בסיסיים כגון גלוקוז, חומצות אמינו, פחמן דו־חמצני וביקרבונט, באמצעות תגובות רב־שלביות ותובעניות באנרגיה. דרך המחזור, הקרויה salvage, לוקחת בסיסים ונוקליאוזידים מפורקים מן החוץ או מפסולת תאית ומחזרת אותם לנוקליאוטידים שימושיים בעלות אנרגטית נמוכה בהרבה. גידולים משתמשים בשתי האפשרויות, אך האיזון ביניהן תלוי באספקת האנרגיה הפנימית שלהם ובמה שסביבת הרקמה מספקת.
כיצד סביבה גידולית מנווטת את הבחירה
המחברים מציגים את אספקת הנוקליאוטידים כבעיית "ניתוב בצורת הסביבה". באזורים רעבים שבהם חומצות אמינו זמינות אך נוקליאוזידים חופשיים נדירים, תאי סרטן נשענים מאוד על מסלולי דה‑נובו והופכים לפגיעים לתרופות החוסמות שלבים אלה. באזורים מטופלים טוב יותר, שבהם הדם מספק שפע של נוקליאוזידים או שבהם המיטוכונדריה חלשה, הגידולים יכולים להסתמך יותר על salvage ולהיות רגישים לחוסמי נשאים המונעים קליטת נוקליאוזידים. כשהשני פתוחים, גידולים מגלים גמישות מטבולית ויכולים להתחמק מתרופה יחידה; כשהם שניהם סגורים, התאים נעצרים בשכפול ה‑DNA, מצטבר נזק ועלולים למות או לעבור למדינות בגרות פחות תוקפניות.
קוים תומכים נסתרים המזינים את אספקת הנוקליאוטידים
כדי לשמור על מפעלי הנוקליאוטידים פועלים נדרשות מספר מעגלים תומכים. מסלול הפנטוז‑פוספט מספק את עמוד השדרה הסוכרי ואת כח החיזור; גלוטאמין והמחזור המפיק אנרגיה במיטוכונדריה מספקים חנקן ואספרטט; כימיה של סרין, גליצין וחומצה פולית תורמת יחידות חד‑פחמניות שמסיימות את הטבעות; וביקרבונט מביא פחמנים חיוניים. מנהלי הסרטן כגון PI3K–AKT–mTORC1, RAS–MAPK ו‑MYC מגדילים יחד את הפעילות של מסלולים אלה, מגבירים אנזימים מרכזיים ואפילו מרכיבים אשכולות של אנזימים שמובילים ביניים בלתי יציבים ביעילות. לעומת זאת, חיישני לחץ כמו LKB1–AMPK ו‑p53 פועלים בדרך כלל כבלמים, מצמצמים את תפוקת הנוקליאוטידים כאשר האנרגיה או שלמות ה‑DNA מאוימות — בלמים שרבים מהגידולים מנטרלים.
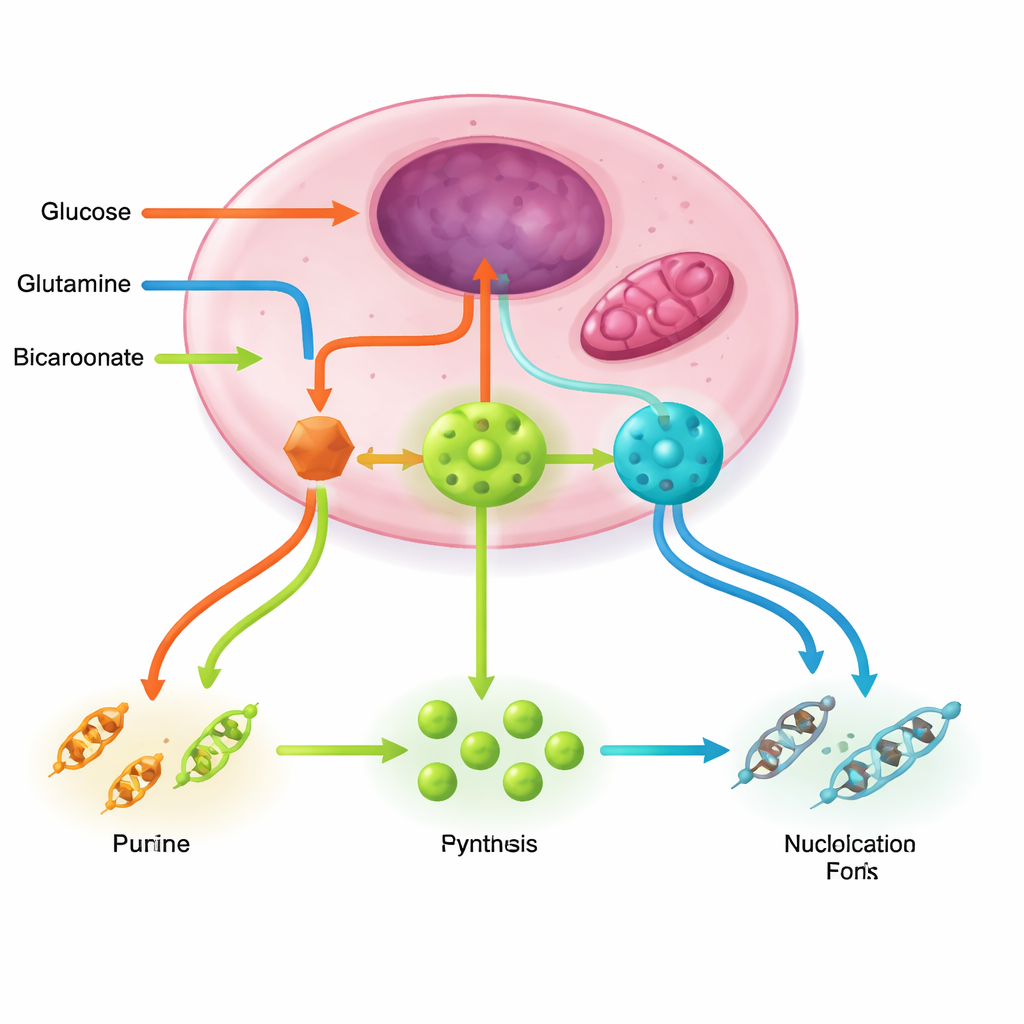
כימותרפיה ישנה, לוגיקה מטבולית חדשה
מכיוון שתאים הגדלים במהירות תלויים כל‑כך בנוקליאוטידים, חלק מהכימותרפיות הראשונות פגעו בחולשה זו. תרופות קלאסיות כגון מתוטרקסאט, 5‑פלואראציל, ציטאראבין, גמציטאבין ומגוון אנלוגים של פורין חוסמות שימוש בחומצה פולית, מעכבות אנזימים ספציפיים או מתחזות לבלוקים בנייה פגומים שמרעילים DNA ו‑RNA. הסקירה מביטה מחדש בתרופות אלו דרך משקפיי מודל הניתוב, ומסבירה מדוע תופעות לוואי והתנגדות נפוצות: רקמות שאינן סרטניות גם הן זקוקות לנוקליאוטידים, וגידולים לעיתים קרובות יכולים לנתב מחדש את הזרימה דרך salvage או מסלולים מקבילים כאשר קשר אחד נחסם.
אסטרטגיות בדור הבא ושאלות פתוחות
גישות חדשות שואפות להיות ברירות יותר על‑ידי תקיפה של החלקים ברשת המוטים לטובת הסרטן. מפותחות תרופות ניסיוניות כנגד אנזימי חד‑פחמן מיטוכונדריאליים כגון MTHFD2, אנזים פירימידין DHODH, ואנזימי פורין כמו IMPDH ו‑PAICS, לעתים בשילובים שגם חוסמים נשאי salvage. המחברים מציעים סימנים מעשיים — כגון רמות נשאים, צפיפות כלי דם, כושר מיטוכונדריאלי וביטוי אנזימים מטבוליים ספציפיים — כדי להכריע אילו גידולים נשענים יותר על דה‑נובו או על salvage ולתאם מטופלים עם טיפולים המכוונים למסלולים אלה. בהסתכלות לעתיד, הם מדגישים שאלות מפתח, כולל כיצד מסלולים אלה משתנים במרחב ובזמן בתוך גידולים אמיתיים, כיצד תאי חיסון וסטרומה סביבתיים מעצבים את הזמינות של נוקליאוטידים, וכיצד לתכנן לוחות זמנים של תרופות סבילים שמנצלים לחץ שכפול בלי להציף רקמות נורמליות. יחדיו, העבודה טוענת שהבנת מטבוליזם הנוקליאוטידים ומיקודו עשויים להפוך דרישה בסיסית של חלוקת תאים לידית אישית ועוצמתית נגד הסרטן.
ציטוט: Vidal-Cruchez, O., Ben-Sahra, I. The oncogenic control of nucleotide synthesis. Oncogenesis 15, 17 (2026). https://doi.org/10.1038/s41389-026-00608-2
מילות מפתח: מטבוליזם של נוקליאוטידים, מטבוליזם של סרטן, סינתזה דה־נובו, דרכי הצלה (salvage), תרפיות מטבוליות