Clear Sky Science · he
תפקיד הדימתילאז היסטוני PHF2 כמעכב גידול בסרטן הכבד על‑ידי ויסות SRXN1
מדוע מחקר סרטן הכבד הזה חשוב
סרטן הכבד הוא אחד הסוגים הקטלניים ביותר ברחבי העולם, והתרופות הקיימות מאריכות חיים רק במידה מוגבלת עבור מטופלים רבים. המחקר הזה שואל שאלה שונה: במקום לכוון לגנים המניעים סרטן המוכרים, האם אפשר לנצל את הדרך שבה הדנ״א נארז ומסומן כימית בתאי הכבד כדי למצוא אפשרויות טיפול חדשות ומדויקות יותר? החוקרים מתמקדים בחלבון מעט ידוע בשם PHF2 ומגלים כיצד ייתכן שהוא מסייע למנוע מתאי כבד להפוך לממאירים.
מחפשים נקודות תורפה במערכת הבקרה של הסרטן
הסרטן אינו מונע רק על‑ידי גנים פגומים; הוא מזין גם על‑ידי בבקרות אפיגנטיות לקויות — התגים הכימיים ומורכבי החלבון שמחליטים אילו גנים נדלקים או כבויים. בקרצינומה של תאי הכבד, הצורה השכיחה ביותר של סרטן הכבד, רבים מהווסתים האלה מופרעים. הצוות בדק בצורה שיטתית 497 מווסתים אפיגנטיים בשש שורות תאי סרטן כבד, באמצעות כלי RNA כדי להפחית זמנית כל ווסת אחד בשורה ואז למדוד עד כמה התאים הסרטניים שורדים. המסך הרחב הזה תוכנן לחשוף על אילו ווסתים הסרטן מסתמך לצמוח, ואילו מהם בדרך כלל פועלים כבלמים על היווצרות גידולים.
גילוי מסייעים ומגינים חדשים של סרטן
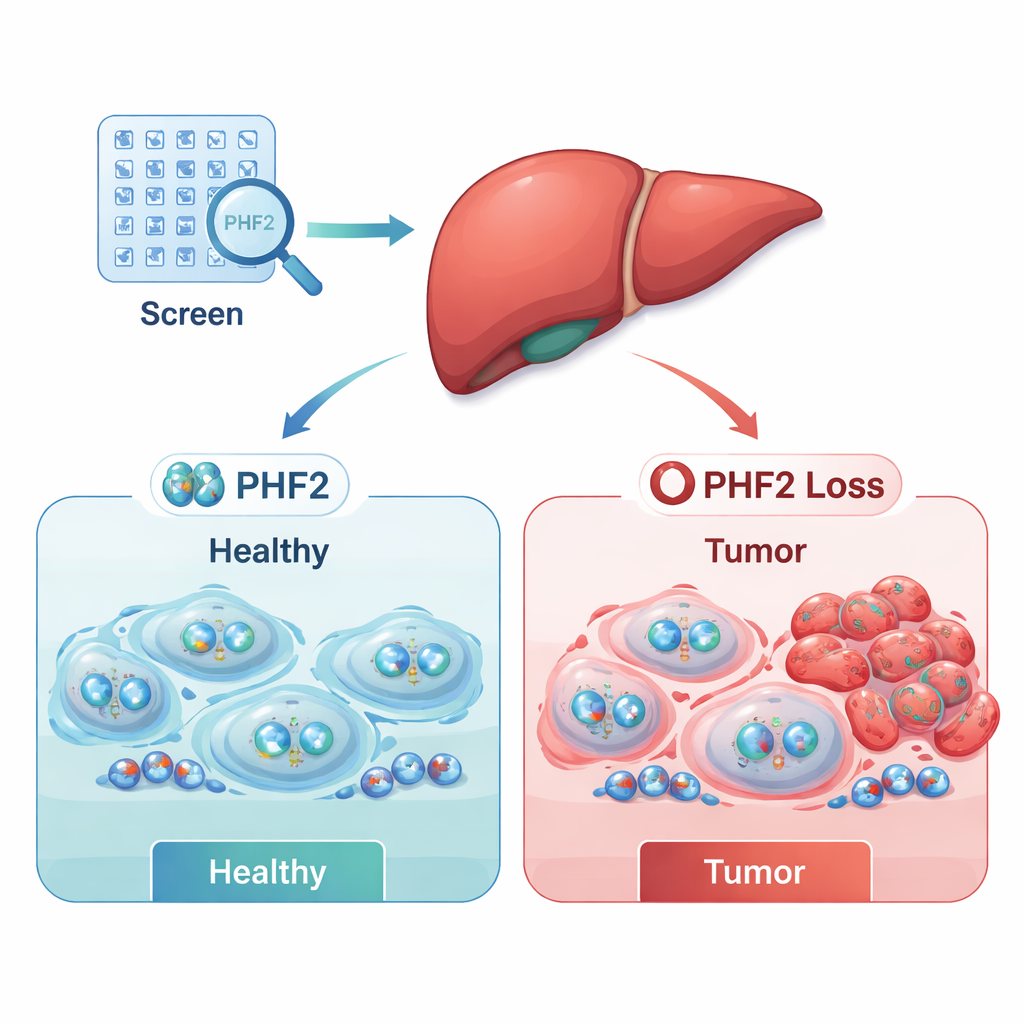
המסך חשף שתי קבוצות עיקריות: מאיצי סרטן פוטנציאליים (אונקוגנים) שאובדן שלהם פגע בהישרדות התאים הסרטניים, ו"בלמים" פוטנציאליים (מעכבי גידול) שאובדן שלהם שיפר את גדילת התאים הסרטניים. על‑ידי שילוב נתוני המעבדה שלהם עם מאגרי נתונים ציבוריים רחבים של מטופלים, החוקרים צמצמו את הרשימה למספר מועמדים רלוונטיים קלינית. שני ווסתים, SUPT7L ו‑SMARCC1, נטו להיות פעילים יותר בגידולים וקושרו להישרדות גרועה יותר. לעומת זאת, ווסת אחד—PHF2—היה לעתים קרובות פחות פעיל בגידולי כבד, ומטופלים שלגידוליהם שמרו על רמות PHF2 גבוהות יחסית חיו בדרך כלל זמן ארוך יותר. דפוסים אלה הציעו כי PHF2 עשוי לפעול כמעכב גידול בסרטן הכבד האנושי.
כיצד אובדן PHF2 משנה תאי סרטן כבד
כדי לבדוק את PHF2 ביתר עומק, הצוות מהנדס תאי סרטן כבד כדי לייצר מידה קבועה פחותה של חלבון זה ועקב אחר התנהגותם לאורך זמן. תאים עם PHF2 מופחת גדלו מהר יותר והראו רמות גבוהות יותר של Ki‑67, סימן לחלוקת תאים פעילה, מה שמצביע על כך ש‑PHF2 בדרך כלל מסייע להגביל פרוליפרציה. ההשפעות הללו היו בולטות במיוחד בשורות תאים הסרטניות שכבר היו אגרסיביות, דבר המרמז כי אובדן PHF2 לבדו עשוי שלא להתחיל סרטן, אך יכול להאיץ את גדילתם של תאים ממאירים לאחר שהגידולים כבר נוצרו.
קשר מפתיע להגנות הלחץ התאי
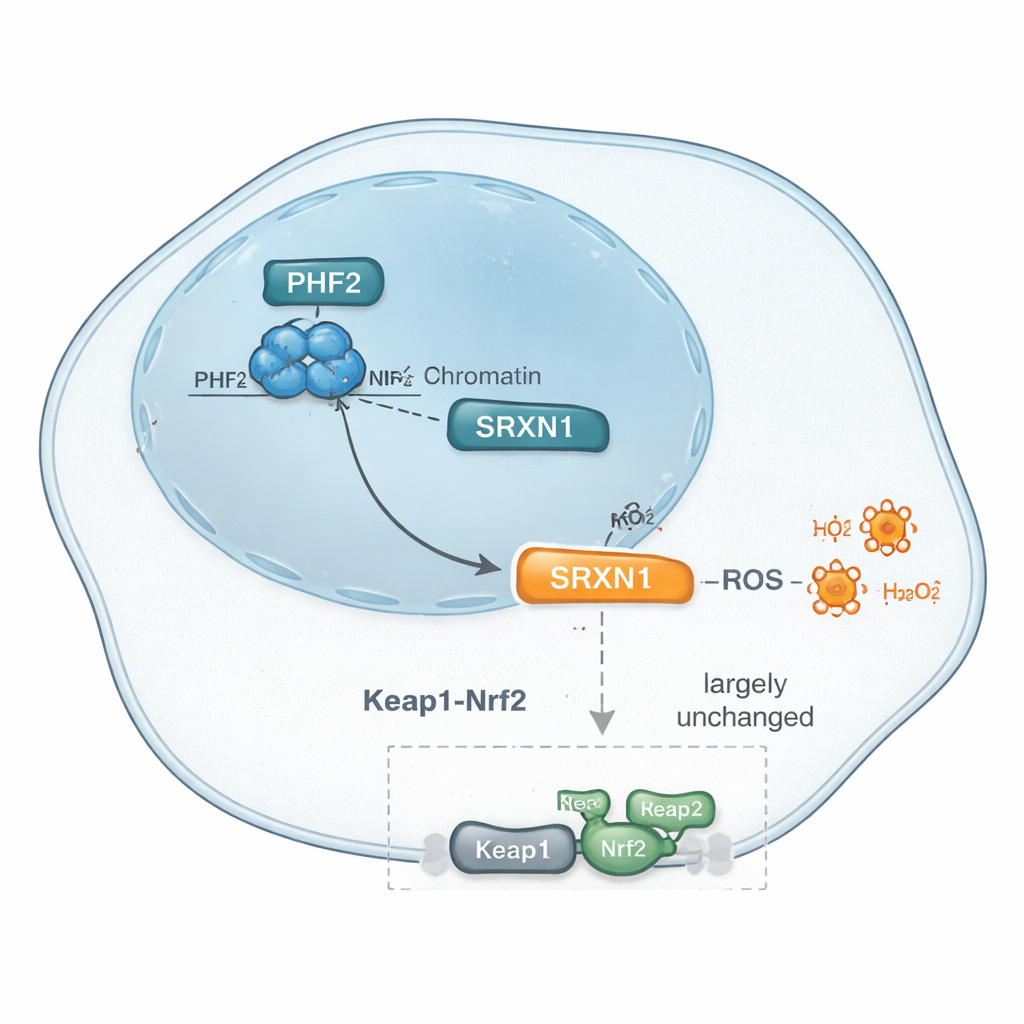
לאחר מכן השתמשו החוקרים בשיטות פרופיל חלבוני מודרניות כדי לתעד אלפי חלבונים שרמותיהם השתנו כאשר PHF2 הופחת. בין המהירויות הרבות העדינות, דפוס אחד בלט: רמות חלבון מגן‑לחץ בשם SRXN1 ירדו בעקביות כאשר PHF2 אבד. SRXN1 עוזר לתאים להתמודד עם זני חמצון ריאקטיביים — תוצרי לוואי כימית פעילות שיכולים לפגוע בדנ״א ובחלבונים אך גם לדחוף תאים סרטניים להסתגל. הנתונים הציעו כי PHF2 מסייע לשמור על רמות SRXN1, וכי שינוי איזון זה עשוי להשפיע על האופן שבו תאי סרטן כבד מגיבים ללחץ פנימי ולמהר את קצב צמיחתם.
פועלת מחוץ למסלול לחץ מוכר
SRXN1 נשלט בדרך כלל על‑ידי מתג תגובת לחץ ראשי בשם Nrf2, שמפעיל גנים אנטי‑אוקסידנטים רבים כאשר תאים ניצבים בפני מתח חמצוני. מאחר ש‑SRXN1 ירד כאשר PHF2 דוכא, הצוות בדק האם PHF2 פשוט פועל דרך מסלול Nrf2 המוכר הזה. הם בחנו גנים וחלבונים מרכזיים הקשורים ל‑Nrf2, טיפלו בתאים בתרופות שמפעילות את Nrf2 על‑ידי חסימת מעכבו Keap1, והשתמשו בכלים גנטיים כדי להפחית ישירות את Keap1. לאורך כל הבדיקות, התגובה של תאים חסרי PHF2 דמתה למדי לזו של תאים נורמליים, וניתוחים רחבים של מסלולים ופקטורי שעתוק לא הצביעו על Nrf2 כשחקן מרכזי. במקום זאת, פקטורים אחרים, כולל ZNF384 ו‑Nrf1 — שניהם נקשרו בעבר לסרטן כבד — עלו כמועמדים. יחד, הראיות מרמזות כי שליטת PHF2 על SRXN1 בתגובות אנטי‑אוקסידנטיות עשויה לעקוף את אותות ה‑Nrf2 הקלאסיים, ומציעות מסלול ויסות לחץ מובהק בגידולים אלה.
מה זה עשוי להעיד על טיפולים עתידיים
ללא‑מומחה, המסקנה המרכזית היא שמחקר זה מזהה את PHF2 כגורם מגן מבטיח בסרטן הכבד: כאשר PHF2 נוכח ופעיל, התאים הגידוליים גדלים לאט יותר; כאשר הוא מוחלש, הם מקבלים יתרון גידול ומשנים את האופן שבו הם מטפלים בלחץ התאי. מאחר ש‑PHF2 עצמו עשוי להיות קשה לחסום או להגביר בעזרת תרופות מולקולריות קטנות קונבנציונליות, המחברים מצביעים על אסטרטגיות מתפתחות כגון טיפולים מבוססי RNA או תרופות שמשפרות את פעילות PHF2 דרך שותפי איתות שמעליו. הם גם מדגישים שהשפעות PHF2 תלויות בהקשר — השפעתו עשויה להשתנות בהתאם למוטציות נוספות כמו מצב p53 — ולכן כל טיפול עתידי ידרוש ככל הנראה בחירת מטופלים זהירה. בסך הכול, העבודה מלבנת את הבנתנו כיצד ווסתים אפיגנטיים מעצבים את התנהגות סרטן הכבד ופותחת דרכים חדשות לעיצוב טיפולים שמחזירים או מחקים את השפעתו המעכבת של PHF2 על הגידול.
ציטוט: Thng, D.K.H., Hooi, L., Yong, W.K. et al. The role of histone demethylase PHF2 as a tumour suppressor in hepatocellular carcinoma by regulating SRXN1. Oncogenesis 15, 6 (2026). https://doi.org/10.1038/s41389-026-00597-2
מילות מפתח: קרצינומה של תאי כבד, ויסות אפיגנטי, PHF2, SRXN1, טיפול בסרטן כבד