Clear Sky Science · he
התמוטטות HILPDA בתיווך TRIM21 מתגברת על עמידות לאימונותרפיה נגד PD-1 בסרטן השד באמצעות הגבלת פלמיטוילציה של PD-L1
מדוע חלק מאימונותרפיות הסרטן מפסיקות לפעול
תרופות המשחררות את המערכת החיסונית, כמו טיפולים נגד PD‑1, שינו את הטיפול במספר סוגי סרטן, כולל צורות אלימות של סרטן השד. עם זאת, גידולים רבים או שאינם מגיבים מלכתחילה או שמוצאים בסופו של דבר דרכים להתחמק. המחקר הזה חוקר מסלול כזה של התחמקות בסרטן השד המשולש‑שלילי ומראה כיצד שינוי חידוד במטבוליזם השומנים של הגידול — ובחינת תרופה משומשת בשם פנרטיניד — עשויים לפתוח מחדש את הדלת בפני המערכת החיסונית כאשר אימונותרפיה סטנדרטית נכשלת. 
עוזר נסתרים שמגן על הגידולים
החוקרים התמקדו בחלבון מועט־הכרה בשם HILPDA, ששויך בעבר לאופן שבו תאים מתמודדים עם שומנים במצבי לחץ. בהשוואה בין גידולי שד בעכברים שנותרו רגישים לטיפול נגד PD‑1 לבין גידולים שהפכו לעמידים, הם מצאו שרמות HILPDA היו גבוהות בהרבה בגידולים העמידים. ניתוחים של מאגרי מטופלים גדולים ודגימות גידול מנשים חולות סרטן השד אישרו כי HILPDA רב יותר בגידולים מאשר ברקמת שד נורמלית, במיוחד במחלות משולשות‑שליליות, ושחולים שגידוליהם מבטאים HILPDA ברמה גבוהה נוטים להציג תוצאה גרועה יותר. בגידולים של אנשים שלא נהנו מטיפולים חוסמי PD‑1 נמצאו גם רמות גבוהות יותר של HILPDA, מה שמקשר חלבון זה ישירות לכישלון הטיפול.
כיצד הגידולים מסיטים את הנוף החיסוני נגדנו
כדי לראות מה HILPDA עושה בפועל בתוך הגידולים, הצוות ומהנדס תאי סרטן שד שייצרו או ייפטרו מהחלבון ואז גידל אותם יחד עם תאי חיסון אנושיים או בעכברים. כאשר HILPDA היה גבוה, הגידולים משכו תאי T רגולטוריים, תאים מדכאי מוצא מיאלואידי ותאים מיקרופגים מסוג M2 — סוגי תאים חיסוניים שמרככים את ההתקפה ועוזרים לגידול להתחבא. בו‑זמנית, מספרם וחוזקם של תאי CD8 קטלניים ותאי טבעיים קטלניים ירדו, ויכולתם לשחרר מולקולות רעילות ואותות דלקתיים הוקפאה. השתקת HILPDA הגבירה את מהלך זה: הגידולים הכילו פחות תאים מדכאים, יותר תאי קטלניים פעילים, צמיחה איטית יותר ופחות גרורות. החשוב מכל, כאשר בעלי‑חיים עם גידולים בעלי HILPDA נמוך קיבלו טיפול נגד PD‑1, גידוליהם התכווצו יותר והעכברים חיו זמן רב יותר, מה שמראה ש‑HILPDA שולטת ביעילות האימונותרפיה.
ייצור שומן, שריון מולקולרי והימנעות ממערכת החיסון
בעת חקירה עמוקה יותר, המדענים גילו כיצד HILPDA מעצב את מטבוליזם הגידול כדי להקשות על ההגנה החיסונית. בתוך תאי הסרטן, HILPDA נקשר לחלבון צ'פרון בשם HSP90 כדי לייצב גורם שעתוק, KLF5, שמניע ייצור שומנים. הטריו הזה מגביר את הסינתזה של חומצות שומן, ובפרט פלמיטאט, וממלא את תאי הגידול בטיפות ליפידיות. אחת מהשומן האלה מצורפת אז ל‑PD‑L1, חלבון מצומת הבקרה שעל פני הגידול ושולח לאימונוציטים אות "אל תתקפו". הצוות הראה שהוספת פלמיטאט לנקודה ספציפית על PD‑L1 פועלת כמו דבק מולקולרי: היא מסייעת ל‑PD‑L1 לשקוע יציב בממברנת התא ומונעת את פירוקו. מוטציה באתר ההיצמדות היחיד הזה פשטה את יציבות PD‑L1 וייחלשה יכולתו להגן על תאי הסרטן, אפילו כאשר HILPDA הייתה בשפע. במילים אחרות, ייצור השומן המונע על‑ידי HILPDA מזין שינוי כימי ב‑PD‑L1 שהופך את המגן החיסוני של הגידול ממוחלש לחזק כפלדה.
הבלם הטבעי שניתן ללחוץ עליו
לכל מאיץ יש בלם, וכאן הבלם הוא חלבון נוסף בשם TRIM21. המחברים גילו ש‑TRIM21 מזהה את HILPDA ומטביע עליה "דגלים" מולקולריים ששולחים אותו למכונת ההשמדה של התא. בגידולי שד מחולות, רמות TRIM21 נטו להיות נמוכות כאשר HILPDA הייתה גבוהה, ו‑TRIM21 נמוך נקשר לתוצאות קליניות גרועות, מה שמרמז שמערכת הבלימה הטבעית הזאת לעתים קרובות מוחלשת בסרטן. הצוות חיפש אז תרופות שיכולות לחזק את TRIM21 וזיהה את פנרטיניד, רטינואיד שכבר נבדק בבני אדם. במודלים תאים ובעכברים של סרטן השד המשולש‑שלילי, פנרטיניד הגביר את פעילות TRIM21, האיץ את פירוק HILPDA, צמצם סינתזת שומן ואת השינוי המגן של PD‑L1, ועיכב את צמיחת הגידול והתפשטותו. המדהים ביותר, שילוב פנרטיניד עם טיפול נגד PD‑1 עשה את הגידולים פגיעים יותר להתקפה חיסונית — עלה מספר תאי T קטלניים ותאי טבעיים קטלניים תוך הפחתה של תאים מדכאים במיקרו‑סביבת הגידול. 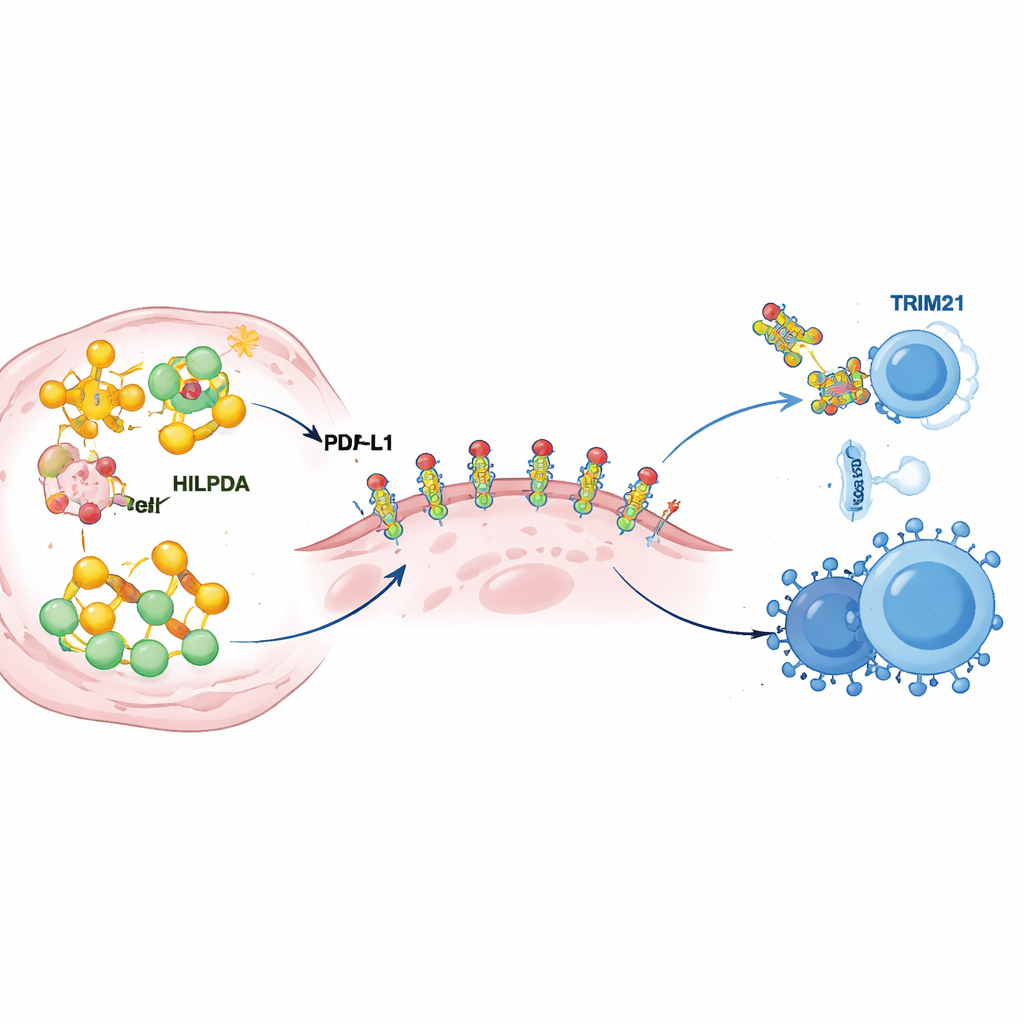
מה משמעות הדבר לטיפול בסרטן בעתיד
העבודה הזאת חושפת שרשרת אירועים שבה תאי סרטן שד בלחץ מגבירים את HILPDA, מגדילים את ייצור השומן ומחזקים כימית את PD‑L1 על פני השטח שלהם, ולא מאפשרים למערכת החיסון להתגבר עליהם אפילו בפני חוסמי PD‑1. TRIM21 פועלת כאמצעי הגנה פנימי שיכול לפרק את HILPDA, אך לעתים קרובות הוא חלש מדי בגידולים. הממצאים שהפנרטיניד מסוגל להפעיל מחדש את מנגנון ההגנה הזה מצביעים על דרך מעשית לשלב תרופה מטבולית עם אימונותרפיה קיימת כדי להתגבר על העמידות. אם יאושרו ניסויים קליניים, ייעוד ציר TRIM21–HILPDA–PD‑L1 עשוי להעניק לחולות סרטן השד המשולש‑שלילי, שקשה לטפל בהם, סיכוי נוסף ליהנות מטיפולים מבוססי חיסון.
ציטוט: Wang, X., Li, G., Wu, J. et al. TRIM21-mediated degradation of HILPDA overcomes anti-PD-1 immunotherapy resistance in breast cancer by limiting PD-L1 palmitoylation. Oncogene 45, 1338–1356 (2026). https://doi.org/10.1038/s41388-026-03728-6
מילות מפתח: סרטן השד משולש שלילי, עמידות לאימונותרפיה, פלמיטוילציה של PD-L1, מטבוליזם שומני גידולי, פנרטיניד