Clear Sky Science · he
L1TD1 מקדם את התקדמות אדנוקרצינומה מוקינוזית של המעי הגס על־ידי חיזוק יציבות mRNA של ABCC3
למה סוג סרטן זה העשיר בחלוח חשוב
סרטן המעי הגס והחלחולת הוא גורם מוביל למוות מסרטן ברחבי העולם. בקבוצה זו קיים תת‑סוג מובהק שנקרא אדנוקרצינומה מוקינוזית, שבו הגידולים מלאים בחלוחה צמיגה המהווה יותר ממחצית מסת הגידול. מחסום רירי דביק זה עלול לעזור לתאי הגידול להסתיר עצמם מהכימותרפיה וממנגנוני ההגנה של הגוף. במחקר זה נשאלת שאלה בסיסית אך מכרעת: מה שולט ביצירת כל אותו חלוח, והאם ניתן לכבות אותו כדי להאט את המחלה ולהגביר את היעילות של הטיפולים?
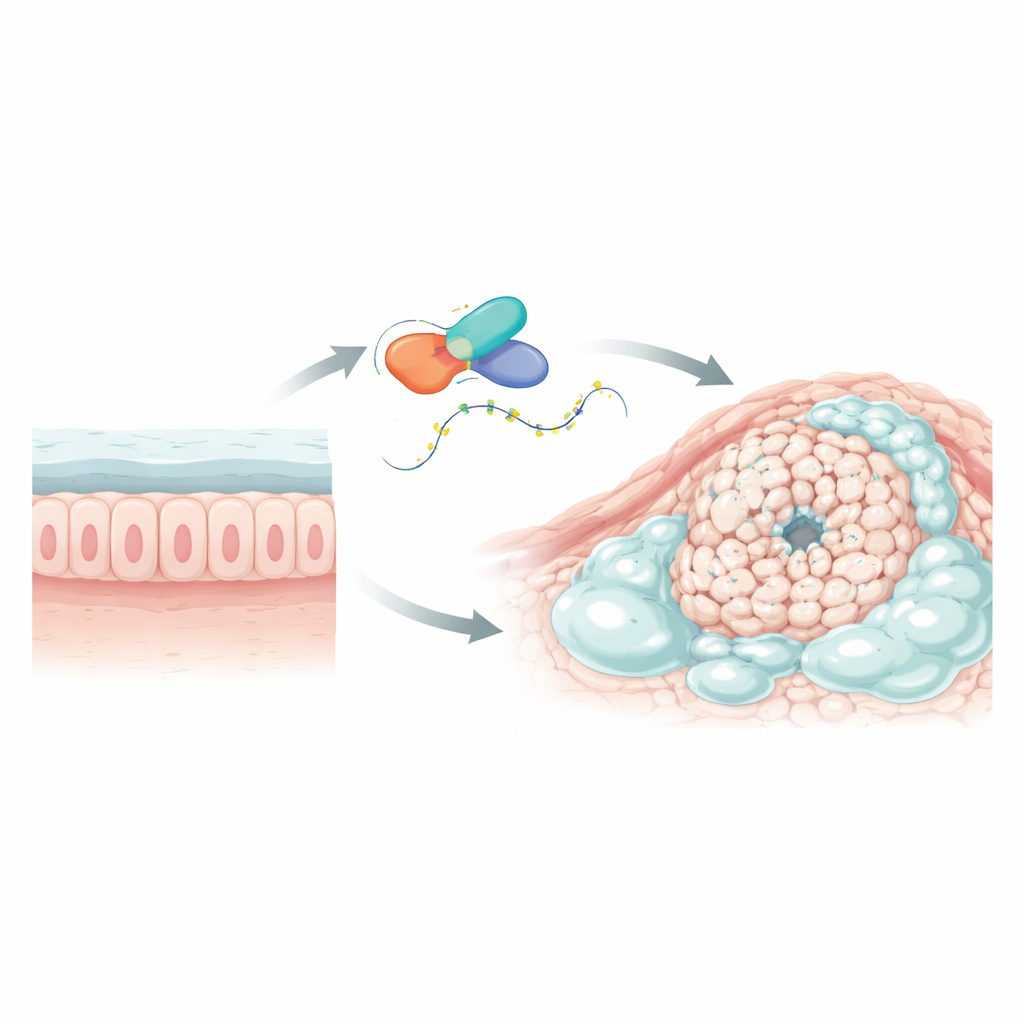
זיהוי גן מרכזי המטיל בעיות
החוקרים חיפשו תחילה במאגרי נתוני סרטן רחבים ובנתוני רצף תא‑בודד גנים שתפקידם שונה בגידולים עשירים בחלוח בהשוואה לסרטן קולורקטלי רגיל ולרקמה בריאה סמוכה. גן אחד, שנקרא L1TD1, בלט באופן ברור. הוא הועתק ברמות גבוהות בגידולים מוקינוזיים אך לא בגידולים הרגילים והיה גבוה יותר ברקמת הגידול לעומת המעי הנורמלי הסמוך. L1TD1 מקודד לחלבון הקשור ל‑RNA, המולקולה הנושאת את המסרים הגנטיים מ‑DNA למכונת ייצור החלבונים של התא. מאחר שחלבוני קשירה ל‑RNA יכולים לכוון בעדינות את משך הזמן שהמסרים נשמרים וכמה הם מתורגמים, L1TD1 היה מועמד חזק לשמש כמוּסָך של ויסות בתת‑סוגים רוויים בחלוחה אלה.
כיצד L1TD1 דוחף גדילה והתפשטות של סרטן
כדי לבדוק מה L1TD1 עושה בפועל, הצוות השתמש בקווי תאי סרטן מעי ובמודלים עכבריים. כאשר הגבירו את רמות L1TD1 בתאי הגידול, התאים התחלקו מהר יותר, זזו בקלות רבה יותר וחדרו דרך מחסומי רקמה בדימוי תוקפני יותר. השתקת L1TD1 הביאה להשפעה הפוכה — האטת גדילה וצמצום חדירה. בעכברים שהוכנסו לתוכם תאים עם רמות גבוהות של L1TD1, נצפו גידולים גדולים יותר והתפשטות תכופה יותר לכבד ולחלל הבטן. גידולים עם ביטוי גבוה של L1TD1 נטו להיות גם גדולים יותר, פחות ממויינים ובשלבים מתקדמים יותר בחולים, מה שמקשר את הגן להתנהגות מחלה גרועה יותר במציאות הקלינית.
הדלקת יצירת החלוח וההתנגדות לתרופות
החלוחה עצמה התגלתה כמרכזית להשפעת L1TD1. תאים עם יותר L1TD1 ייצרו כמויות גבוהות יותר של חלבונים מרכזיים היוצרים חלוחה, במיוחד MUC2 ו‑MUC5AC, והציגו תכונות של תאי גביע — תאי המעי שמפרישים חלוחה באופן רגיל. תרביות תלת‑ממד וצביעה של רקמות מחולים ובעכברים אישרו כי רמות גבוהות של L1TD1 הולכות יד ביד עם חלוחה עבה ושופעת יותר. חשוב מכך, החלוחה לא הייתה רק צופה מן הצד: כאשר החוקרים הפחיתו באופן סלקטיבי את MUC2, רוב העלייה בגדילה, בהחדירה ובהתנגדות לכימותרפיה שנגרמה על‑ידי L1TD1 נעלמה. תאים עשירים ב‑L1TD1 היו קשים יותר להריגה באמצעות התרופה הנפוצה אוקסליפלטין, וגידולים שנשאו תאים אלה התקמצו פחות בעכברים מטופלים — דבר הממחיש את החלח כפגז שה‑L1TD1 מסייע לבנות.
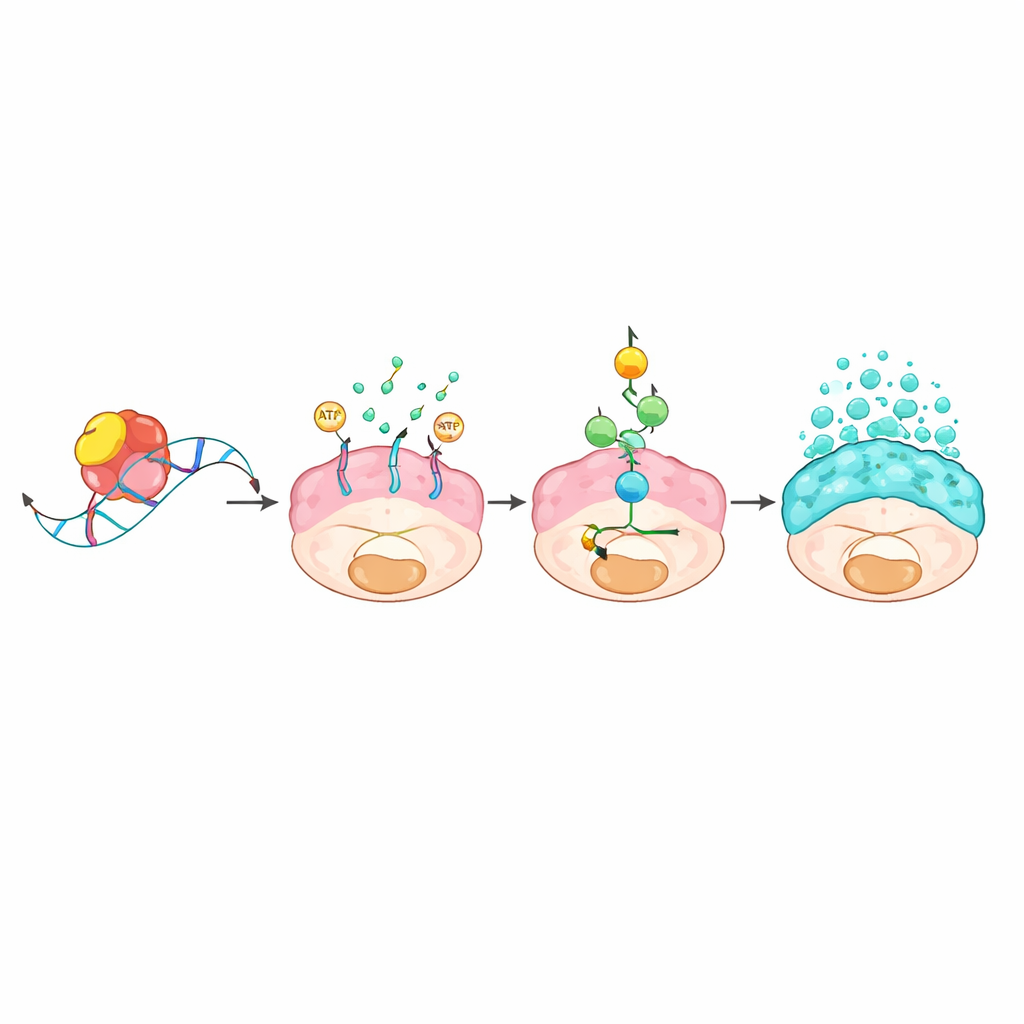
שרשרת מולקולרית שמקשרת בין ויסות RNA לשיטפונות חלוחה
הצוות שאל כיצד חלבון קשור‑RNA יכול לגרום לשינויים כה דרמטיים. על‑ידי תפיסת מולקולות RNA הקשורות פיזית ל‑L1TD1 והשוואת פעילות הגנים בנוכחות היעדרו, זיהו גן נשא שנקרא ABCC3 כמטרה עיקרית. L1TD1 התחבר למוטיב קצר "GUGU" בקצה התחתון של המסר ה‑RNA של ABCC3, וייצב אותו כך שהתא ייצר יותר מחלבון ABCC3, הידוע כ‑MRP3. נשא זה ישב בממברנת התא וצורך אנרגיה לשאוב חומרים מתוך התא. השרשור התוצאתי של בריחת האנרגיה הפעיל מערכת אזעקת מטבולית שמרכזת את החיישן AMPK, אשר בתורו הפעיל מסלול קלאסי של גדילה ומתח הידוע כ‑MAPK. לאחר שהופעל, קסקדה זו הגברה את הייצור והשחרור של חלבוני חלוחה וחיזקה את יכולת תאי הסרטן לגדול, לנוע ולהתנגד לתרופות. חסימת ABCC3 באופן גנטי או בעזרת תרכובת ניסיונית, או עיכוב מסלול ה‑MAPK — כל אלה החלישו את ייצור החלוחה ופגעו בחוזק הגידולים.
מה משמעות הממצאים לחולים
בהתבוננות משולבת, העבודה חושפת מערכת ויסות בשלבים עבור סרטן קולורקטלי עשיר בחלוחה: L1TD1 מייצב את ה‑RNA של ABCC3, ABCC3 מרוקן אנרגיה תאית, מסלול AMPK–MAPK נדלק, והגידול מגיב בהפרשת עודפת של חלוחה ובהפיכה לאגרסיבי יותר ועמיד יותר לתרופות. מבחינת החולים, הדבר מציע כמה כיוונים מבטיחים. רמות L1TD1 ו‑ABCC3 עשויות לסייע לסמן גידולים שצפויים להתנהג בצורה גרועה או לעמוד בהתנגדות לכימותרפיה הרגילה. חשובה לא פחות, תרופות שמפריעות לאינטראקציה בין L1TD1 ל‑ABCC3, חוסמות את פעילות השאיבה של MRP3, או מטרות את מסלולי האיתות ההורדיים עשויות לדלל את מחסום החלוחה, להאט את גדילת הגידול ולהפוך את הטיפולים הקיימים ליעילים יותר נגד צורה מאתגרת זו של סרטן המעי הגס.
ציטוט: He, H., Yuan, J., Wang, H. et al. L1TD1 promotes colorectal mucinous adenocarcinoma progression by enhancing ABCC3 mRNA stability. Oncogene 45, 1071–1086 (2026). https://doi.org/10.1038/s41388-026-03716-w
מילות מפתח: סרטן קולורקטלי מוקינוזי, L1TD1, ABCC3 MRP3, ייצור מוקוס, התנגדות לכימותרפיה