Clear Sky Science · he
PMM2 יוצרת אינטראקציה עם TRIM28 כדי לשכור את E2F4 ולקדם גליקוליזה מוּדלת על‑ידי KIFC3 והתקדמות סרטן המעי הגס
מדוע הסיפור הזה על סרטן חשוב
סרטן המעי הגס הוא אחד מסוגי הסרטן הקטלניים בעולם, בחלקו מפני שרבים מהגידולים לומדים לפרמט את מערכות האנרגיה של הגוף כדי להזין גידול שאינו נשלט. המחקר הזה חושף כיצד אנזים מעט ידוע, PMM2, מסייע לגידולים במעי הגס לשרוף סוכר בעוצמה גבוהה ולהתפשט, ולמה זה הופך אותו למטרה מבטיחה לפיתוח תרופות ובדיקות אבחנה עתידיות.
מנוע גידולי רעב־סוכר
תאי סרטן לעתים קרובות משנים את אופן השימוש שלהם בגלוקוז, ומעדיפים צורת שריפת סוכר מהירה ופחות יעילה הידועה כגליקוליזה. החוקרים החלו בהשוואה של אלפי גנים בדגימות גידול של המעי הגס לעומת רקמה סמוכה תקינה. PMM2, אנזים שמשתתף בדרך כלל בהצמדת שרשראות סוכר לחלבונים, בלט כאחד הגנים שמעלים את הביטוי שלהם בצורה החזקה ביותר בסרטן. תאי גידול עם עודף PMM2 גדלו מהר יותר, יצרו יותר מושבות והתפשטו ביתר קלות במעשׂה מעבדה, בעוד שתאים שבהם מכבו את PMM2 האטו את קצב הגדילה שלהם, נדדו פחות והיו נוטים למות יותר.
כיצד תאי הגידול מטעינים את השימוש בסוכר
כשהצוות הפחית את רמות PMM2 בתאי סרטן המעי הגס, התאים לקחו פחות גלוקוז, ייצרו פחות ATP (מטבע האנרגיה העיקרי שלהם) ושחררו פחות לקטאט, תוצר הפסולת של הגליקוליזה. מדידות מטבוליות רגישות אישרו כי החמצת המדיום שמסביב ירדה, בעוד השימוש בחמצן עלה, כלומר התאים עברו משימוש גליקוליטי מוגבר לנשימה תקינה יותר. חלבונים מסייעים מרכזיים בגליקוליזה, PKM2 ו‑LDHA, ירדו גם הם. באופן מפתיע, אפילו גרסה קטליטית "מתה" של PMM2 יכלה עדיין לקדם את ההתנהגות הרעבה לסוכר, מה שמראה שתפקידו של האנזים בסרטן אינו תלוי בכימיה הקלאסית שלו, אלא בקשרים שהוא יוצר בתוך התא.
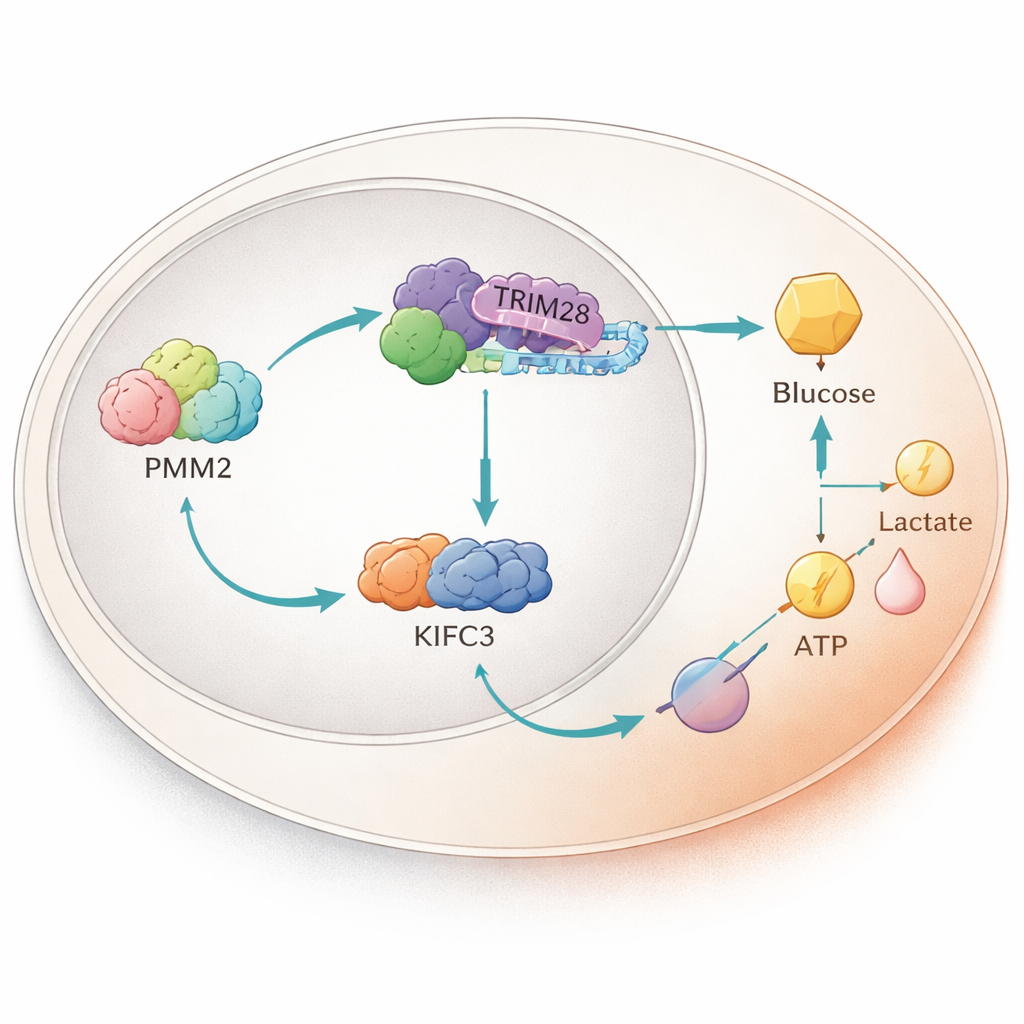
מרוצת חלבונים בתוך הגרעין
בחיפושים מעמיקים יותר, המדענים מצאו ש‑PMM2 מתחבר פיזית לחלבון אחר בשם TRIM28, שיכול לעבור אל הגרעין ולהשפיע על פעילות הגנים. PMM2 מסייע ל־TRIM28 להצטבר בגרעין, שם TRIM28 מצטרף לפקטור שעתוק, E2F4. יחד, השלישייה הזאת מגבירה את ייצורו של חלבון מנוע הנקרא KIFC3 על‑ידי קשירה לאזור בקרה ספציפי ב‑DNA שלו. ניסויים שמחקו את אזור PMM2 הנדרש לקשירה ל‑TRIM28 ביטלו את יכולתו של PMM2 להגביר את הגליקוליזה וגדילת התאים, ובכך מדגישים שזו שותפות החלבונים — ולא תפקידו האנזימטי הקלאסי של PMM2 — שמעניקה יתרון לגידול.
הדלקת מתג מטבולי מרכזי
KIFC3, שמוכר יותר בשל תפקידו בהנעת מטען לאורך השלד התאי הפנימי, התגלה כמתג מטבולי חיוני. כשהחוקרים הורידו את רמות KIFC3, תאי סרטן המעי הגס צרכו פחות גלוקוז, ייצרו פחות ATP ולקטאט, והפעילות הגליקוליטית שלהם נחלשה, בעוד שהשימוש בחמצן עלה. חשוב לציין, השתקת KIFC3 ביטלה חלקית את ההגברה בגליקוליזה ואת יתרון הגדילה שבאופן רגיל נגרמים על‑ידי PMM2. בעכברים הושתלו בהם תאי סרטן אנושיים של המעי הגס, גידולים עם עודף PMM2 גדלו גדולים יותר, אך אפקט זה הוחלש כאשר KIFC3 הושתק. דגימות הגידול מהחיות הראו רמות גבוהות של PMM2, KIFC3 וסימני גליקוליזה, וקשרו את שרשרת האירועים בחומר חי.
מדגמי מעבדה לדגימות מטופלים
כדי לקרב את העבודה לקליניקה, הצוות יצר גידולים תלת־ממדיים זעירים, ארגנוֹאידים, מתוך סרטן המעי הגס של מטופלים. ארגנוֹאידים עם רמות גבוהות של PMM2 ו‑KIFC3 גדלו מהר יותר וייצרו יותר ATP ולקטאט מאשר אלו עם רמות נמוכות. הכפלת הביטוי של PMM2 בארגנוֹאידים העלתה את KIFC3 והגליקוליזה, בעוד שהפחתת PMM2 הובילה להשפעות ההפוכות. ניתוחי מערכי גידולים של מטופלים הראו בנוסף שרמות גבוהות של PMM2 נקשרו למחלה מתקדמת יותר, לפיזור בבלוטות הלימפה ולתוחלת חיים קצרה יותר באופן כללי, ובכך מייצגות את PMM2 כמועמד חזק לסמן ביולוגי.
מה משמעות הממצאים לטיפול עתידי
במילים פשוטות, המחקר מראה כי רבים מהגידולים במעי הגס נוטים לשלב את PMM2 בשרשרת חלבונית גרעינית — דרך TRIM28 ו‑E2F4 — כדי להגביר את KIFC3 ובכך את מנוע שריפת הסוכר שלהם. ההתפרצות המטבולית הזאת מסייעת לגידולים לגדול ולהתפשט. מאחר שדרך זו תלויה באינטרקציות בין חלבונים ולא בתפקיד האנזימטי הקלאסי של PMM2, היא פותחת דרכים טיפוליות חדשות: מולקולות קטנות, פפטידים או חומרים מתכלים (degraders) שיפריעו לקשירת PMM2 ל‑TRIM28, יחסמו את גישת E2F4 ל‑DNA, או יחלישו את פעילות KIFC3 עשויים, עקרונית, לשלול מהגידולים את הדלק המועדף עליהם. אף על פי שטיפולים כאלה אינם זמינים עדיין, שרשרת PMM2–TRIM28–E2F4–KIFC3 בולטת כמפת דרכים מבטיחה לאסטרטגיות מדויקות וממוקדות מטבוליזם נגד סרטן המעי הגס.
ציטוט: Peng, Z., Ma, B., Song, Z. et al. PMM2 interacts with TRIM28 to recruit E2F4 and promote KIFC3-mediated tumor glycolysis and colorectal cancer progression. Oncogene 45, 1145–1160 (2026). https://doi.org/10.1038/s41388-026-03707-x
מילות מפתח: סרטן המעי הגס, מטבוליזם גידולי, גליקוליזה, איתות אונקוגני, סמן ביולוגי