Clear Sky Science · he
הקשר בין רטינואידים, קולטני חומצה רטינואית ואפיגנטיקה בסרטן השד
מדוע ויטמין A חשוב בסרטן השד
רוב האנשים מכירים את ויטמין A כחומר חיוני לראייה, אך הצורה הפעילה שלו בגוף, חומצה רטינואית, מסייעת גם לתאים להחליט אם לגדול, להתמחות או להיכנס לאפופטוזה כשניזוקו. מאמר סקירה זה בוחן כיצד חומצה רטינואית ו"עמדות העגינה" שלה בתאים משתנות בסרטן השד, מדוע תוצאות מבטיחות במבחנה לא תורגמו עדיין לתרופות מוצלחות בחולים, וכיצד תובנות חדשות לגבי "התוכנה" של התא הסרטני — קודו האפיגנטי — עשויות להחיות אסטרטגיית טיפול זו.
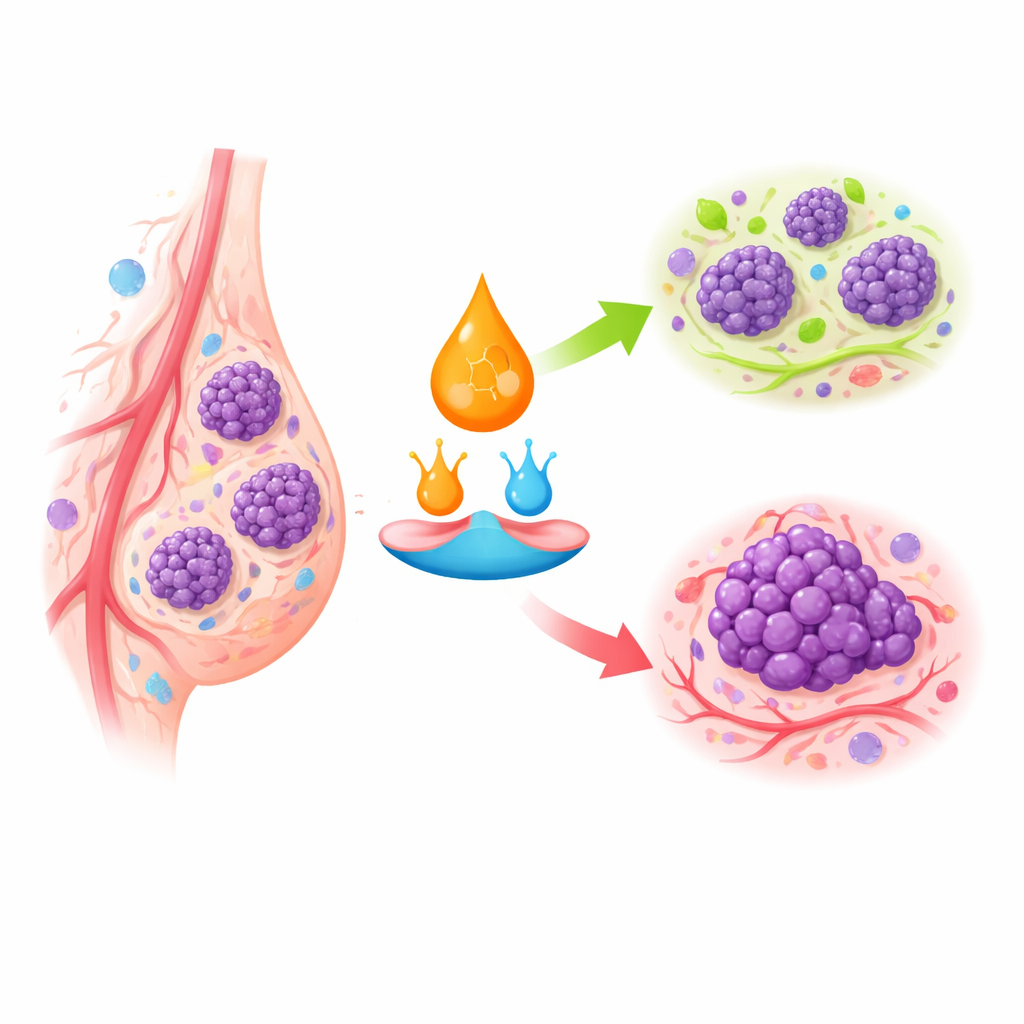
אורות תנועה תאיים לצמיחה ולאבדן־חיים
חומצה רטינואית פועלת על ידי קשר לקולטנים מסוימים בתוך התאים, שמאחרים מפעילים או מדכאים קבוצות גנים שלמות. ברקמת השד הבריאה המערכת הזו מעודדת תאים להפסיק להתחלק, להתבגר לצורות יציבות, או למות אם נהפכים לא תקינים. בסרטן השד, במיוחד בתתי־הסוגים התוקפניים יותר, קולטנים מרכזיים חסרים או מדוכאים, וההובלה הפנימית של חומצה רטינואית משתנת. במקום להישלח לקולטנים שמעכבים צמיחה, היא עלולה להיות מנותבת למסלולים המעודדים הישרדות וריבוי. זה מסביר מדוע כמה גידולי שד כמעט ואינם מגיבים לתרופות רטינואידים אף על פי שהן יעילות מאוד בסוגי סרטן דם מסוימים.
מחליפים נסתרים בתוכנת התא הסרטני
המחברים מתמקדים באפיגנטיקה — תגיות כימיות על ה‑DNA ועל חלבוני האריזה שלו המתפקדות כהגדרות תוכנה עבור הגנום. ברבים ממקרי סרטן השד תגיות אלו נועלות קולטנים חשובים לחומצה רטינואית, במיוחד אחד הנקרא RARβ2, במצב "כבוי" מבלי לשנות את רצף ה‑DNA עצמו. קבוצות מתיל נוספות על ה‑DNA והידוק של חלבוני הכרומטין סוגרות את הקולטן הזה, בעוד ששקעים אנזימטיים אחרים מעצבים מחדש את נוף הכרומטין לטובת צמיחה והגירה. רנ״א שאינו מקודד לחלבון, שמשפיע על פעילות גנים, משנים אף הם את האותות הרחק מהכוונה למות או להתמיינות. יחד, שינויים אלה מעניקים לתאי הסרטון גמישות לעמוד בפני טיפול ולהתאים ללחץ.
חיווט מחדש של מסלולי האות
חשוב שהנעילות האפיגנטיות הללו הפיכות. במודלים במעבדה, תרופות שמסירות מתילציה של DNA או מרפות את הכרומטין יכולות לשחזר את RARβ2 ורכיבים אחרים של מסלול חומצה רטינואית. בשילוב עם חומצה רטינואית עצמה וכימותרפיה סטנדרטית, סוכני "ההכנה" האלה מקטינים גידולים ביעילות רבה יותר ומפחיתים את מאגר התאים הדמויי־שחלה החשוב להישנות. גם הדרך שבה חומצה רטינואית מועברת בתוך התא חשובה: חלבון נשא אחד מכוון אותה לקולטנים המדכאים צמיחה, בעוד אחר מספק אותה למסלולים המעודדים גדילה. שינוי האיזון בין הנשאים הללו יכול להפוך את חומצה רטינואית מפעולה בדומה לדשן לפעולה כבלם.
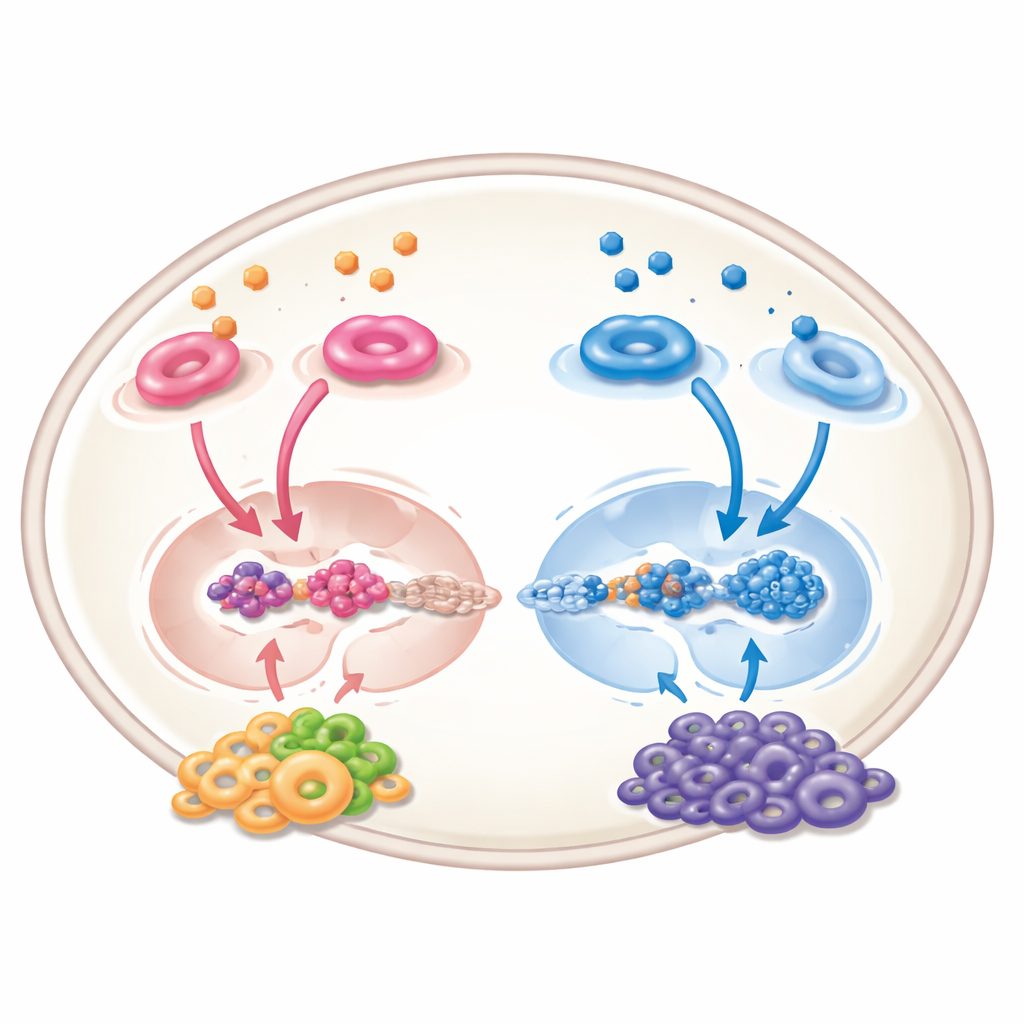
מעבר לגידול: השפעת השכונה
חומצה רטינואית אינה פועלת אך ורק על תאי הסרטן; היא גם משנה את "השכונה" הסובבת את הגידול — כלי דם, תאי חיסון ותאי תמיכה. במערכות ניסיוניות היא יכולה להפחית צמיחת כלי דם חדשים, לדחוף תאי חיסון למצב פעיל יותר המילחם בגידול, ולהגביל תאים מדכאים שמטשטשים בדרך כלל את ההגנות של הגוף. עם זאת, התמונה אינה חד־משמעית: בתאי הסטומה מסוימים המקיפים את הגידול, הפעלת איתות חומצה רטינואית עלולה לקדם דווקא את צמיחת הסרטן על ידי חיזוק ערוצי תקשורת כימיים שמושכים ותומכים בתאים ממאירים. השפעות מנוגדות אלה מחייבות שכל טיפול עתידי יהיה מדויק בהתאמתו לסוגי תאים נכונים ובאופן הנכון.
עיצוב ניסויים חכמים יותר לעתיד
ניסויים קליניים מוקדמים בתרופות רטינואיד בסרטן השד נכשלו ברובם, אך הם התקיימו לפני הבנתנו של תתי‑הסוגים, סמן־ביולוגיות ופיזיולוגיה תרופתית מורכבת. המחברים טוענים שניסויים חדשים צריכים לבחור חולים שהגידולים שלהם מגלים סימני מולקולריים לרגישות לרטינואידים, כגון שימור ביטוי קולטנים או דפוסי מתילציה ספציפיים, ולהשלב רטינואידים עם תרופות שמשחררות חסימות אפיגנטיות, מטרות מסלולי גדילה, או מחזקות את התקיפה החיסונית. פורמולציות משופרות ששומרות על רמות קבועות של התרופה בגוף, יחד עם מעקב צמוד הן אחר הגידול והן אחר הרקמה הסובבת, יהיו חיוניות. אם ניתן להתגבר על המכשולים האלה, טיפולים מבוססי חומצה רטינואית עשויים עדיין למצוא מקום ככלים מדויקים נגד צורות נבחרות של סרטן השד.
ציטוט: Szymański, Ł., Schenk, T., Ławiński, M. et al. Association of retinoids, retinoic acid receptors and epigenetics in breast cancer. Oncogene 45, 961–970 (2026). https://doi.org/10.1038/s41388-026-03699-8
מילות מפתח: חומצה רטינואית, סרטן השד, אפיגנטיקה, תרפיית התמיינות, מיקרו‑סביבה של הגידול