Clear Sky Science · he
סורטילין מפגין פעילות הדומה לדיכוי גידול על ידי הגבלת פונקציית ההעברה של EGFR
מדוע זה חשוב לטיפולי סרטן
סרטן הריאה הוא הגורם המוביל לתמותת סרטן בעולם, ורבים מהתרופות המודרניות פונות למולקולה הנקראת EGFR שמניעה את גדילת הגידול. תרופות אלה לעתים קרובות עובדות טוב בתחילה, אך הגידולים בדרך כלל מפתחים עמידות. מחקר זה חושף "בלם" טבעי בתוך תאי סרטן הריאה — תפקיד בלתי צפוי לחלבון שנקרא סורטילין — שמצליח להחליש את האותות המקדמים סרטן של EGFR. הבנת הקשר הזה עשויה לעזור להסביר מדוע חלק מהחולים מגיבים טוב יותר לטיפולים מכווני‑EGFR ולהציע דרכים חדשות לשמור על יעילות הטיפולים לאורך זמן.
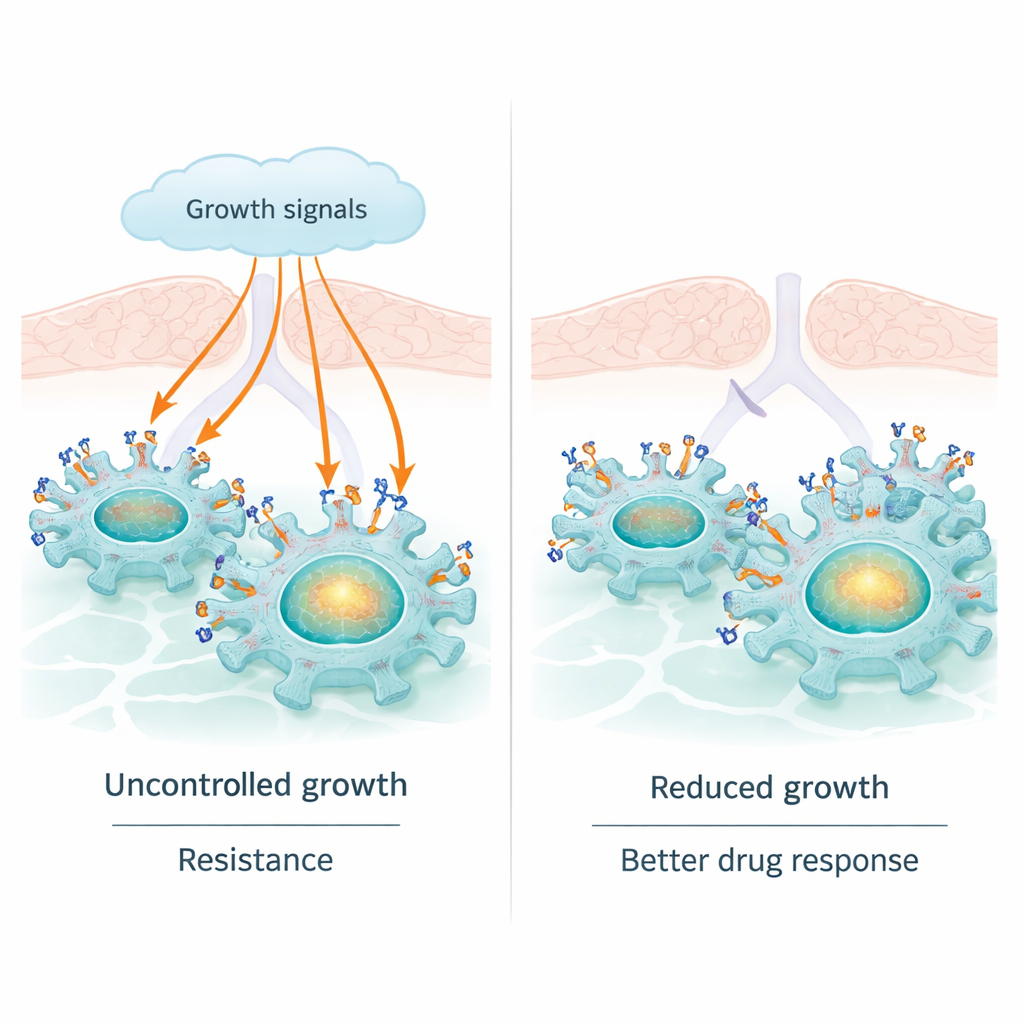
מתג גדילה שהלך למצב יתר
EGFR הוא קולטן הממוקם על פני שטח תאים רבים, ושמזהה אותות גדילה מהסביבה. בחלק גדול מאדנוקרצינומות הריאה, EGFR משתנה כך שהוא נשאר דלוק באופן קבוע. הדבר מאכיל גדילה וחלוקה מתמשכת, ולכן כדורים החוסמים את EGFR, המכונים מעכבי טירוזין קינאז, יכולים להקטין גידולים. אך ל‑EGFR יש גם תפקיד פחות מוכר: הוא יכול לנוע אל גרעין התא ולפעול ישירות על ה‑DNA, ולהפעיל גנים כגון cMYC ו‑CCND1 שמגבירים עוד יותר גדילה, שרידות ועמידות לטיפול. התפקיד הגרעיני הזה של EGFR עשוי לסייע לגידולים להימלט גם כשהפעילות שלו על פני השטח נחסמת כימית.
סורטילין נכנס לגרעין
סורטילין היה ידוע קודם לכן בעיקר כחלבון מיון המסייע בהבאה פנימה של EGFR ממעטפת התא ושולח אותו לעבר פירוק, ובכך מחליש את אותות הגדילה שלו. בעבודה זו מראים המחברים שסורטילין גם עוקב אחרי EGFR אל תוך הגרעין כאשר תאי סרטן הריאה מועצבים. באמצעות מיקרוסקופיה ברזולוציה גבוהה ופרקציית ביוכימית, הם תיעדו קומפלקסים של EGFR וסורטילין שמתגבשים בתוך הגרעינים זמן קצר לאחר ההפעלה. באופן מהותי, כאשר EGFR לא יכל להיכנס לגרעין, גם סורטילין נשאר מחוץ לגרעין, מה שמעיד ש‑EGFR משמש כ"כרטיס" של סורטילין לכניסה למחיצה זו. כשהם שם, נמצאו קומפלקסי EGFR–סורטילין קשורים לרצפי DNA בסמוך לאתרי ההתחלה של גנים מרכזיים לבקרת הגדילה, כולל cMYC ו‑CCND1.
בלם מובנה על גנים סרטניים
כדי להבין מה עושים הקומפלקסים הללו, החוקרים מיפו את האזורים שבהם הם קושרים ברחבי הגנום ומדדו שינויים בפעילות הגנים. הם מצאו ש‑EGFR לבדו נוטה לקדם את הפעלת הגנים הקשורים לגדילה, בעוד שנוכחות סורטילין באותם אזורי DNA מעכבת אפקט זה. כאשר רמות הסורטילין הוקטנו באופן מלאכותי, הקישור של EGFR לגנים היעד עלה, וגנים מזרזי סרטן כגון cMYC ו‑CCND1 הפכו ליותר פעילים. לעומת זאת, הגברת רמות הסורטילין מספרה את האפקט: אחיזתו של EGFR ב‑DNA רופפת, גיוס מכונת השעתוק פחת, והביטוי של גנים אונקוגניים אלו ירד. בעכברים, גידולי ריאה מהונדסים שמייצרים כמות עודפת של סורטילין צמחו באיטיות והציגו רמות מופחתות של cMYC ו‑CCND1.
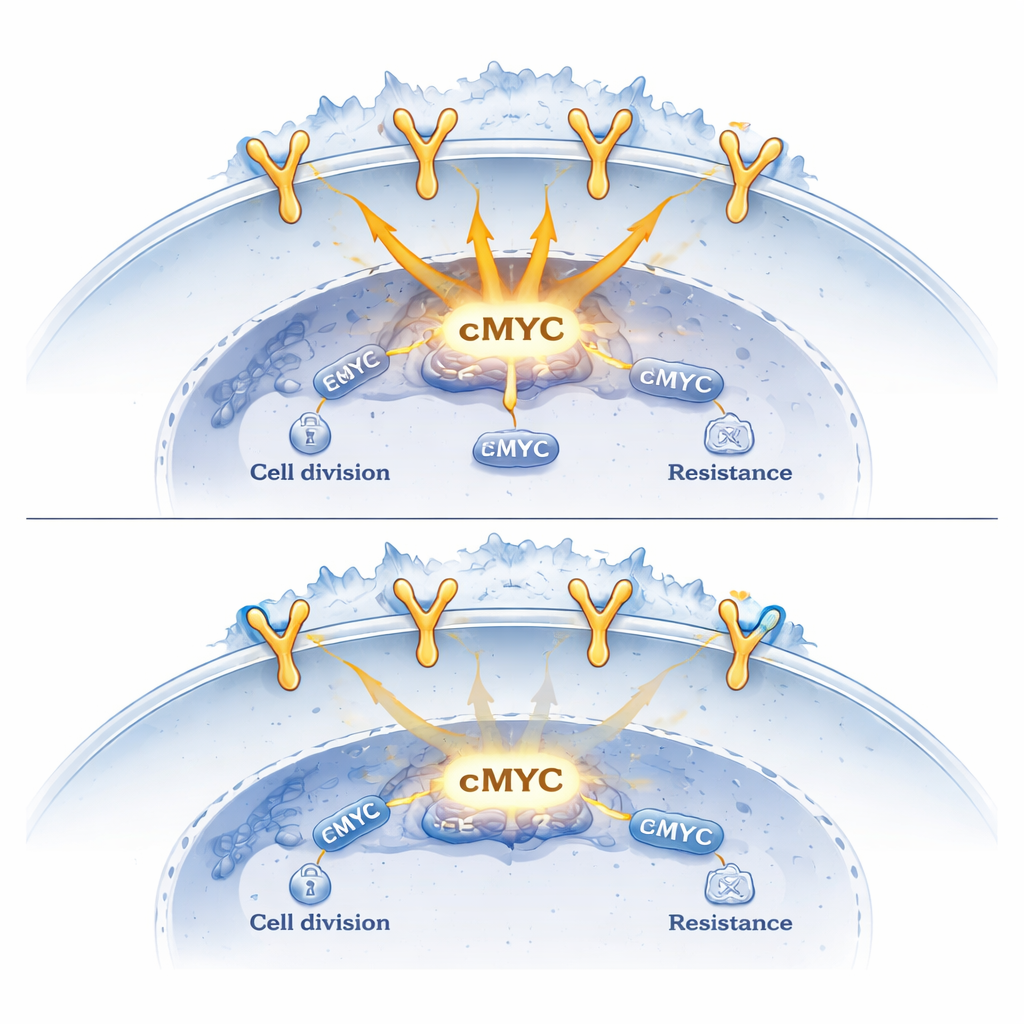
הדדיות עם תרופות ל‑EGFR
המחקר חקר גם כיצד מנגנון זה מתקשר לאוזימרטיניב, תרופה נפוצה המיועדת לחסום מוטציות בעייתיות של EGFR. באופן מפתיע, גם כאשר אוזימרטיניב כיבה את הפעילות האנזימטית של EGFR, הקולטן עדיין זז אל הגרעין. שם, הוא המשיך לקשור DNA, במיוחד בקרבת הגן cMYC. עם זאת, גם סורטילין הצטבר בגרעין בתנאים הללו. כאשר סורטילין היה בשפע, רמות cMYC ירדו יותר בתגובה לאוזימרטיניב ותאי הסרטן הפכו לפחות ברי־קיום. ניתוח של גידולים ממטופלים ובסיסי נתונים ציבוריים גדולים הראה שרמות סורטילין נמוכות לעתים קרובות באדנוקרצינומות ריאה בהשוואה לרקמת ריאה נורמלית, ושביטוי סורטילין גבוה קשור בעקביות לביטוי נמוך של cMYC.
מה המשמעות הזו עבור חולים
כאשר מסתכלים על הממצאים יחד, התמונה מציירת את סורטילין כמעין שותף בדיאלוג הדומה לחלבון מדכא‑גידול שנוסע עם EGFR אל הגרעין ומעכב אותו. על‑ידי הגבלת יכולתו של EGFR להפעיל גנים עוצמתיים לקידום גדילה כגון cMYC, סורטילין יכול להאט התקדמות גידול ולהגביר את השפעתן של תרופות החוסמות EGFR. מכיוון שלרבים מהגידולים בריאה יש רמות סורטילין מופחתות, הם עלולים להידרש מחוסר הבלם הפנימי הזה, דבר שעשוי להסביר מדוע חלק מהסרטן אגרסיבי במיוחד או מפתח עמידות במהירות. מדידת רמות סורטילין בגידולים עשויה לסייע לחזות עד כמה מטופל יגיב לטיפולים מכווני‑EGFR, ואסטרטגיות המעלות את פעילות הסורטילין יכולות להציע דרך חדשה לשמור על שליטה טובה יותר לטווח ארוך על סרטן המונע על‑ידי EGFR.
ציטוט: Lapeyronnie, E., Granet, C., Tricard, J. et al. Sortilin exhibits tumor suppressor-like activity by limiting EGFR transduction function. Oncogene 45, 875–888 (2026). https://doi.org/10.1038/s41388-026-03680-5
מילות מפתח: סרטן הריאה, EGFR, סורטילין, cMYC, עמידות לטיפולים ממוקדים