Clear Sky Science · he
גליונות ננו היברידיים של WS2 מוכתמים בנחושת עם PEG לטיפול רב‑מצבי ממוקד בסרטן
מדוע טיפולים חכמים יותר לסרטן חשובים
רבים ממטופלות וסובלות מסרטן השד עדיין נחשפים לטיפולים קשים שיכולים לפגוע ברקמה בריאה מבלי לעצור את הגידול במלואו. המחקר הזה מתאר סוג חדש של משטח זעיר ומהונדס, קטן מדי כדי להיראות בעין, שתוכנן לנוע בגוף, למקם עצמו בגידולי שד ולתקוף אותם בכמה מנגנונים מתואמים בו‑זמנית. על‑ידי שילוב חום, כימיה ותרופה קלאסית בקופסה ממוקדת אחת, המחקר שואף להפוך את הטיפול לחזק יותר ועדין יותר כלפי שאר הגוף.
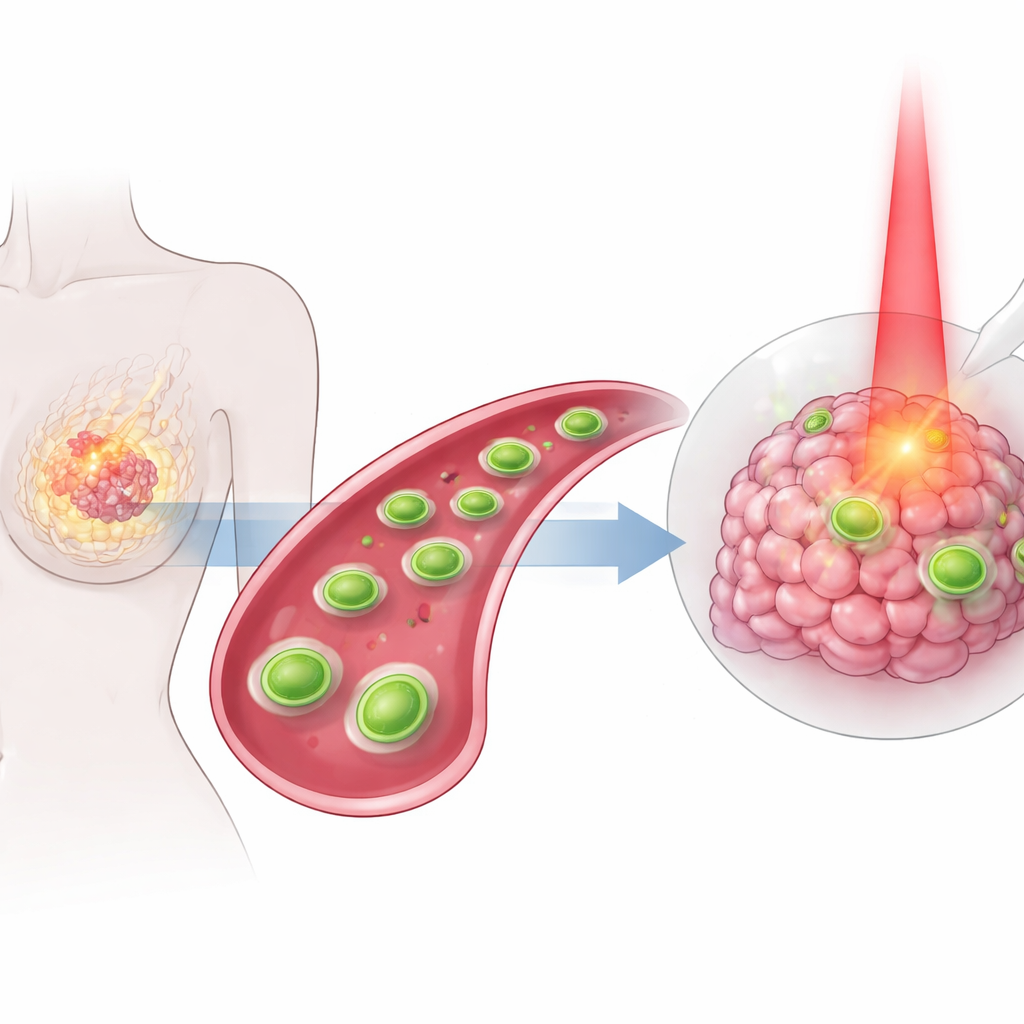
גיליונות זעירים שנבנו לשאת ולשחרר טיפול
הליבה של הגישה היא חומר על‑דק עשוי טונגסטן וגופרית, בצורת גליונות ננומטריים. גליונות אלה סופגים באופן טבעי אור תת‑אדום קרוב והופכים אותו לחום. הצוות יצר תחילה את הגליונות ולאחר מכן שטח בעדינות את פני השטח כדי שיוכלו לשאת מרכיבים שימושיים נוספים. אטומי נחושת נענו באופן מפוזר היטב על הגליונות, ונוספה ציפוי רך וגמיש בדומה ל"מעיל גשם" מולקולרי שיעזור לחלקיקים להתפזר בנוזלי גוף ולהמנע מהתקלחויות. לבסוף, קשור חומצה פולית — ויטמין שרבים מתאים סרטניים סופגים בנחישות — כמכשיר איתור, וטוענו על המשטח את תרופת הכימותרפיה הנפוצה דוקסורוביצין. התוצאה היא פלטפורמה שכבתית זעירה שיכולה להיסחף בדם, לזהות תאי גידול ולשאת מטען תרופתי משמעותי.
כיצד אור, כימיה ותרופה פועלים יחד
כאשר חלקיקים אלה מגיעים אל הגידול מתרחש מספר אירועים בו‑זמנית. כאשר אזור הגידול מואר בלייזר אדום עדין, גליונות הטונגסטן‑גופרית מתחממים ביעילות, מגבירים את הטמפרטורה המקומית במידה שמייצרת מתח ופגיעה בתאי הסרטן מבלי לחמם יתר על המידה את שאר הגוף. במקביל, אטומי הנחושת על הגליונות מגיבים עם מולקולות פרוקסיד הטבעיות שנמצאות ברמות גבוהות יותר בתוך הגידולים. תגובה זו ממירה את הפרוקסיד לחמצונים агresיביים קצרים‑מועד הפוגעים במרכיבים תאיים מבפנים. גידולים גם נוטים להיות מעט חומציים יותר מרקמה בריאה; בסביבה החומצית הזו, ותחת חימום באמצעות הלייזר, הקשר בין המשטח לדוקסורוביצין נחלש, ומאפשר שחרור גדול יותר של התרופה בדיוק במקום שבו היא דרושה. שלושת ההשפעות הללו — חום, התקפה כימית וכימותרפיה ממוקדת — תוכננו לחזק זו את זו.
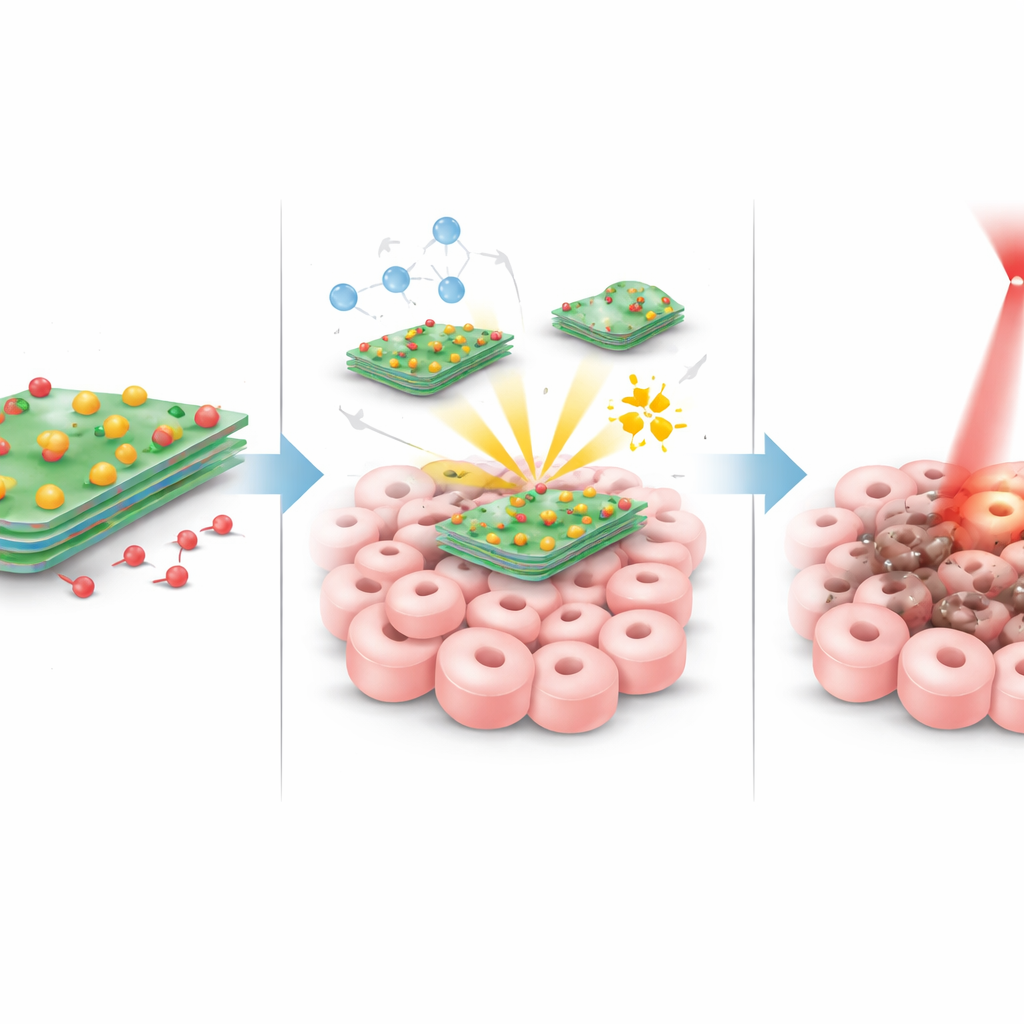
עדויות מתאים ובעכברי גידול
בצלחות מעבדה, הגליונות המצופים עצמם הראו מעט נזק לתאים נורמליים, דבר המרמז על בטיחות בסיסית טובה. אך כשהם טענו בדוקסורוביצין והוארו בלייזר בנוכחות פרוקסיד, הם גרמו למות חזק של תאי סרטן השד, הרבה יותר מכל טיפול יחיד. החוקרים גם הראו שהחלקיקים מייצרים זינוק של חמצונים פעילים בתוך תאי הגידול, מאשר שהכימיה של הנחושת פעילה. בעכברים נשאים של גידולים בחזה, חלקיקים המצופים בחומצה פולית הצטברו חזק יותר ולפרק זמן ארוך יותר ברקמת הגידול בהשוואה לחלקיקים לא‑ממוקדים. כאשר העכברים קיבלו את השילוב המלא — חלקיקים ממוקדים בתוספת חשיפת אור אדום — הגידולים הצטמצמו בצורה דרמטית, משך החיים שלהם גדל, ומשקל גופם ובריאות האיברים נותרו ברובם תקינים, דבר שמרמז על תופעות לוואי מוגבלות בהשוואה לטיפול תרופתי סטנדרטי.
מה זה עלול לסמן לטיפול עתידי בסרטן
בהרכבה כללית, הממצאים מציעים כי גליונות מהונדסים אלה פועלים כמרבב כלים לטיפול בסרטן: הם מחפשים גידולים, מחממים אותם, מרעילים אותם מבפנים באמצעות כימיה תגובתית ומספקים תרופה מבוססת באופן מדויק יותר, תוך כדי פגיעה מועטה יותר בשאר הגוף. העבודה עדיין נמצאת בשלב מחקר בעל חיים, ונשארות שאלות חשובות לגבי בטיחות לטווח ארוך, פירוק וכיצד לייצר חלקיקים כאלה לשימוש אנושי. עם זאת, העיצוב מדגים כיצד שילוב של מספר טיפולים ממותנים בחבילה חכמה אחת המותאמת לסביבת הגידול יכול לייצר אפקט כולל הרבה חזק יותר. אם מחקרים עתידיים יאמתו את בטיחותם ויעילותם, פלטפורמות ננומטריות רב‑תכליתיות כאלה עשויות לעזור להפוך את טיפול בסרטן השד ליותר ממוקד, יעיל ופחות מכאיב למטופלות.
ציטוט: Li, D., Wen, C., Wu, H. et al. PEGylated Cu-doped WS2 hybrid nanosheets for targeted multimodal cancer therapy. Microsyst Nanoeng 12, 121 (2026). https://doi.org/10.1038/s41378-026-01218-z
מילות מפתח: טיפול בסרטן השד, ננו‑רפואה, טיפול פוטו‑תרמי, העברת תרופות ממוקדת, טיפול כימודינמי