Clear Sky Science · he
JAK2V617F משנה את תפקוד גורם הרגישות לחמצן HIF-1 לגרום לרגולון היפוקסי לא‑סטנדרטי במיאלופרוליפרטיב ניאופלזיות
מדוע זה חשוב לסרטן הדם
חלק מסוגי סרטן הדם האיטיים, המוכרים כמיאלופרוליפרטיב ניאופלזיות, יכולים לבעור בלי סימן למשך שנים לפני שמיד לפתע עוברים ללוקמיה תוקפנית. המחקר שואל שאלה פשוטה אך מכרעת: כיצד מוטציה נפוצה שמניעה סרטן חוטפת את מערכת החישה הפנימית של התא לחמצן, והאם ניתן לכוון את החטיפה הזו באופן סלקטיבי מבלי לפגוע בתאים בריאים? התשובות עשויות לפתוח דרך חדשה לטיפול בחולים בסיכון גבוה תוך שמירה על רקמות תקינות שתלויות גם הן באיתותי חישה לחמצן.
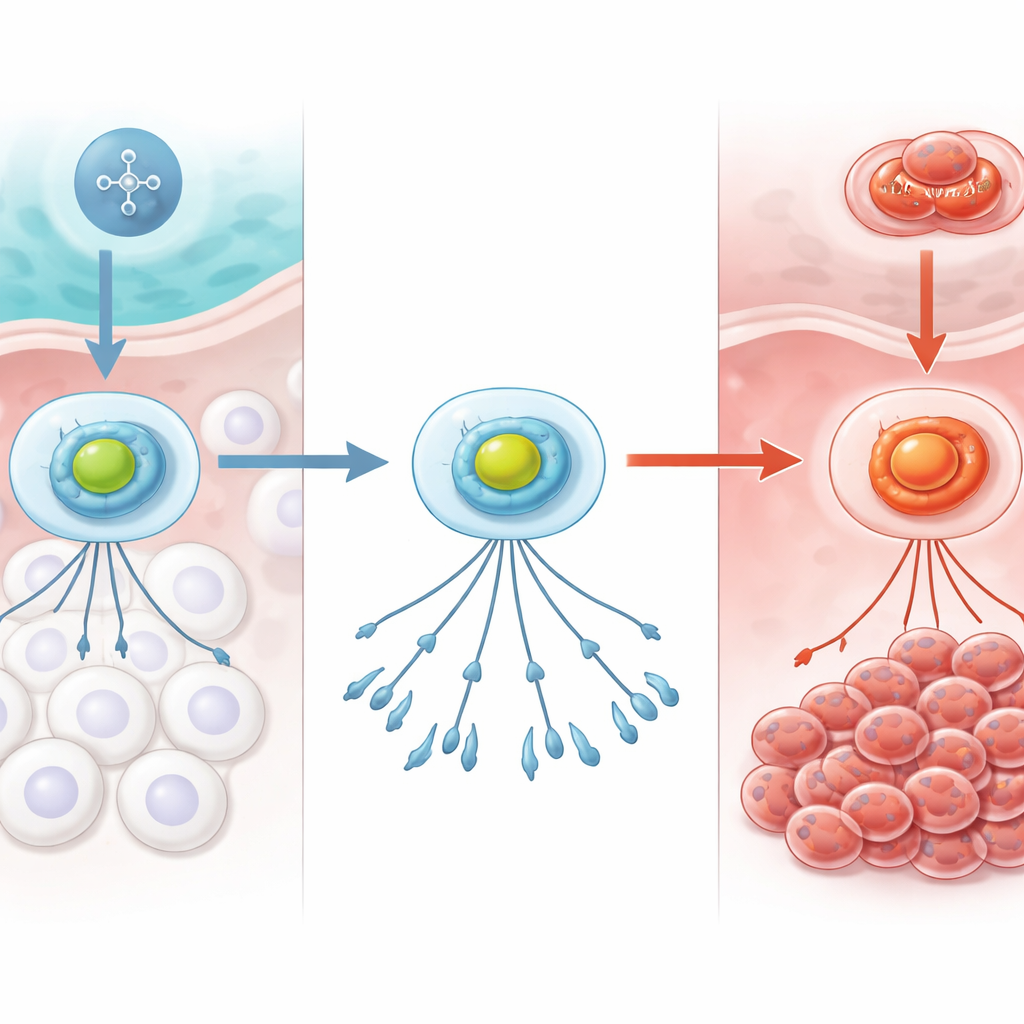
מערכת האזעקה של הגוף לחמצן
תאים עוקבים באופן רציף אחרי כמות החמצן הזמינה. בלב מערכת זו עומד קומפלקס חלבוני בשם HIF‑1, שמתפקד כמו אזעקת חמצן. בתנאים נורמליים ומאובטחים בחמצן, תת‑יחידה של HIF‑1 מתפרקת במהירות וכך האזעקה כבויה. כאשר רמת החמצן יורדת, הפירוק נפסק, HIF‑1 מתייצב, נע אל ה‑DNA של התא ומפעיל גנים המסייעים להסתגלות — למשל על ידי שינוי השימוש באנרגיה או עידוד יצירת כלי דם חדשים. בסרטן, אותה מערכת יכולה לפעול לטובת הגידול, ועוזרת לתאים ממאירים להתמודד עם סביבות מלחיצות כגון מוח העצם דל‑החמצן.
כאשר מוטציה משנה את האזעקה
החוקרים התמקדו במוטציה בשם JAK2V617F, שכיחה מאוד במיאלופרוליפרטיב ניאופלזיות. עבודות קודמות הראו כי מוטציה זו משאירה את אזעקת HIF‑1 דלוקה גם כאשר יש חמצן בשפע. בעזרת תאי מעבדה מהונדסים, הקביצה השוותה את מקומות הקשירה של HIF‑1 ל‑DNA בשתי מצבים: חוסר חמצן אמיתי, וחמצן נורמלי בנוכחות המוטציה JAK2V617F. הם מצאו שבתאים המוטנטיים HIF‑1 נקשר למקומות מעטים יותר בגנום, מגיב פחות לשינויים בחמצן, ומתקשר עם מערך שונה של שותפי חלבון, רבים מהם משתתפים בעיבוד RNA. במילים אחרות, המוטציה אינה רק מדליקה את HIF‑1 באופן קבוע — היא מכווננת את האזעקה למערך שונה של מטרות.
תוכנית גנים ספציפית לסרטן
מהניסויים הללו הגדירו המחברים מספר קבוצות גנים התלויות ב‑HIF‑1, כולל אחת שהם כינו חתימת היפוקסיה JAK2V617F. לאחר מכן בדקו עד כמה חתימות אלה פעילות בתאי דם מ‑172 חולים עם מיאלופרוליפרטיב ניאופלזיה חיובית ל‑JAK2V617F. להפתעתם, תוכניות הגנים הרגילות של HIF‑1 באי‑חמצן לא חזו את חומרת המחלה או את אורך החיים של החולים. בניגוד לכך, חתימת ההיפוקסיה הספציפית למוטציה הפרידה בבירור חולים עם מחלה קשה יותר וקושרה להישרדות כללית גרועה יותר. רבים מהגנים בקבוצה זו היו פעילים במיוחד בפרוגניטורים של מגהקריוציטים — תאי מוח העצם שמתרבים וגורמים לצלקת במחלה — וכמה היו מעורבים בתיקון נזקי‑DNA, תהליך שיכול לסייע לתאי סרטן לשרוד סטרסים מזיקים.
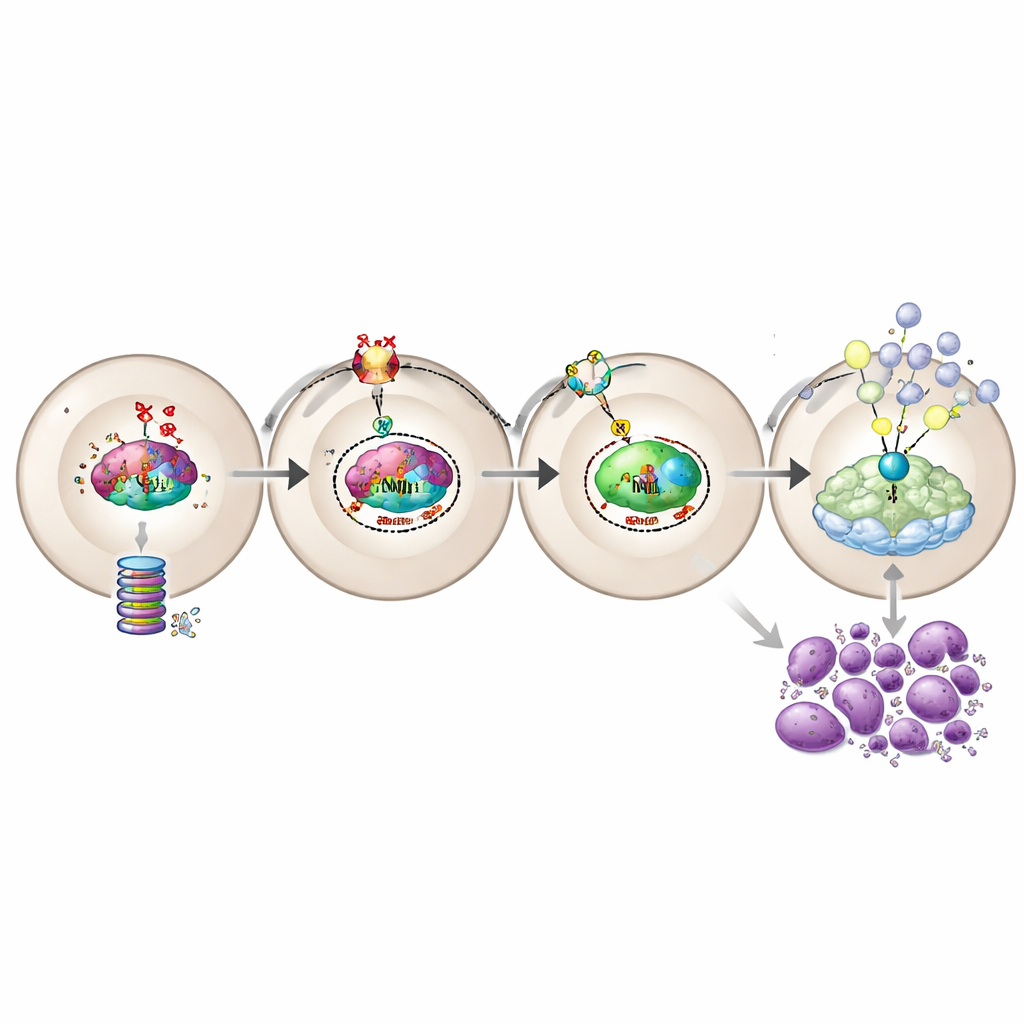
רמזים להחמרה פתאומית של המחלה
חשש מרכזי לחולים הוא המעבר הפתאומי ממחלה כרונית ללוקמיה תוקפנית בשלב זליגי. בניתוח דגימות תואמות מחולים לפני ואחרי השינוי, הקביצה זימזה תת‑קבוצה קטנה בת 13 גנים, שכינויה חתימת HIF1‑MPN‑BP, שעלתה או ירדה בהתאמה להמרה. תת‑קבוצה זו נקשרה בחוזקה לציוני סיכון גבוהים יותר, להישרדות גרועה יותר ולצלקת מח עצם מוגברת. באופן חשוב, דפוס זה נראה ספציפי למחלה המונעת על ידי JAK2V617F, ולא תכונה כללית של כל הלוקמיות. רבים מהגנים בתת‑קבוצה נראים כמטרות סבירות לתרופות, ומציעים רשימת מועמדים ממוקדת לטיפולים עתידיים שמטרתם לחסום התקדמות.
מוצא העוזר החבוי של המוטציה
כיצד JAK2V617F שומר על HIF‑1 פעיל באופן בלתי תלוי בחמצן? באמצעות שיטות בכימיה של חלבונים גילו המחברים שבתאים המוטנטיים HIF‑1 נושא שתי תגיות כימיות חדשות (זרחונים) בתוך אזור שבדרך כלל שולט על פירוקו. הם ייחסו שינויים אלה ל‑PIM1, קינאז שמופעל במורד איתות ה‑JAK2. חסימת PIM1 בעזרת תרופות ניסיוניות הורידה את רמות HIF‑1 בתאים המוטנטיים, אך השאירה את תגובת האי‑חמצון הנורמלית ברובה שלמה. גם עיכוב PIM1 צמצם באופן סלקטיבי את ביטוי גני HIF1‑MPN‑BP המסכנים ודחף תאים מוטנטיים לכיוון מוות תאי, בעוד הוא חסך את התאים הלא‑מוטנטיים.
מה משמעות הדבר לחולים
המחקר מראה כי אותו חלבון חישה לחמצן, HIF‑1, מתנהג בצורה שונה מאוד בהתאם לאופן ההפעלה שלו. במיאלופרוליפרטיב ניאופלזיות המונעות על ידי JAK2V617F, ציר האיתות JAK2–PIM1 מייצב את HIF‑1 בצורה שמתנתקת מבקרת החמצן הרגילה ומצמצמת את פעילותו לקבוצת גנים המקדמת מחלה. מכיוון שהתוכנית המשוננת הזו קשורה באופן הדוק לחומרת המחלה ולסיכון להמרה, וניתנת להשקטה על‑ידי חסימת PIM1, היא מציעה נתיב מבטיח למיקוד פעילות HIF‑1 הממאירה תוך שמירה על תפקידו החיוני ברקמות בריאות. טיפולים המנצלים את ההבחנה הזו עשויים בעתיד לעזור למנוע ממחלת דם איטית להעשות ללוקמיה מסכנת חיים.
ציטוט: Kealy, D., Ellerington, R., Bansal, S. et al. JAK2V617F reprograms Hypoxia Inducible Factor-1 to induce a non-canonical hypoxia regulon in myeloproliferative neoplasms. Leukemia 40, 609–621 (2026). https://doi.org/10.1038/s41375-025-02843-9
מילות מפתח: מיאלופרוליפרטיב ניאופלזיות, JAK2V617F, HIF-1, קינאז PIM1, המרה לשלב זליגתי