Clear Sky Science · he
השתלה מעוררת פוטנציאל אוסטאוגני פריא-אימפלנטרי דרך תמסורת מכנית מווסתת על ידי ציר Snx5‑EGFR
מדוע חשוב לשמר את עצם הלסת לאחר אובדן שן
כאשר שן נוצרת, עצם הלסת הסובבת נוטה להתכווץ, מה שמקשה על הצבת שתלים דנטליים יציבים מאוחר יותר ומשפיע על המראה הפנים. רופאי שיניים התבוננו זמן רב בכך שהצבת שתל בחלל לאחר עקירה נראית כמשמרת את העצם, אפילו לפני שהשתל משולב בתפקוד לעיסה. המחקר הזה שואל שאלה פשוטה אך מהותית: כיצד פעולת ההשתלה עצמה "מפעילה" את מערכת התיקון של העצם, והאם אפשר לנצל תהליך זה כדי לשפר שיקום עצם הלסת?
שתלים כמגני עצם שקטים
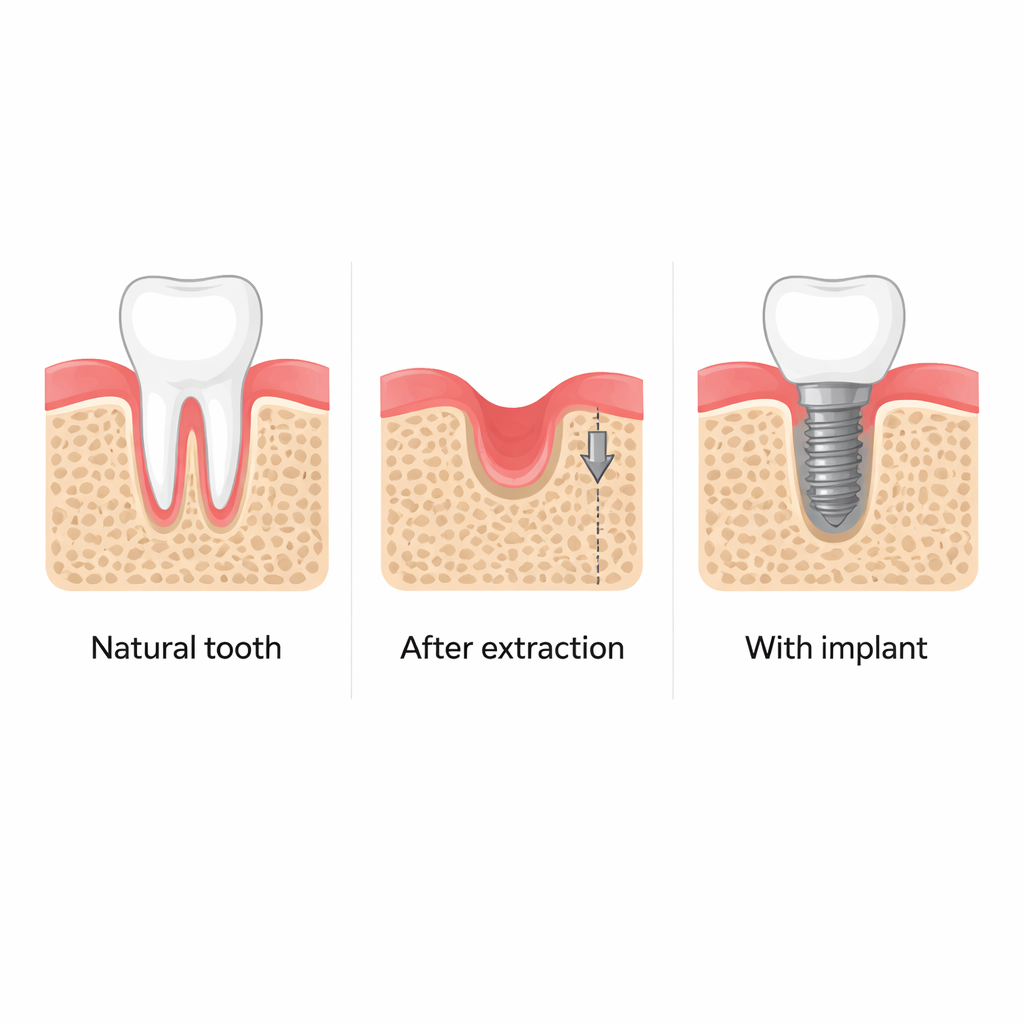
סריקות קליניות של מטופלים וניסויים מפורטים בעכברים מאשרים שהצבת שתל דנטלי זמן קצר לאחר עקירה מסייעת לשמור על גובה ועובי עצם הלסת הסובבת. לעומת זאת, חללים שנשארו להחלים בעצמם מאבדים כמות משמעותית של עצם לאורך מספר חודשים. סביב השתלים מצאו החוקרים יותר תאי אב אוסטאוגניים בלתי בשלים (אוסטאופרוגניטורים), שמעידים שהתשומה הביולוגית של הרקמה לצד העמוד המתכתי גבוהה יותר. פעילות משופרת זו אינה נראית מונעת על‑ידי כוחות לעיסה, אלא על ידי המתח המכניקלי הייחודי שנוצר כששתל הדוק נוקבע לתוך עצם שגודלה מעט קטן יותר.
מתג נסתר בתוך תאי גזע של העצם
הצוות התמקד בקבוצת תאי מיאלופואטיים במח העצם המסומנים בחלבון בשם LepR, הידועים כמקור מרכזי לעצם חדשה במבוגרים. בהשוואת פעילות גנים בתאים אלה מתוך עצם רגילה, עצם צמודה לשתל ותאים שנחשפו למתח במעבדה, הם זיהו מולקולה אחת — sorting nexin 5 (Snx5) — שרמותיה ירדו בעקביות כשהיו נוכחים איתותים מכניים. באזורים סביב השתלים, תאי LepR עם Snx5 נמוך נטו יותר לשאת סמנים של תאי בניית עצם מוקדמים, מה שמרמז שהפחתת Snx5 מסייעת לדחוף את תאי הגזע השקטים האלה למצב פעיל של יצירת עצם.
כשמתג השינוי שבקוי, העצם לא חשה כוח כראוי
כדי לבחון מה עושה Snx5 בפועל, השתמשו החוקרים בעכברים ובתאי גזע חסרי חלבון זה. ללא Snx5, תאי הגזע הראו נטייה פנימית חזקה לייצר עצם, אפילו ללא גירוי נוסף. אך כאשר המדענים החילו מתיחה מכנית — המדמה את המתח באזור השתל — התאים הרגילים הגבירו את פעילות בניית העצם, בעוד שתאי חסרי Snx5 כמעט שלא הגיבו. בעכברים חיים, שתלים בחיות רגילות עוררו יצירת עצם חדשה ברורה סביב העמוד הטיטניום. לעומת זאת, בעכברים ללא Snx5 לא נצפה גידול עצם נוסף אחרי ההשתלה, מה שמוכיח כי Snx5 חיוני להמיר אותות מכניים לתגובה של תיקון עצם נוספת ולאו דווקא ליצירת עצם בסיסית.
איך מסלול מיחזור שולט באותות העצם
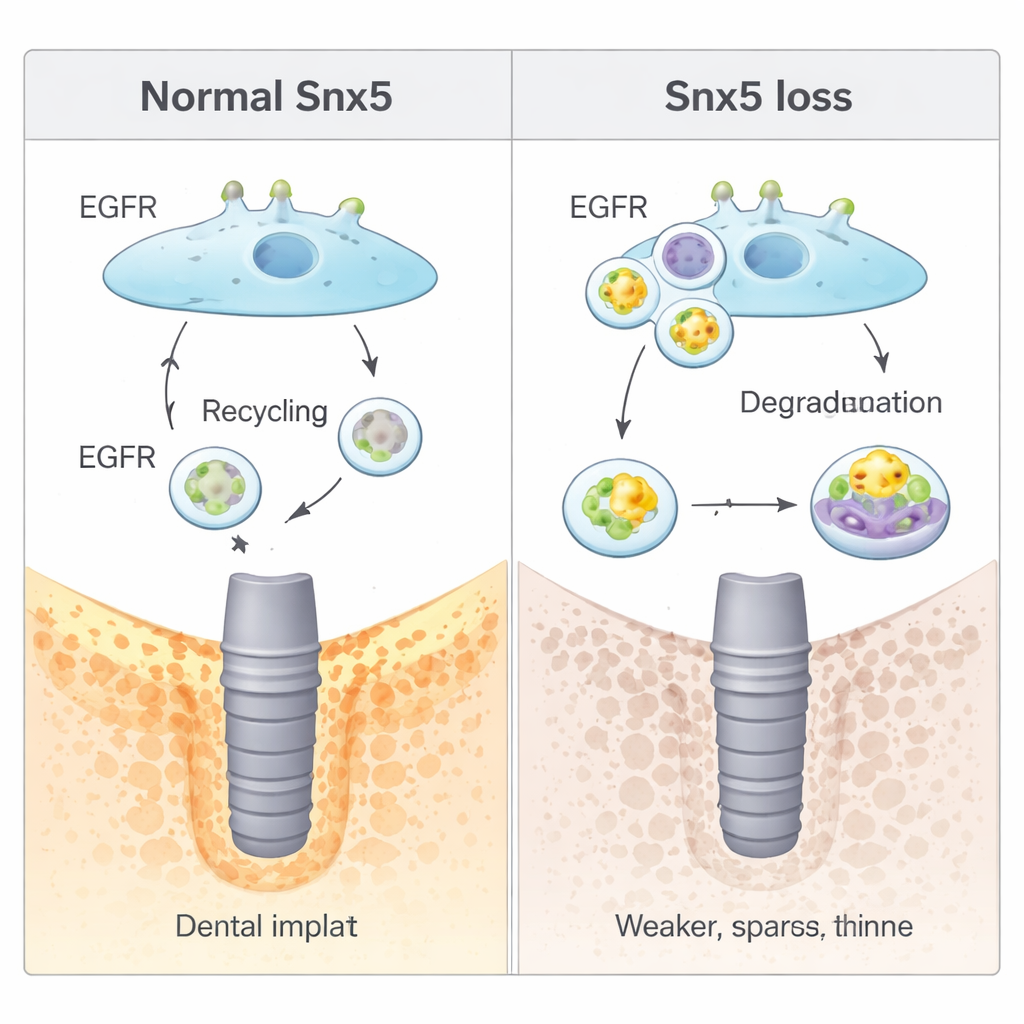
המחקר חשף לאחר מכן כיצד Snx5 פועל ברמת המולקולות. רבים מהאותות הגדילה בתאים עוברים דרך קולטנים על פני התא שנשאבים פנימה וממופים בין מיחזור להרס. Snx5 שייך למשפחה של חלבוני "מיון" המכוונים את התנועה הזו. כאן הראו כי Snx5 מנווט את קולטני גורם הגדילה האפידרמלי (EGFR) — בקרים מרכזיים של גדילה תאית והבחנה לעצם — חזרה לממברנת התא לאחר קליטתם. כשהיה חסר Snx5, עוד EGFR הוסטו למחלקות "עיכול" תאיות (ליזוזומים) והפורקו. זה הפחית את אותות EGFR ובאופן בלתי צפוי הגביר את יצירת העצם הבסיסית, אך השאיר את התאים פחות מסוגלים להתאים את התנהגותם כאשר כוחות מכניים השתנו. תרופות שהפעילו באופן מלאכותי את EGFR דיכאו את יצירת העצם העודפת שנראתה בחוסר Snx5, בעוד שתרופות שחסמו פירוק ליזוזומלי שיחזרו את אותות EGFR והקטינו שוב את בניית העצם.
מה המשמעות למטופלי השתלים בעתיד
לאדם מן השורה, ממצאים אלה מציעים שעצם הלסת מכילה מערכת מובנית היכולה לחוש את הלחץ והמתיחה העדינים שנוצרים כאשר שתל מופעל ולתרגם אותם לצמיחת עצם נוספת. Snx5 משמש כבודק תנועה ששומר על מחזור נכון של קולטן הגדילה המרכזי, EGFR, כך שתאי גזע העצם יוכלו "לשמוע" ולהגיב ל׳לחישות׳ המכאניות הללו. כאשר הבודק הזה משתנה, העצם עשויה להיווצר ביתר קלות במנוחה אך לא תוכל להגיב בדייקנות לכוחות. הבנת ציר Snx5–EGFR פותחת פתח לטיפולים חדשים — תרופות או ציפויים חיצוניים לשתלים — שיכולים לכוונן את רגישות העצם למכניקה, לסייע בשימור עצם הלסת ולשפר את הצלחת השתלים במצבים קליניים מאתגרים.
ציטוט: Jiang, X., Weng, Y., Feng, Y. et al. Implantation awakens peri-implant osteogenic potential via Snx5-EGFR axis-mediated mechanical transduction. Int J Oral Sci 18, 18 (2026). https://doi.org/10.1038/s41368-025-00423-2
מילות מפתח: שתלים דנטליים, שחזור עצם בלסת, מכנוטרנסдукציה, תאי גזע עצם, אותות EGFR