Clear Sky Science · he
תובנות מבניות על מוטציות הקשורות למחלה במכונות עיבוד ה-microRNA
איך מספריים זעירים של RNA מעצבים בריאות ומחלה
בתוך כל תא פועל מערכת עריכה נסתרת שמגזרת מסרים גנטיים לפני שהם נקראים. מערכת זו נשענת על מקטעי RNA זעירים שנקראים microRNA, שממלאים תפקיד של כפתורי כיוונון עדינים עבור אלפי גנים בו־זמנית. כשה"מכונות" המולקולריות שמייצרות את ה-microRNA פועלות כשורה, התאים גדלים, מתחלקים ומתמחים בצורה מבוקרת. אבל כאשר מכונות אלה ניזוקות על ידי מוטציות, מאזן הפעילות הגנטית עלול להתהפך ולהוביל לסרטן, להפרעות דם או לבעיות בהתפתחות המוח. מאמר זה מסביר כיצד הבנת הצורות התלת־ממדיות של המכונות האלה עוזרת למדענים לזהות מה משתבש ואילו דרכים עשויות לתקן זאת.
ערכת ההחשכה הגנטית של התא
microRNA הן חתיכות קצרות של RNA, באורך של כ־22 אבני בניין, שאינן מקודדות לחלבונים בעצמן. במקום זאת, הן נקשרות ל-mRNA ארוכים וסימנות אותם להשמדה או חוסמות את תרגומם, ובכך מכווצות את ביטוי הגנים במקום לכבותם לחלוטין. כדי לייצר microRNA אלו, התאים מעבירים קדם־RNA ארוכים דרך קו ייצור מרובה שלבים. ראשית, האנזים DROSHA חותך את הטרנסקריפים הראשוניים הגדולים בגרעין התא לחתיכות קצרות בצורת סיכות שיער. החתיכות הללו נעות לציטופלזמה, שם אנזים נוסף, DICER, מודד ובועט אותן למדוּמות דו־גדיל בגודל microRNA. לבסוף, גדיל אחד מכל דו־גדיל נטען לתוך חלבון הנקרא ארגונוט (Argonaute 2, AGO2), שמשתמש ב-microRNA כמדריך כדי לאתר מסרים תואמים ולהשתיקם. 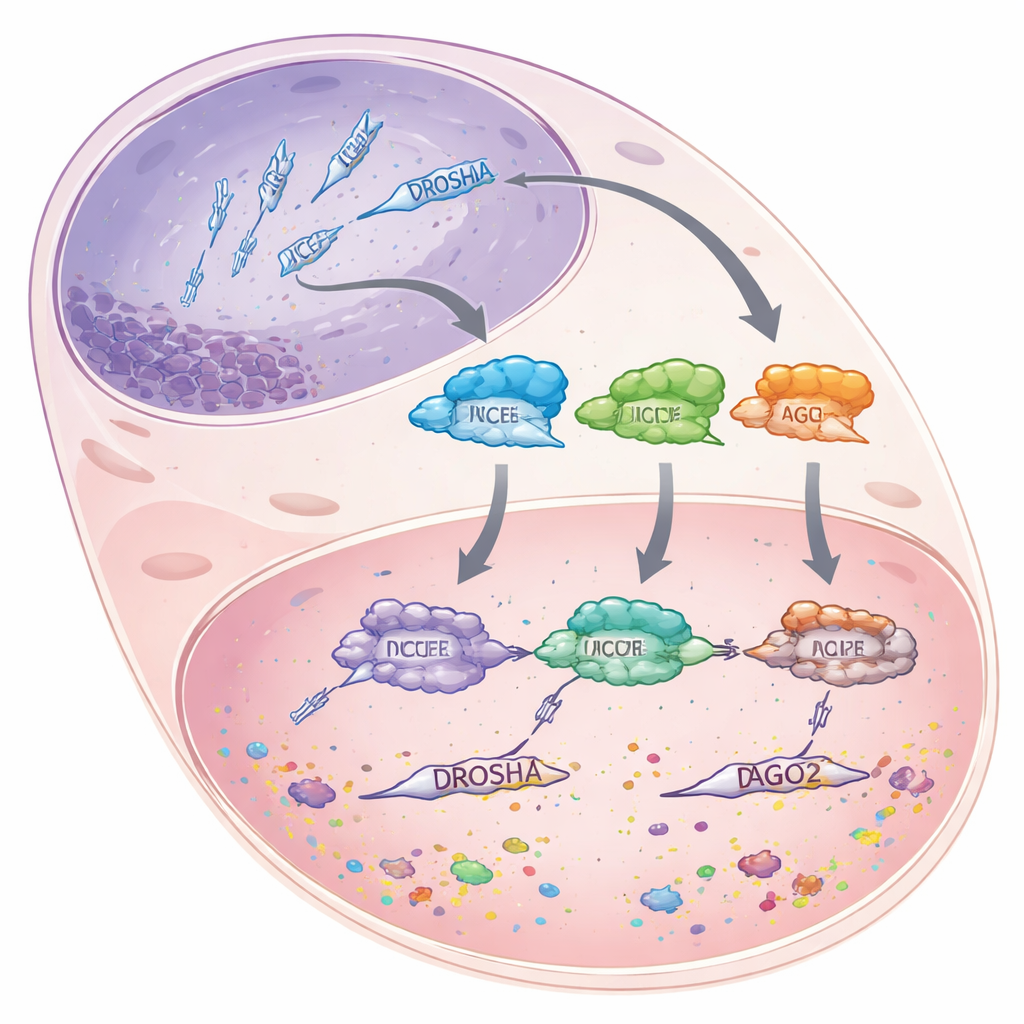
צורות עדינות עם תפקידים מדויקים
DROSHA, DICER ו‑AGO2 אינם מספריים פשוטים; כל אחד מהם בנוי ממספר חלקים אינטראקטיביים שצריכים לזוז בתיאום. DROSHA פועל יחד עם חלבון שותף, DGCR8, כדי לאחוז בקצוות של סיכת־השיער הראשונית ולהכריע בדיוק היכן לחתוך. DICER משתמש במין סרגל מובנה שמורכב מהדומיינים שלו כדי לקבוע מרחק קבוע בין המקום שבו הוא מחזיק את קצה הסיכה לבין מרכז הקטליזה שבו הוא מבצע את החיתוך. AGO2 עוטף גדיל microRNA יחיד כך שאזור ה"זֶרַע" שלו חשוף באופן מדויק לזיהוי מטרות, בעוד כן יוני מתכת וחומצות אמינו מרכזיות בגרעינו מסתדרים כדי לפרוס את המטרות כאשר התאמה היא חזקה דיה. בכל שלושת החלבונים מובלים חריצים טעונים בחשמל חיובי וקישורים גמישים את גדילי ה‑RNA למקומם, בעוד כיסי קשירת מתכת ושאריות קטליטיות מבצעים את הגזור הכימי.
כשמספריים מעוקמים או קהים
מחקרים גנטיים בחולים עם סרטן, מחלות דם ותסמונות התפתחות עצבית חשפו אשכולות של מוטציות במכונות ה‑microRNA הללו. רבות מן השינויים המזיקים ביותר נמצאים ישירות במרכזי הקטליזה או במשטחי האחיזה הצמודים ל‑RNA. ב‑DROSHA, לדוגמה, החלפות כמו E1147K ו‑D1219G נמצאות בלב אזור החיתוך ומפריעות ליכולתו להחזיק יוני מתכת חיוניים, מה שמשאיר את האנזים חסר יכולת לעבד microRNA ראשוניים. מוטציות אחרות ב‑DROSHA, כגון קיצוצים שמסירים את אזור החיתוך או שינויים שגורמים לאי־יציבות של ההליקסים התומכים בו, מחלישים את כל הקומפלקס וגורמות לירידות גלובליות ברמות microRNA בגידול וילמס, בהפרעות מח עצם ובמחלות מערכת העצבים. ב‑DICER, מוטציות שחוזרות על עצמן מתרכזות באחד משני דומייני החיתוך שלו, ומעוותות את הייצור כך שזרוע אחת של דו‑הגדיל של ה‑microRNA נאבדת, ומשנה את האיזון בין אותות המעודדים גדילה לאותות המעכבים אותה. 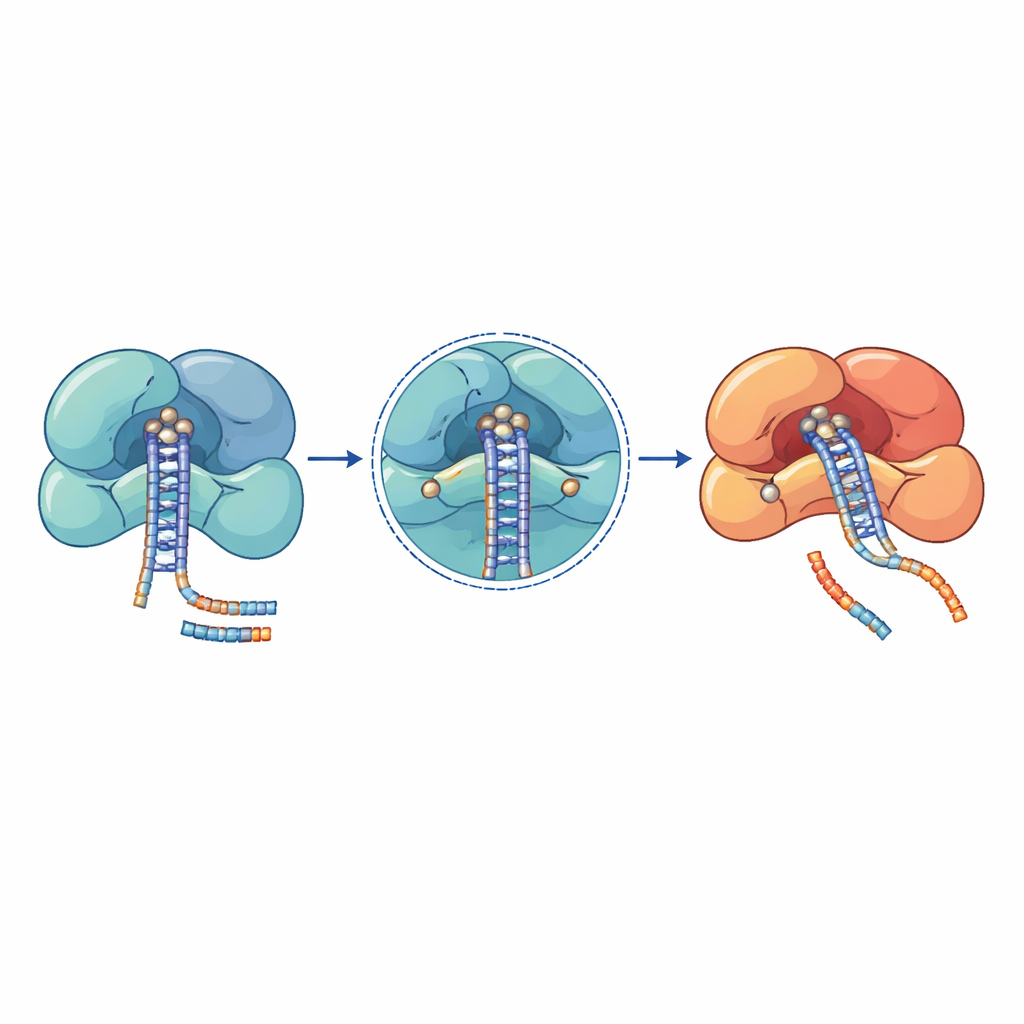
מדריכים משולשים במוח ומעבר לו
מוטציות ב‑AGO2 מספרות סיפור שונה אך קרוב. פגיעות ישירות לליבת הקטליזה שלו נדירות, ככל הנראה משום שהן תהיינה קטלניות בשלב מוקדם של ההתפתחות. במקום זאת, וריאנטים המקושרים למחלות נוטים להופיע באזורי קישורים גמישים ובמפרקי דומיינים שמחזיקים את צורת ה‑AGO2 יחד. בתסמונת לסל–קריינקמפ (Lessel–Kreienkamp), מצב התפתחות עצבית, מוטציות באותם קישורים ובמשטחים מסביבם מטות בעדינות את האופן שבו חלקי PAZ, MID ו‑PIWI של AGO2 נארזים ונעים. הדבר יכול להטות את מיקום ה‑microRNA המדריך או להחליש את אחיזתו במטרות ה‑RNA, וטשטש את הדיוק של השתקת הגנים במהלך התפתחות המוח. שינויים מבניים דומים בכל נקודה לאורך מסלול ה‑microRNA—בין אם ב‑DROSHA, DICER או AGO2—יכולים ליצור אפקט רב‑שכבתי, ולשנות רשתות שלמות של גנים המעורבים בצמיחה תאית, ביצירת דם או בכיוונון נוירונלי.
מהפיכת תובנות מבניות לטיפולים עתידיים
על־ידי השמת מוטציות מחלות על מפות תלת־ממדיות ברזולוציה גבוהה של החלבונים האלה, החוקרים יכולים לסווג בדיוק כיצד כל שינוי גורם לבעיה—בין אם על ידי כתישת הלהב הקטליטי, המרפסת מגעים קריטיים עם חלבונים שותפים או כיפוף הליקסים מרכזיים מחוץ לציר. התובנות המבניות הללו פותחות את הדלת להתערבויות ממוקדות: מולקולות קטנות שייצבו ממשקים מוחלשים, RNAs מתוכננים שינחו אנזימים חלקית פונקציונליים חזרה לתת־המטרות הנכונות, או תרכובות אלוסטריות שידחקו חלבונים מוטנטיים לצורות פעילות יותר. לצופה שאינו מומחה, המסר המרכזי הוא ששינויים מבניים זעירים במספריי ה‑RNA של התא יכולים להשפיע בצורה ניכרת על הבריאות, אך הם גם מספקים ידיות מדויקות לעיצוב טיפולים מתקדמים, המודעים למוטציות.
ציטוט: Lee, H., Lee, J. & Roh, SH. Structural insights into disease-associated mutations in the microRNA processing machinery. Exp Mol Med 58, 639–649 (2026). https://doi.org/10.1038/s12276-026-01669-4
מילות מפתח: microRNA, התערבות RNA, DROSHA DICER AGO2, גנטיקה של סרטן, הפרעות בהתפתחות עצבית