Clear Sky Science · he
מנגנוני בקרה על יציבות חלבון Snail: מערכת היוביקוויטין–פרוטאזום ואוטופגיה מווסתת-צ׳פרונים
מדוע התפשטות הסרטן תלויה בחלבון שברירי
סרטן הופך למסכן חיים כשַתאי הגידול ניתקות מהגידול המקורי ונודדות לאיברים מרוחקים. התפשטות זו, או גרורה, תלויה במידה מסוימת בחלבון ‘‘מפתח’’ רב עוצמה בשם Snail, שעוזר לתאים לשחרר את הקשרים ביניהם ולהיות ניידים יותר. מאמר זה מסביר כיצד תאים שומרים בדרך כלל על Snail תחת שליטה על ידי פירוק מהיר שלו בשתי מערכות פינוי עיקריות. הבנת האיזון הזה מציעה רעיונות חדשים להאטה או למניעה של גרורות.
מתאים צפופים לנודדים פולשים
ברקמות בריאות, תאים אפיתליאליים יוצרים שכבות מסודרות, דמויות לבנים, שנשארות במקום ומדביקות בחוזקה לשכנותיהן. עבור תא גידול להימלט, לעתים קרובות הוא עובר שינוי שנקרא מעבר אפיתלי–מזנכימלי (EMT), שבו הוא מאבד את המגעים הצפופים ורוכש יכולת לנוע ולהיכנס לרקמות אחרות. Snail הוא מניע מרכזי של השינוי הזה: כשקיים בגרעין התא, הוא מכבה גנים השומרים על צמדי תאים ומפעיל גנים התומכים בתנועתיות ובחדירה. רמות גבוהות של Snail מקושרות לסרטן אגרסיבי ולתוצאות גרועות בחולים, ולכן תאים פיתחו דרכים לשמור על רמות נמוכות וקצרות-חיים של Snail בתנאים נורמליים.
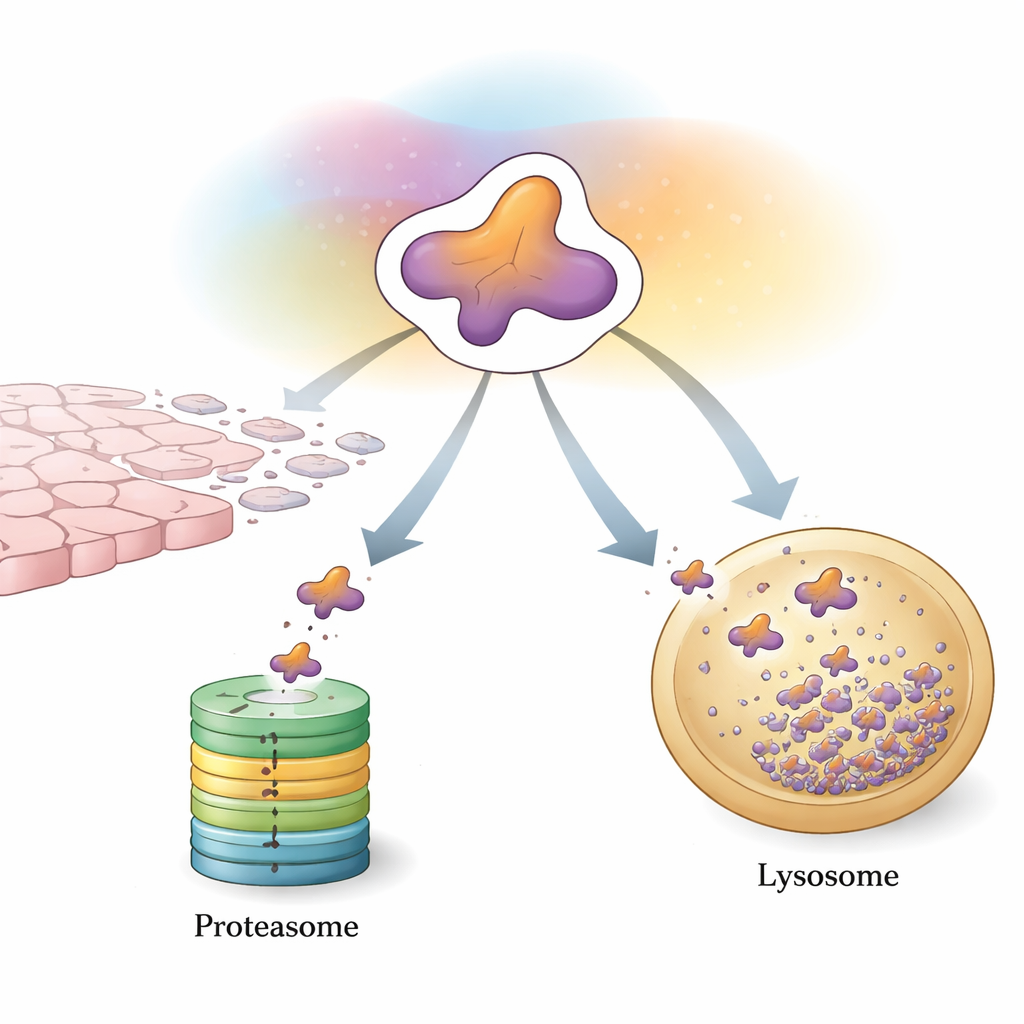
קו הבקרה הראשון של התא: תייגו וגרסו
אחת הדרכים העיקריות שבהן תאים שומרים על Snail היא באמצעות מערכת היוביקוויטין–פרוטאזום, ‘‘מערכת תיוג וגריסה’’ לחלבונים לא רצויים. אנזימים מיוחדים מצמידים ל-Snail דגלים קטנים העשויים מחלבון בשם יוביקוויטין. כאשר דגלים אלה מצטברים בתבנית מסוימת, Snail מנותב לפרוטאזום, קומפלקס בצורת חבית המפרק אותו לחתיכות. קבוצה גדולה של חלבונים מסייעים מווסתת את התהליך. חלק מהאנזימים מצמידים שרשראות שמעודדות פירוק ושולחות במהירות את Snail למגרסה, מה שעוזר להגביל את גדילת הגידול והתפשטותו. אחרים מוסיפים שרשראות שמייצבות את Snail או מגבירות בעקיפין את ביטוי הגן שלו, ומטות את המאזן לטובת EMT וגרורות. שינויים כימיים כגון זרחון ואצטילציה פועלים כמו מתגים נוספים, שקובעים אילו מסייעים יכולים להיקשר ל-Snail והאם הוא ייהרס או יישמר.
הסרת הבלמים: אנזימים שמצילים את Snail
הסיפור אינו מסתיים בתיוגו של Snail להשמדה. קבוצה נוספת של אנזימים, דה-יוביקוויטינאזות, יכולה להסיר את דגלי היוביקוויטין ולציל את Snail מהפרוטאזום. רבים מהאנזימים הללו מופעלים או מחוזקים בסרטן, מה שמאפשר ל-Snail להימנע מפירוק ולהשתמר בגרעין. פעולתם תלויה מאוד בהקשר התאי: במצבים מסוימים הם מייצבים ישירות את Snail, ובאחרים משפיעים על מיקום Snail בתא או על האינטראקציות שלו עם חלבונים שותפים. אותות ממסלולים הקשורים לסרטן, כגון גורמי גדילה ותשובות למתח, מתערבבים ברשת זו וקובעים האם Snail יוסר במהירות או יורשה להפעיל את תוכנית ה-EMT.
רשת ביטחון שנייה: מסירה סלקטיבית למרכז המיחזור התאי
מעבר לפרוטאזום, תאים מסתמכים על אוטופגיה, אוסף מסלולים שמעבירים חלבונים לאברונים חומציים הנקראים ליזוזומים לפירוק. סקירה זו מדגישה צורה בררנית מאוד הידועה כאוטופגיה מווסתת-צ׳פרונים (CMA) כנתיב משמעותי נוסף לשליטה ב-Snail. CMA מזהה רצף קצר בתוך Snail ובעזרת חלבוני לווי מסירה את Snail הציטופלזמטי לליזוזומים להשמדה. בתאי סרטן שד פחות אגרסיביים, המערכת הזו שומרת על Snail מחוץ לגרעין ורגיש להסרה ליזוזומלית. בסרטן שד אגרסיבי יותר, מסוג שלילי משולש, Snail נוטה להצטבר בגרעין ולהימנע מ-CMA, מה שמחזק את יכולתו להפעיל EMT וגרורה.
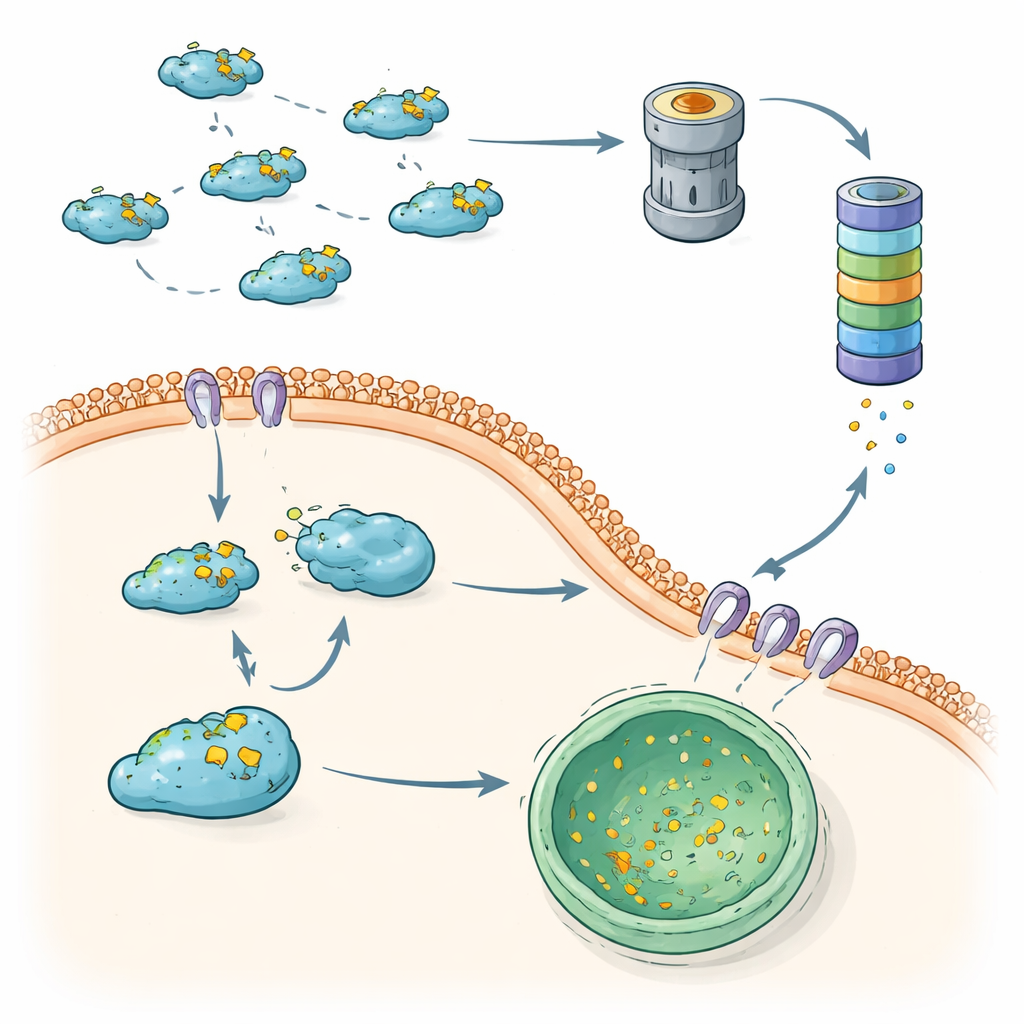
כשבקרת האיכות נכשלת, הגרורה צוברת משמעות
לסיכום, הממצאים הללו מגלים שתאים משתמשים בשני צירי ‘‘בקרת איכות’’ משלימים כדי לרסן את Snail: מסלול היוביקוויטין–פרוטאזום ופירוק ליזוזומלי מבוסס CMA. כאשר השניים פועלים כראוי, Snail מתחלף במהירות, מגביל EMT ועוזר למנוע השתלשלות תאים מפרשות. כאשר ציר אחד או שניהם מוחלשים — באמצעות שינויים באנזימים המתוייגים, דה-יוביקוויטינאזות או מרכיבי CMA — Snail נעשה יציב יותר, מצטבר בגרעין ומקדם באופן חזק התנהגות חודרת. על ידי מיפוי מסלולי הפירוק המשולבים הללו, המאמר מציג אפשרויות טיפוליות חדשות: תרופות המשחזרות או מחזקות את פירוק Snail, או שמכוונות להחזיר את Snail לנתיבי CMA או לפרוטאזום, עשויות לסייע בהחזרת הבלמים על הגרורה בלי לכבות לחלוטין מערכות מיחזור חלבונים חיוניות אלה.
ציטוט: Kim, M., Hong, KS., Kim, T. et al. Regulatory mechanisms for Snail protein stability: ubiquitin–proteasome system and chaperone-mediated autophagy. Exp Mol Med 58, 408–415 (2026). https://doi.org/10.1038/s12276-026-01667-6
מילות מפתח: גרורת סרטן, מעבר אפיתלי–מזנכימלי, חלבון Snail, מיחזור חלבונים, אוטופגיה