Clear Sky Science · he
תוספת L‑אספארטאט מתקנת MASLD ו‑MASH בעכברים על ידי עיכוב שבירת המיטוכונדריה באמצעות אינטראקציה בין טסיות־דם והפטוציטים דרך ציר ATP–P2X7–NEK7–DRP1
מדוע מחקר הכבד הזה חשוב
אנשים רבים נושאים שומן עודף בכבד מבלי לדעת זאת. בעיה חרישית זו, שכיום מכונה מחלת כבד סטאוטית משויכת ללקות מטבולית (MASLD), עלולה להתפתח לדלקת קשה, צלקת ואפילו לסרטן כבד. המאמר המסוכם כאן בוחן האם חומצת אמינו טבעית ופשוטה, L‑אספארטאט, יכולה להגן על הכבד בעכברים ומגלה אשם בלתי צפוי בפגיעה הכבדית: טסיות דם יתר פעילות שפוגעות ב״תחנות הכוח״ של תאי הכבד, המיטוכונדריה.
בעיה שכיחה בחיים המודרניים
MASLD קשורה באופן הדוק להשמנה ולסוכרת סוג 2 ועלולה להשפיע בקרוב על יותר משליש מאוכלוסיית העולם. ב‑MASLD תאי הכבד מתמלאים שומן, נלחצים ומתחילים למות, מה שמפעיל דלקת ויוצר צלקות. מיטוכונדריה בריאה שורפת בדרך כלל שומנים וסוכרים לאנרגיה, אך במחלה זו הן נהרסות ומתפרקות לחתיכות, כך שהכבד שורף פחות שומן ומצטבר בו יותר. למרות היקף הבעייה, רק תרופה אחת אושרה עד כה והיא עוזרת לחלק קטן מהחולים, ולכן החוקרים מחפשים טיפולים בטוחים ומשתלמים המשחזרים את מכונות האנרגיה של הכבד.
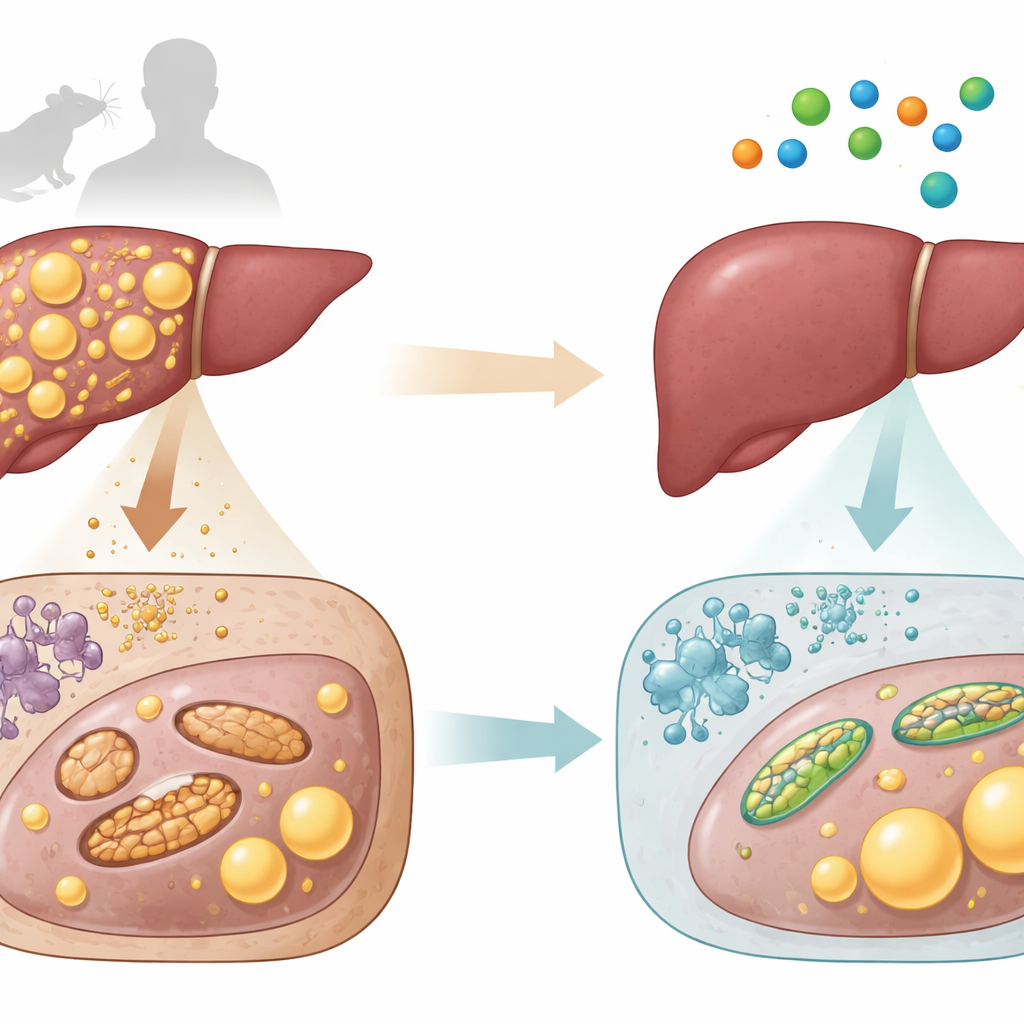
חומצת אמינו פשוטה כבעלת פוטנציאל עזר
L‑אספארטאט היא לבנה קטנה של חלבונים שלוקחת חלק גם במחזורים האנרגטיים של הגוף וכבר משמשת קלינית כחומר תומך כבד. החוקרים מדדו תחילה L‑אספארטאט בדגימות דם וכבד מעכברים ומאנשים. הם מצאו שבחיות ובמטופלים אנושיים עם כבד שומני ופגוע יותר היו ברמות נמוכות יותר של L‑אספארטאט ברקמת הכבד. בשתי המינים, ככל שהייתה פחות L‑אספארטאט כך היה יותר שומן וככל שהיו איתותים חזקים יותר לפגיעה בכבד. דפוס זה רמז לכך שהירידה ב‑L‑אספארטאט עלולה להלך יד ביד עם החמרת בריאות הכבד.
היפוך כבד שומני ודלקת בעכברים
לאחר מכן הקבוצה בדקה האם הוספת L‑אספארטאט יכולה באמת לתקן את המחלה. הם האכילו עכברים בדיאטה עתירת שומן וכולסטרול או בדיאטה מיוחדת שמעוררת דלקת וצלקת כבד חמורה, המדמה MASLD אנושי ואת צורתו המתקדמת MASH. כאשר העכברים קיבלו הזרקות L‑אספארטאט במינונים השווים לאלה בשימוש קליני, הכבד שלהם היה בהיר ופחות שמנוני, רמות אנזימי כבד בדם ירדו ובבדיקות מיקרוסקופיות נצפו פחות טיפות שומן, פחות דלקת וקמטוטים מצטמצמים. היתרונות האלה הופיעו הן במצב הכבד השומני המוקדם והן במחלה דלקתית מתקדמת והיו להשוות להשפעות של תרופות ייחוס מוכרות באותם דגמים.
הגנה על תחנות הכוח של התא
מבט פנימי בכבד הראה שבעכברים חולים היו פחות מיטוכונדריות, רבות מהן מוגדלות ופגומות או מרוסקות לפירורים קטנים. טיפול ב‑L‑אספארטאט שיקם רשת בריאה יותר של מיטוכונדריות מוארכות. הוא חיזק את פעילות קומפלקסי האנזימים המרכזיים שמייצרים אנרגיה, הגדיל את שימוש החמצן והייצור של ATP במיטוכונדריה, והעלה סמנים של ״ניקוי״ וחידוש המיטוכונדריה. מדידות על כל הגוף הראו צריכת חמצן והוצאה אנרגטית גבוהות יותר, מה שמעיד שהעכברים שרפו יותר דלק באופן כללי ולא רק אכלו פחות.
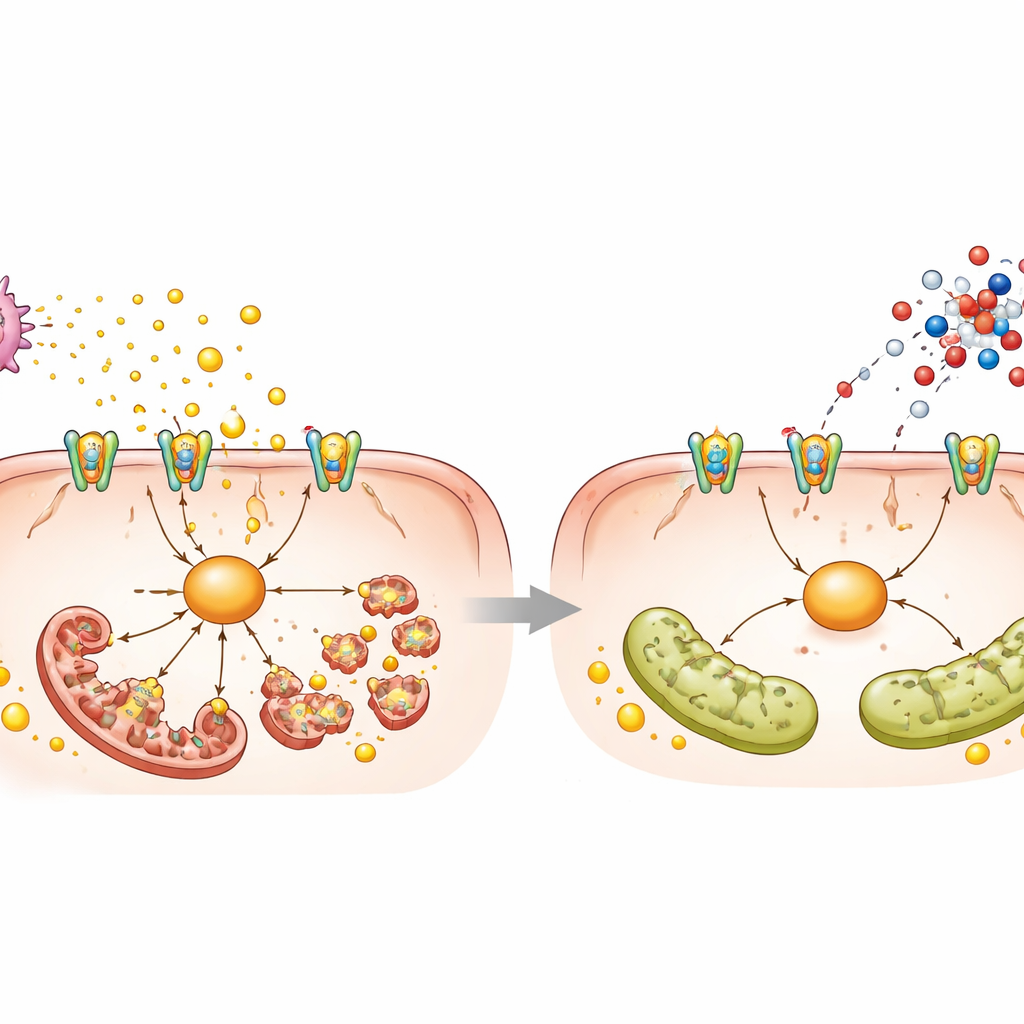
טסיות, אות רעיל, ורצף מולקולרי
כדי להבין כיצד L‑אספארטאט מפעיל את ההשפעות הללו, החוקרים שיתפו פרופילי פעילות גנים ומטבוליטים לאחר מינון יחיד. עלה אות בלתי צפוי: מסלולים המקושרים להפעלת טסיות והשליח המולקולרי cGMP. בכבד שומני, טסיות בדם ובכבד היו מרובות יותר ומופעלות, והן שיחררו ATP נוסף — מולקולת אנרגיה נורמלית שהופכת למזיקה כשהיא נוזלת אל מחוץ לתאים. ATP זה הפעיל קולטן בשם P2X7 על תאי הכבד, אשר בתורו הפעיל חלבון בשם NEK7 וחלבון השבר DRP1, שהניעו את פירוק המיטוכונדריה וקידמו הצטברות שומן ומות תאים. L‑אספארטאט העלה את רמות ה‑cGMP בתוך הטסיות, החריש את הפעלתן והצברתם, צמצם שחרור ATP ורגוע את שרשרת P2X7–NEK7–DRP1 בתוך תאי הכבד. חסימה ישירה של הטסיות באספירין, עיכוב P2X7 או הדחקת NEK7 חיקו רבים מהאפקטים המגנים של L‑אספארטאט, ותמכו ברעיון שאינטראקציה בין טסיות לכבד היא מרכזית לפגיעה.
מה זה יכול להוביל עבור מטופלים
ביחד, ממצאים אלה מציעים שבמחלת כבד שומנית, טסיות יתר פעילות מציפות את הכבד ב‑ATP, מה שמפעיל קסקדה מולקולרית שמרעישה את המיטוכונדריה ומחמירה הצטברות שומן ופגיעה. בעכברים, תוספת L‑אספארטאט שוברת את הלולאה הזו: היא מאדה את טסיות הדם, מגבילה שחרור ATP, שומרת על צורת ותפקוד המיטוכונדריה ומתהפכת הן בכבד שומני פשוט והן במחלה דלקתית ופיברוטית. מאחר ש‑L‑אספארטאט זול וכבר משמש כסוכן תומך כבד, המחקר מדגיש אותו כמועמד מבטיח לבדיקה ב‑MASLD ו‑MASH אנושיים, ובמקביל מצביע על נזק מיטוכונדריאלי מונע טסיות כיעד חדש לטיפולים עתידיים.
ציטוט: Cao, WJ., Su, R., Fu, HL. et al. Supplementation of L-aspartate corrects MASLD and MASH in mice by inhibiting platelet–hepatocyte interaction-mediated mitochondrial fragmentation via the ATP–P2X7–NEK7–DRP1 axis. Exp Mol Med 58, 533–547 (2026). https://doi.org/10.1038/s12276-026-01648-9
מילות מפתח: מחלת כבד שומנית, טסיות דם, מיטוכונדריה, L‑אספארטאט, מחלת כבד מטבולית