Clear Sky Science · he
לולאת משוב חיובית ESRP1/circPHGDH/miR-149/RAP1B מקדמת התנהגויות ממאירות וגликוליזה בתאי סרטן הערמונית
מדוע מחקר זה חשוב לבריאות גברים
סרטן הערמונית הוא אחד הסוגים הנפוצים ביותר של סרטן בגברים, ולעתים קרובות גידולים מתפתחים בסופו של דבר לצורות אגרסיביות ולעמידות לטיפולים. מחקר זה חושף מעגל בקרה נסתר בתוך תאי סרטן הערמונית שמסייע להם לגדול מהר יותר, להתפשט ביתר קלות, ולשנות את הדרך שבה הם צורכים סוכר כמקור אנרגיה. מיפוי הלולאה המולקולרית הזה מצביע על נקודות תורפה חדשות שעשויות לשמש מטרה לעיכוב ההתקדמות או לשיפור יעילות טיפולים קיימים.
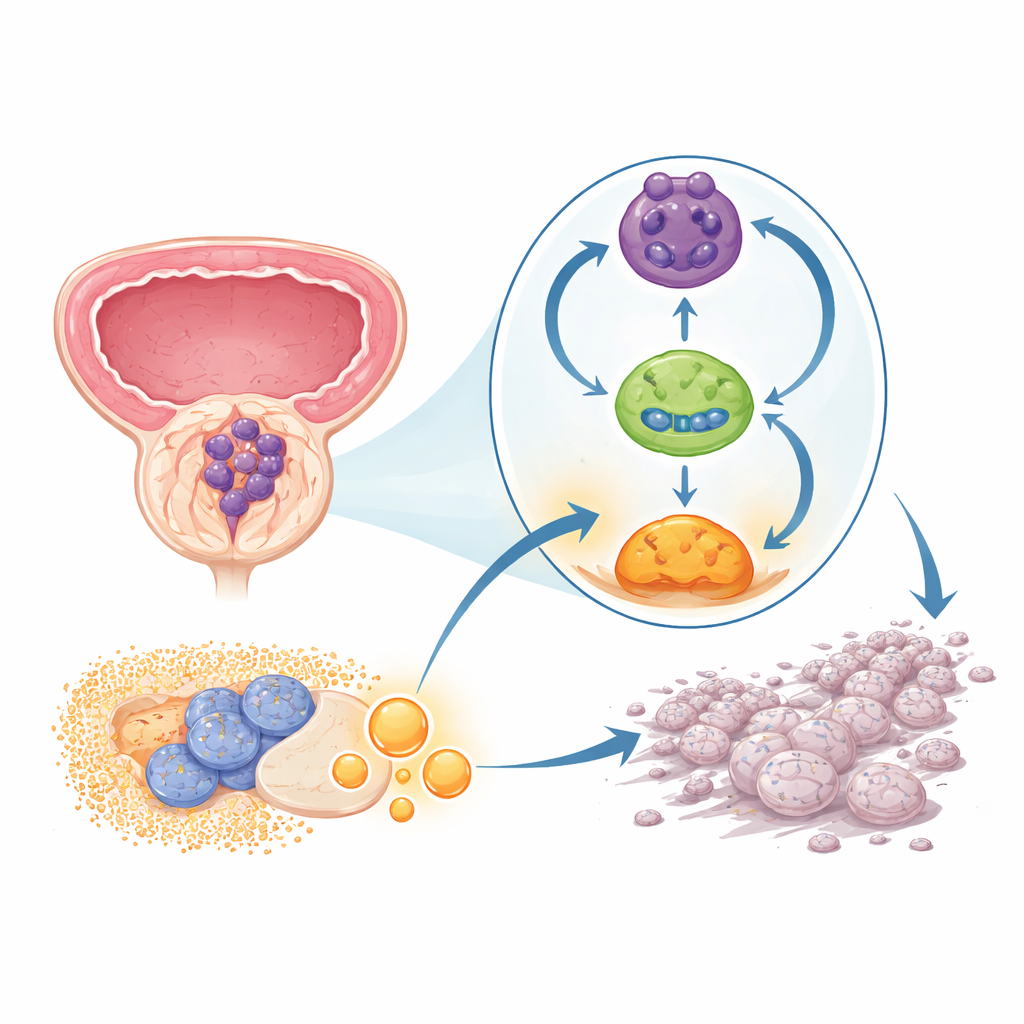
לולאה נסתרת שמשאירה את הסרטן דולק
הצוות התמקד בסוג חומר גנטי שנמצא לאחרונה בתשומת לב — RNA מעגלי. בניגוד לשרשראות הליניאריות הרגילות, מולקולות אלה יוצרות טבעות סגורות והן יציבות באופן יוצא דופן. במגרעות גידול של הערמונית ובשורות תאים, החוקרים מצאו RNA מעגלי מסוים, שנקרא circPHGDH, ברמות גבוהות באופן עקבי לעומת רקמה סמוכה שאינה סרטנית. בחולים שבהם הגידול הכיל יותר RNA זה נצפו גידולים גדולים יותר, התפתחות מקומית מתקדמת ומטאסטזות מרוחקות, מה שמעיד ש-circPHGDH תורם לצורה מסוכנת יותר של המחלה.
כיצד תאי הסרטן משנים את ההתנהגות שלהם
כדי לברר מהו תפקידה של circPHGDH, המדענים שינו את רמותיו בתאי סרטן הערמונית שנגודלו במעבדה. כאשר הם הפחיתו את circPHGDH, התאים יצרו פחות מושבות, נעו ופולשו דרך ממברנות פחות ביעילות, והופיעו בהם סימנים לשמירה על מצב אפיתלי יותר, שפחות נוטה להתפשט. במקביל, התאים סטו מאסטרטגיית מטבוליזם התלויה בסוכר שאופיינית לגידולים רבים: התלות בגликוליזה ירדה, והם השתמשו יותר בייצור אנרגיה מבוסס חמצן. כאשר חיזקו את circPHGDH, כל התכונות המעודדות סרטן הללו זזו בכיוון ההפוך.
RNAים קטנים וריליי איתותי לצמיחה
המחקר עקב אחר המנגנון שבאמצעותו circPHGDH מפעיל את ההשפעות הללו. בציטוזול התא, circPHGDH מתפקד כספוג עבור RNA רגולטורי זעיר בשם miR-149, סופג אותו ומונע ממנו לדכא את המטרות הרגילות שלו. יעד מרכזי הוא RAP1B, חלבון איתות שמשולב למסלול מרכזי של צמיחה והישרדות הידוע כחיוני בסרטן הערמונית. כאשר miR-149 מעוכב על ידי circPHGDH, רמות RAP1B עולות ומפעילות אותות יורדים שמקדמים חלוקת תאים, תנועה ומטבוליזם מבוסס גликוליזה. שיקום miR-149 או הפחתה ישירה של RAP1B הפך רבים מהאפקטים המזיקים, הן בתרביות תאים והן בעכברים נשאים תאים אנושיים של סרטן הערמונית.
פסולת מטבולית שמדליקה את הלהבה
שכבה נוספת בסיפור עוסקת באופן יצירתו של circPHGDH מלכתחילה. יצירתו תלויה בחלבון ספlicing שנקרא ESRP1, שעוזר להחליט כיצד מסרים של RNA גולמיים נחתכים ומחוברים מחדש. החוקרים הראו ש-ESRP1 נקשר לאתרי מפתח סביב אזור circPHGDH ומעדיף את הצורה המעגלית על פני הגרסה הליניארית הסטנדרטית. חשיבותית עוד יותר, הם גילו שלקטט — תוצר סופי של גликוליזה — יש השפעה כימית על ESRP1 במקום יחיד, שמגבירה את יציבות החלבון. מכיוון ש-circPHGDH עצמו דוחף את התאים לכיוון יותר גликוליטי ובכך לייצר יותר לקטט, נוצר מעגל מחזק עצמי: ESRP1 מגדיל את circPHGDH, circPHGDH מגביר את RAP1B והגликוליזה, הגликוליזה מייצרת לקטט, והלקטט, בתורו, מייצב את ESRP1.
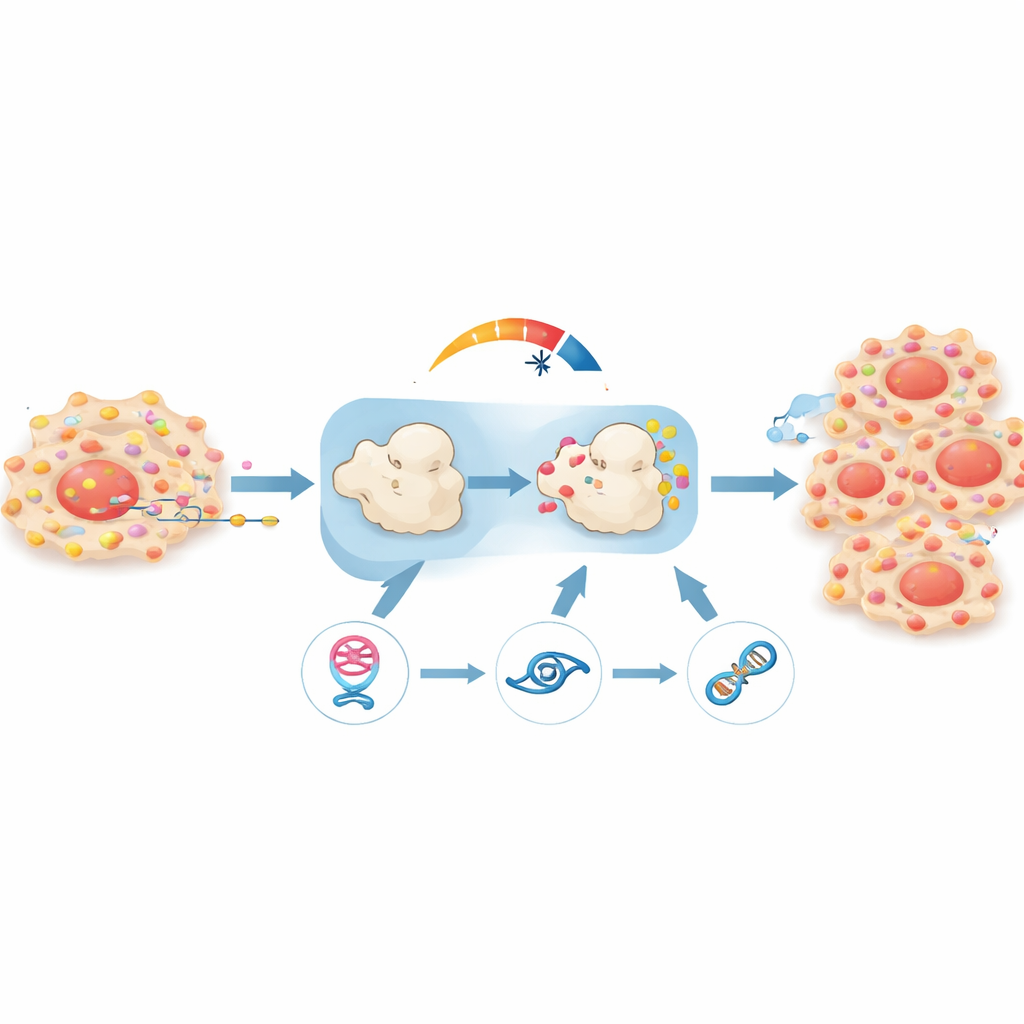
ראיות ממודלים חייתיים
כדי לבדוק האם הלולאה אכן משמעותית בארגניזם חי, הצוות השתיל תאי סרטן ערמונית אנושיים בעכברים. גידולים שבהם circPHGDH היה מושתק גדלו לאט יותר, שקלו פחות והראו סימנים מופחתים של התפשטות, כפי שנמדד בדמיה של כל הגוף ובניתוח רקמות. סמנים של רביית תאים היו נמוכים יותר, ומבנה הגידול נראה פחות אגרסיבי תחת המיקרוסקופ. כאשר החוקרים חסמו את miR-149 או הכניסו מחדש RAP1B באותו ניסוי, רוב צמיחת וההפצה חזרו, מה שאישר שרשרת circPHGDH–miR-149–RAP1B היא מניע מרכזי בהתנהגות המחלה.
מה משמעות הממצאים עבור טיפולים עתידיים
ביחד, הממצאים חושפים לולאת משוב חיובית שבה חלבון ספlicing, RNA מעגלי, RNA רגולטורי קטן וחלבון איתות משתפים פעולה כדי לדחוף תאי סרטן הערמונית לצמיחה מהירה, פלישה ומטבוליזם תאב סוכר. עבור הקוראים שאינם מומחים, המסר המרכזי הוא שתאי סרטן יכולים לכוון את הבקרה הגנטית והמטבולית שלהם למעגלים מחזקים עצמית ששומרים על התקדמות המחלה. שבירת הלולאה — על ידי הפרעה ל-circPHGDH, שיקום miR-149, חסימת RAP1B או מניעת המודיפיקציה התלויה בלקטט של ESRP1 — מציעה כמה דרכים מבטיחות לפיתוח תרופות עתידיות שמטרתן להאט או לעצור סרטן ערמונית אגרסיבי.
ציטוט: Wang, X., Yu, L., Qian, X. et al. A ESRP1/circPHGDH/miR-149/RAP1B positive feedback loop promotes the malignant behaviors and glycolysis of prostate cancer cell. Exp Mol Med 58, 622–635 (2026). https://doi.org/10.1038/s12276-026-01646-x
מילות מפתח: סרטן הערמונית, RNA מעגלי, מטבוליזם גידול, מיקרוRNA, נתיבי איתות