Clear Sky Science · he
המרה מכנית דרך קולטני תאי T: קונסנסוס, מחלוקות ומבט לעתיד
איך תאי החיסון חשים את עולמם
מערכת החיסון שלנו עושה יותר מאשר לגמול אותות כימיים; היא גם מרגישה כוחות פיזיים. מאמר סקירה זה בוחן כיצד תאי T — תאי דם לבנים הצדים וירוסים וסרטן — עשויים להשתמש בעיסות ומשיכות זעירות על קולטניהם המשטחיים כדי להחליט האם לתקוף. הבנת "חוש המישוש" הזה בקנה מידה מולקולרי עשויה לעצב מחדש את האופן שבו אנו חושבים על חיסונים, אימונותרפיה של סרטן ומחלות אוטואימוניות.
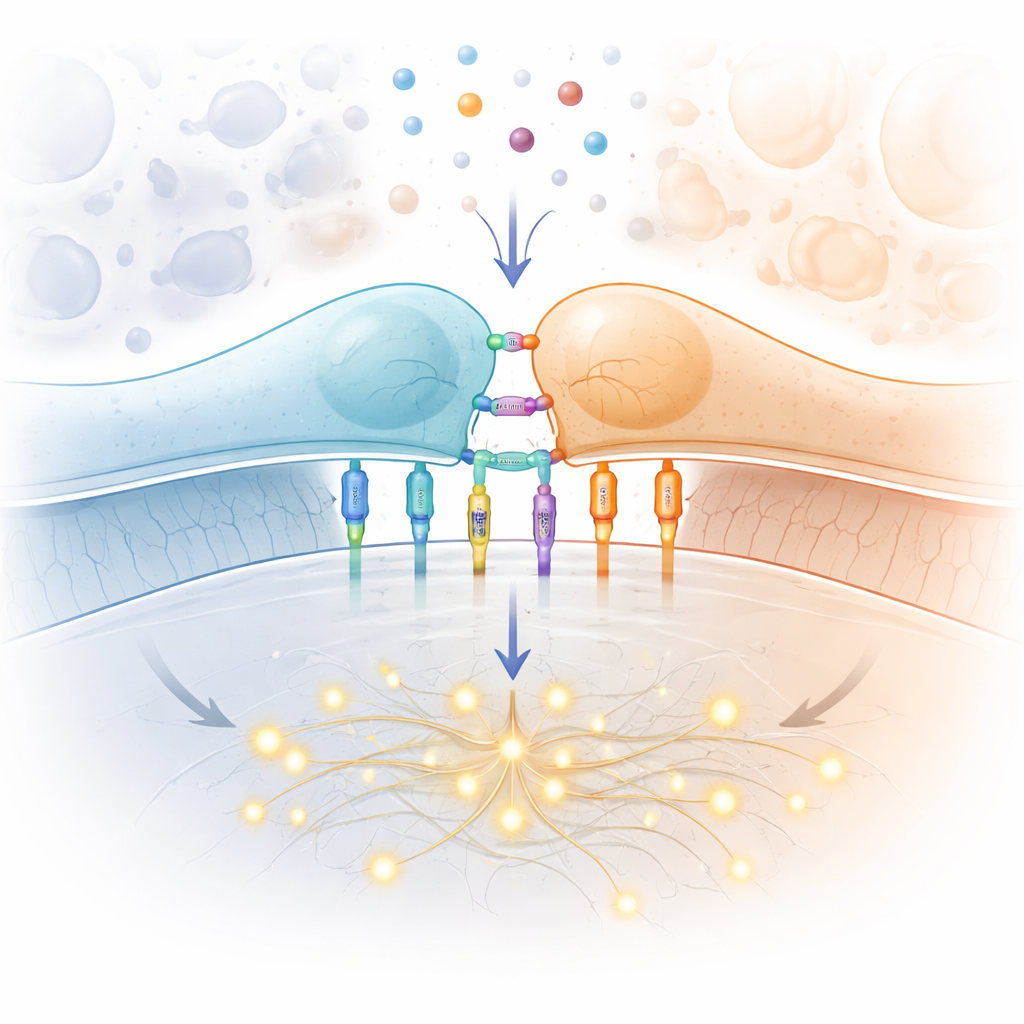
התפקיד המיוחד של קולטן תא ה‑T
בלב הסיפור עומד קולטן תא ה‑T, מכונה מולקולרית על פני תא ה‑T הבוחנת מקטעי חלבון המוצגים על ידי תאים אחרים. כאשר נמצא המקטע הנכון, תא ה‑T יכול להיכנס לפעולה, להתרבות ולהשמיד מטרות נגועות או סרטניות. על הקולטן הזה לעמוד בקבוצת דרישות קשיחה: עליו להגיב למספר זעיר של מקטעים זרים, להתעלם מים של מקטעי עצמי חסרי מזיק, לפעול במהירות בזמן שתאי ה‑T מסיירים בגוף ולעשות זאת עבור מיליוני וריאנטים של קולטנים בכל אדם. החיווט הקלאסי של מסלול ההשעיה בתוך התא — הכולל קינאזות חלבון, מבנים עזר ופקטורי שעתוק — ממופה היטב. מה שנשאר תעלומה הוא הצעד הראשון עצמו: כיצד פעולה פשוטה של קשירה למקטע במשטח התא הופכת את הקולטן מדומם לפעיל.
רעיונות מתחרים על הניצוץ הראשון
חוקרים הציעו כמה מודלים לאופן שבו קולטן תא ה‑T נדלק לראשונה. בגישה אחת, האיתות מתחיל כאשר הקולטנים נאספים לצברים קטנים, מה שמגביר את הריכוז המקומי ומאפשר לתגובות האיתות להתקדם ביעילות רבה יותר. רעיון נוסף מדגיש שינויים בצורה: קשירה עשויה לסובב או להרפות חלקים במורכב הקולטן, לשחרר מקטעים קבורים בתוך התא כדי שאנזימים יוכלו למתח אותם. מודל שלישי מצביע על צפיפות במקום המגע שבין תאים: כאן, זוגות קולטנים–ליגנד קצרים נארזים לאזורים צפופים שמוציאים פיזית אנזימים גדולים שמכבידים בדרך כלל על האותות, מה שמטה את המאזן לכיוון הפעלה. לכל מודל יש תמיכה ניסויית והוא מסביר חלק מהחידה, אך אף אחד מהם לבדו לא מתאר במלואו את הרגישות הקיצונית של הקולטן ואת יכולתו להבחין בין מקטעי חלבון דומים מאוד.
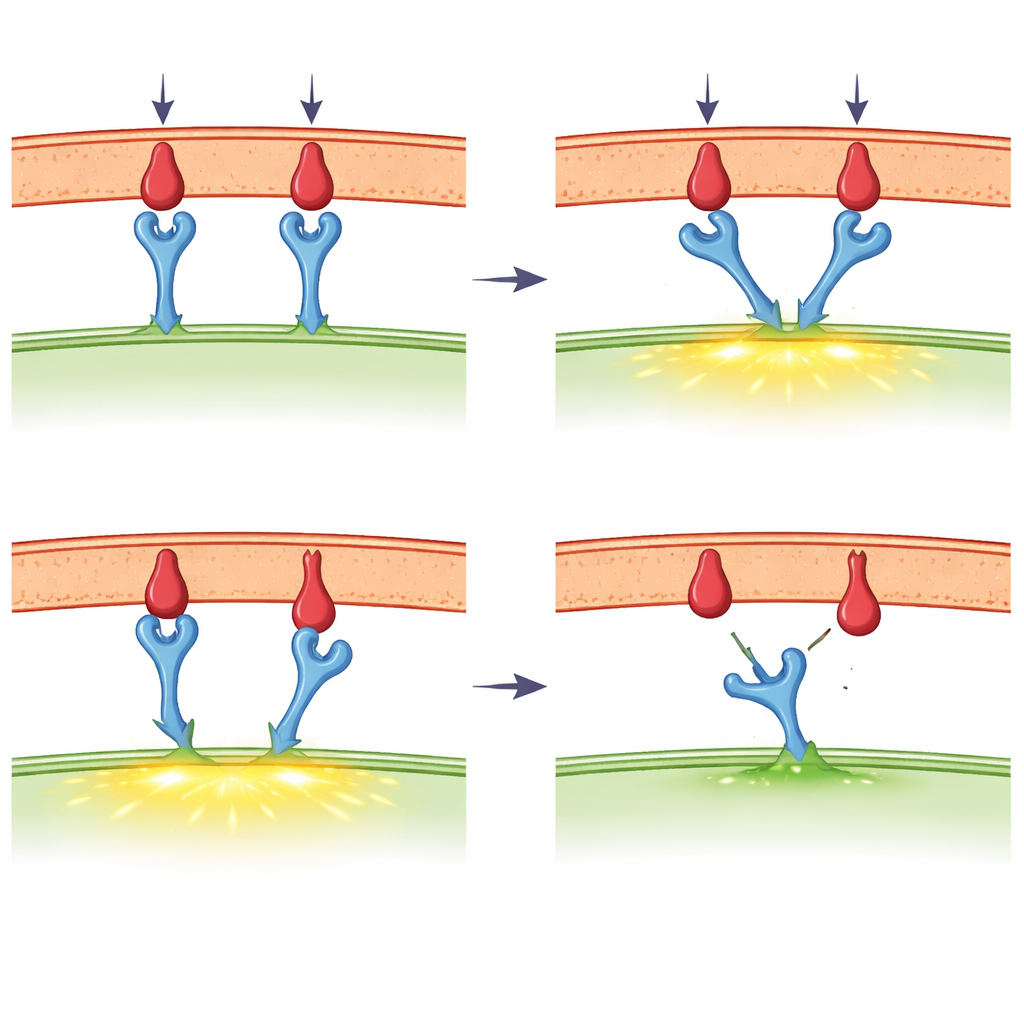
כשמגע וכוח נכנסים לתמונה
מוקד מרכזי בסקירה הוא הרעיון המתפתח שקולטן תא ה‑T מתנהג כחיישן מכני — מכשיר שמגיב לכוח. בעזרת כלים רגישים במיוחד, מדענים משכו על קשרים בודדים בין קולטן וליגנד עם כוחות שקטנים במיליארד מיליארד ממשקל תפוח. הם מוצאים שלמקטעים זרים עוצמתיים, משיכה מתונה יכולה למעשה להאריך את משך חיי הקשר, התנהגות הידועה כתגובה מסוג "catch". מקטעים חלשים או מקטעי עצמי מציגים במקום זאת התנהגות מסוג "slip": הם נוטשים מהר יותר כשנמשכים. תאי ה‑T עצמם מייצרים כוחות כאלה דרך שלדם הפנימי של פילמנטים אקטין וחלבוני מנוע, במיוחד באזור המגע הצפוף הקרוי הסינפסה החיסונית. גלאי מתיחות מולקולרי חדשים מראים שכוחות בטווח שבו מופיעה התנהגות ה‑catch אכן נוכחים במהלך ההפעלה המוקדמת של תאי ה‑T, אף ששיטות ניסוי שונות לעיתים מדווחות ערכים שונים ועוררו דיון ער.
פיענוח עצמי מול זרות לאורך זמן
המאמר בוחן גם כיצד תאי ה‑T יכולים להפוך אירועי מגע רועשים וחולפים להחלטות מהימנות. רעיון ותיק, ה‑kinetic proofreading, מציע שהאיתות מתקדם דרך רצף של שלבים שדורשים זמן; רק מקטעים ששומרים על הקולטן קשוב מספיק זמן מאפשרים לשרשרת להגיע לנקודת אי‑חזור. המחברים דנים כיצד השפעות מכניות יכולות להחדד את המסנן הזמני הזה: כוחות משיכה מאריכים את חיי הקשרים הפרודוקטיביים ומקצרים את אלה הבלתי‑פרודוקטיביים, מה שמרחיב את הפער בין גירויים חזקים לחלשים. הם גם שוקלים כיצד תאי ה‑T עשויים לאגד הרבה מגעים קצרים במקום להסתמך על מגע יחיד ארוך, ואיך משוב בתוך רשת האיתות יכול לאחסן סוג של "זיכרון" מולקולרי של מפגשים אחרונים. שיפורים אלה מסייעים להסביר כיצד תאי ה‑T משיגים גם מהירות וגם דיוק בסביבות רקמתיות מורכבות.
עקרונות משותפים בין קולטני המערכת החיסונית
למרות שקולטן תא ה‑T תובעני במיוחד במה שהוא נדרש להשיג, רבים מעקרונות העיצוב שלו מופיעים גם בקולטנים חיסוניים אחרים. קולטני תאי B וקולטני נוגדנים על תאי החיסון המולדים חולקים מוטיבים איתותיים דומים ולעתים פועלים באזורים במגע צמודים שבהם צפיפות, אשכולות וכוחות ציטוסקלטליים חשובים. תגובות דמויות‑catch לכוח דווחו כעת עבור כמה זוגות קולטן–ליגנד כאלה. הדבר מרמז שתחושת רמזים מכניים עשויה להיות אסטרטגיה כללית שמערכת החיסון משתמשת בה כדי לבדוק האם מטרה מעוגנת היטב, מוצגת נכון ושווה תגובה.
מדוע זה חשוב לבריאות ולטיפול
לקורא הרחב, המסקנה היא שתאי ה‑T אינם סופרים פשוט את נוכחותם של מולקולות זרות — הם גם בודקים כיצד המולקולות האלה מרגישות כשהן נמשכות. על ידי שילוב כימיה, פיזיקה וביולוגיה של התא, סקירה זו טוענת שקולטנים חיסוניים ממירים הבדלים עדינים גם בקשירה וגם בכוח להחלטות חי‑ומוות עבור תאים. הבנה מעמיקה יותר של הכללים המכאנוביולוגיים האלה יכולה להנחות עיצוב של טיפולים מבוססי תאי־T טובים יותר, חיסונים מדויקים יותר ותרופות חדשות המכווננות תגובות חיסוניות כלפי מעלה או מטה על‑ידי שינוי לא רק מה שהקולטנים קושרים, אלא גם כיצד הם מעורבים מכנית.
ציטוט: Travaglino, S., Jeon, Y., Kim, Y. et al. Mechanotransduction through T cell receptors: consensus, controversies and future outlooks. Exp Mol Med 58, 319–335 (2026). https://doi.org/10.1038/s12276-026-01639-w
מילות מפתח: קולטן תא T, המרה מכנית, catch bonds, סינפסה חיסונית, proofreading קינטי