Clear Sky Science · he
גורם הבקרה אינטרפרון 5 מעורב בפתוגנזה של אמפיזמה דרך NLRP3 ותאים מביעים Ly6C
מדוע המחקר הריאתי הזה חשוב
מחלת ריאות חסימתית כרונית (COPD) ואמפיזמה גוזלות את נשימתם של מיליוני אנשים, לעיתים שנים רבות אחרי שהפסקו לעשן. התרופות הקיימות יכולות לעזור לפתוח את דרכי הנשימה, אך הן עושות מעט כדי להרגיע את הדלקת החבויה שממשיכה לפגוע בריאות. המחקר הזה מגלה "מוביל עגלה" מולקולרי לנזק הזה, ומציע דרך חדשה להגן על הנאדיות העדינות ולהאט את הירידה בתפקוד הריאה.
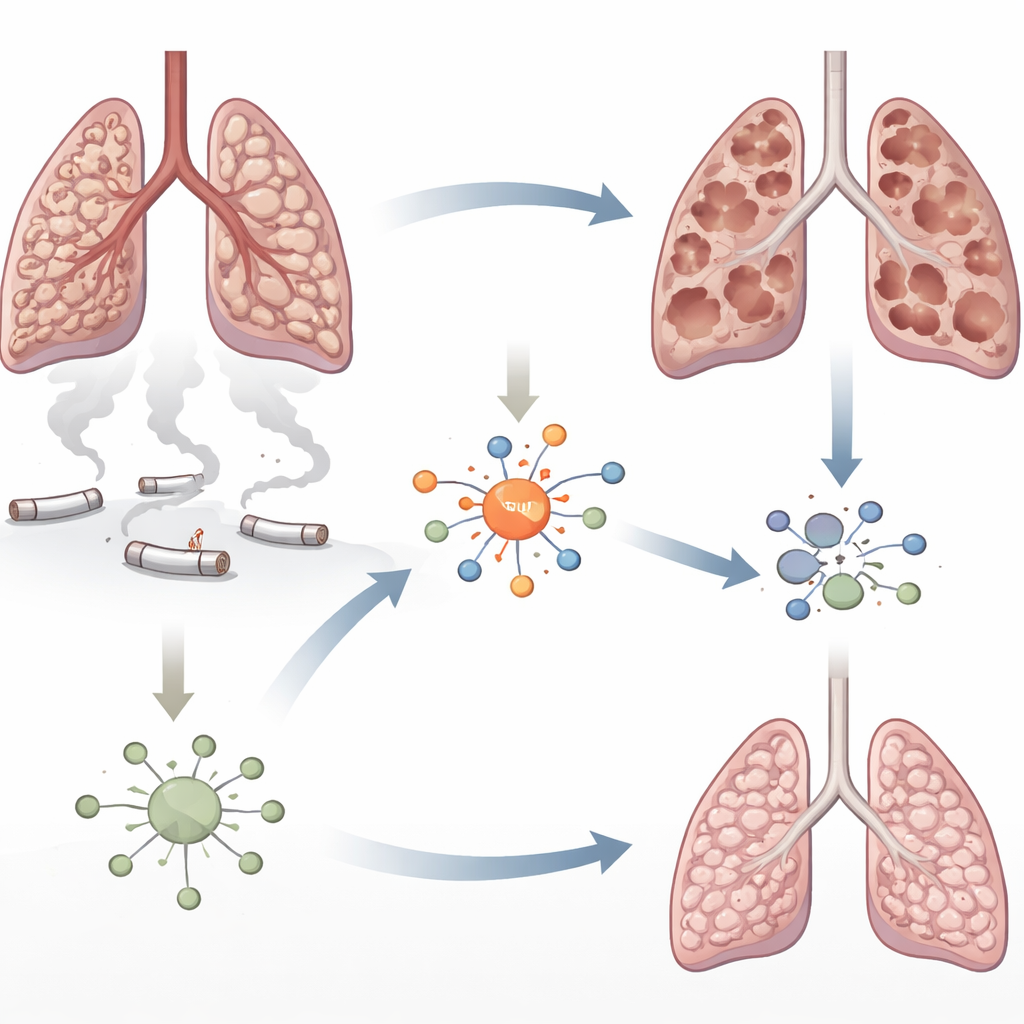
מבט צמוד על ריאות שניזוקו מעשן
אמפיזמה מאופיינת בהתמוטטות הדרגתית של הנאדיות הקטנות שמחליפות חמצן ופחמן דו-חמצני. עשן סיגריות מוצף את הריאות בחלקיקים רעילים שפוגעים בתאים ומגייסים גל של תאים חיסוניים. החוקרים התמקדו בחלבון שנקרא גורם הבקרה של אינטרפרון 5 (IRF5), הידוע כמדלל דלקת במחלות אוטואימוניות אך שלא נחקר היטב ב‑COPD. מחקרים קודמים רמזו שרמות IRF5 עולות בריאות החשופות לעשן. כאן ביקשו החוקרים לבדוק האם IRF5 רק מלווה את הדלקת או שאכן תורם להשמדת רקמת הריאה.
כיבוי מתג מרכזי בעכברים
על מנת לחקור את תפקידו של IRF5, הקבוצה הנדסה עכברים החסרים לחלוטין את הגן לחלבון זה. הם חשפו אז עכברים רגילים ועכברי חסרי IRF5 לעשן סיגריות במשך מספר שבועות והשוו את מצב הריאות שלהם. בעכברים רגילים, העשן גרם לסימני אמפיזמה ברורים: הקירות בין הנאדיות השכנות נעלמו, והשאר רוחב גדול ונפוח מדי. לעומת זאת, העכברים ללא IRF5 היו מוגנים ברובה מפגיעה מבנית זו, אף שהעשן עדיין הביא תאים חיסוניים לחללים האוויריים והגביר תרכובות דלקתיות רבות. ממצאים אלה הצביעו על IRF5 כקשר מכריע בין חשיפה לעשן להריסת הארכיטקטורה של הריאה.
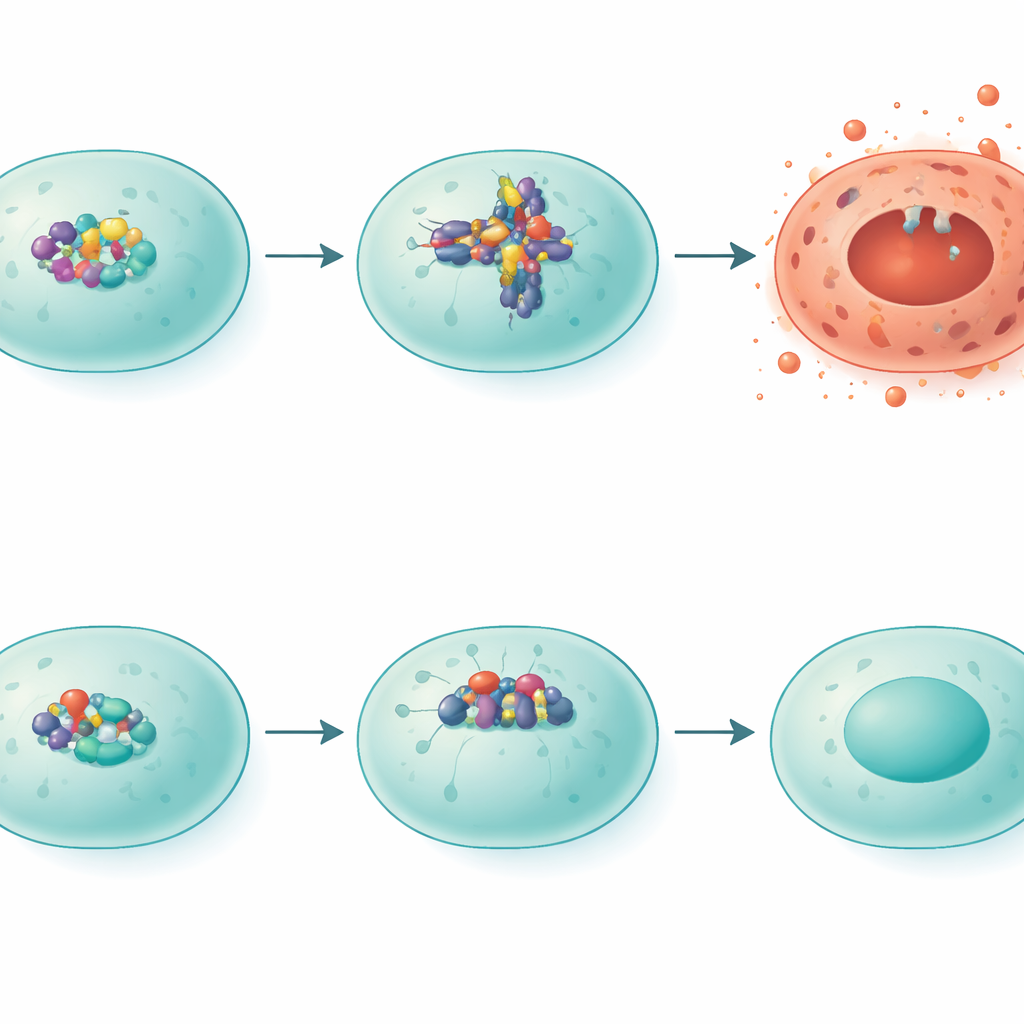
כיצד IRF5 דוחף תאים לעבר מוות סוער
החוקרים התמקמו אז בצורת מוות תאי אלימה מסוימת הנקראת פירופטוזה, שמחוררת ממברנות תא ומפזרת תכולה דלקתית ברקמה הסובבת. קומפלקס חלבוני הידוע כ‑NLRP3 עומד בלב התהליך הזה. בעכברים רגילים החשופים לעשן, רמות NLRP3 עלו, ודפוסי חלבון נוסף, גסדרמין D, התאימו למצב המזכיר פירופטוזה. בעכברים חסרי IRF5, רמות NLRP3 היו נמוכות בהרבה וגסדרמין D יוחלף לצורות אחרות המקושרות לתוצאות פחות הרסניות. כאשר הצוות הגביר באופן מלאכותי את IRF5 בתאים קשורים לריאה במעבדה, רמות NLRP3 עלו, ואישר הדבר כי IRF5 פועל כמפסק שחלבוני גנים זו מדליק את הנתיב הפוגע.
תאים חיסוניים מגוננים נכנסים לתמונה
IRF5 שינה גם את הרכב התאים החיסוניים בריאה. בעכברים חסרי IRF5 נרשמה עלייה בולטת בתת־קבוצה של תאים שמקורם בדם המסומנים בחוזקה על פני השטח במולקולה שנקראת Ly6C. תאי Ly6C‑גבוהים אלה כללו גם מונוציטים וגם תאי T והופיעו בכמויות גדולות יותר לאחר חשיפה לעשן. כאשר המדענים טיהרו תאי Ly6C‑גבוהים מעכברים חסרי IRF5 והזריקו אותם לעכברים רגילים שנחשפו לעשן, הנתרמים פיתחו פחות הרס של נאדיות והראו רמות NLRP3 מופחתות בריאה. ניסויים נוספים גילו כי IRF5 מדכא ישירות את פעילות גן Ly6C, מה שמרמז שכאשר IRF5 נוכח, מיוצרים או שומרים פחות תאים אלה שעשויים להיות מגינים.
ריאות אנושיות מאשרות את האות
כדי לבדוק האם הממצאים עשויים להיות רלוונטיים לבני אדם, המחברים בחנו רקמות ריאה ממנותחים להסרת גידול ריאתי. הם השוו דגימות מאנשים עם יכולת חילוף גזים טובה לאלה עם אמפיזמה משמעותית. רמות החלבון IRF5 היו גבוהות באופן ניכר בריאות מקבוצת האמפיזמה. למרות שהמחקר לא היה גדול דיו כדי לקשור במדויק את IRF5 לחומרת תסמינים או להתפרצויות, התבנית תאמה את הממצאים בעכבר: יותר IRF5 בריאות חולות, פחות בריאות בריאות יותר.
מה זה עשוי לסמל לטיפולים עתידיים
ביחד, העבודה מציירת את IRF5 כמארגן מרכזי של נזק ריאתי מונע‑עשן. הוא ממריץ מנוע מוות תאי שמרכזו NLRP3 ומסיט את התאים החיסוניים הרחק מאוכלוסיות Ly6C‑גבוהות שנראות כמסייעות לשמר את מבנה הנאדיות. עבור מטופלים, ההשלכה ברורה: תרופה הממתנת את פעילות IRF5 עשויה, בתיאוריה, להפחית את הצורות ההרסניות ביותר של הדלקת מבלי לכבות לחלוטין את מערכת החיסון. למרות שעדיין אין טיפולים כאלה ל‑COPD, המחקר מספק מטרה מולקולרית ברורה ודרך ביולוגית סבירה לעבר טיפולים שעושים יותר מאשר לפתוח דרכי נשימה צרים — הם עשויים באמת להגן על השלד העדין של הריאה.
ציטוט: Heo, SH., Park, S.Y., Kim, N.H. et al. Interferon regulatory factor 5 involves the pathogenesis of emphysema through NLRP3 and Ly6C expressing cells. Exp Mol Med 58, 425–435 (2026). https://doi.org/10.1038/s12276-025-01632-9
מילות מפתח: אמפיזמה, מחלת ריאות חסימתית כרונית (COPD), דלקת, חיסון ריאתי, מוות תאי